Clear Sky Science · tr
STING, TOX ile birlikte HO-1 ekspresyonunu baskılayarak tümör içi CD8+ T hücresinde ferroptoza yol açar ve immünoterapi direncini tetikler
Bu araştırma kanser tedavisi için neden önemli
Modern kanser immünoterapileri, vücudun kendi öldürücü T hücrelerini serbest bırakarak çalışır; yine de birçok tümör bu hücreleri susturmanın yollarını bulur. Bu çalışma, tümörlerin kullandığı CD8+ “öldürücü” T hücreleri içindeki gizli bir kendini yok etme anahtarını ortaya koyuyor ve bu anahtarı kapatmanın immünoterapinin etkinliğini nasıl önemli ölçüde artırabileceğini gösteriyor.
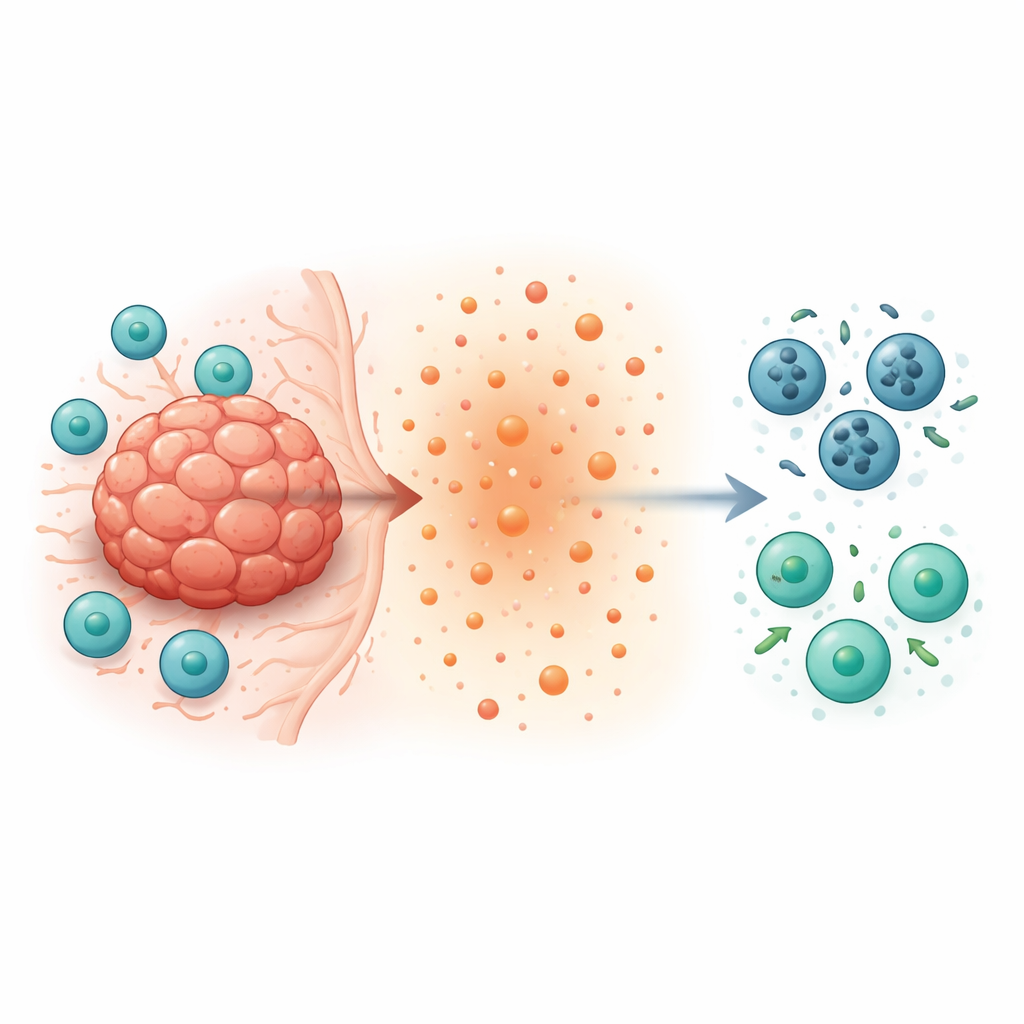
Tümörle savaşan T hücreleri içinde gizli bir ölüm yolu
Tümör içinde CD8+ T hücreleri kanser hücrelerini avlayıp yok etmeli. Ancak sıklıkla nadir, yavaş ve kısa ömürlü hale gelirler. Yazarlar, T hücreleri içindeki iki moleküle—DNA hasar sensörü STING ve T hücre bitkinliğiyle ilişkilendirilen protein TOX—a odaklandı. CD8+ T hücrelerinden STING, TOX veya her ikisi eksik olan fareler oluşturup çeşitli tümörleri naklettiler. Sürpriz biçimde, T hücreleri STING veya TOX eksik olan fareler tümörleri çok daha iyi temizledi. Bu farelerde tümörler daha yavaş büyüdü, çok daha fazla CD8+ T hücresi barındırdı ve bu T hücreleri interferon-gama ve granzyme B gibi daha fazla kanser öldürücü molekül üretti. Bu, tümör içindeki T hücrelerini sessizce sabote eden içsel bir programın varlığına işaret etti.
Demir kaynaklı hücre ölümü bağışıklığı nasıl zayıflatır
Tümör nüfuzlu T hücrelerdeki gen etkinliğini inceleyerek araştırmacılar, tümör içindeki normal T hücrelerinin ferroptoza, yani belirli bir hücre ölümü biçimine yatkın olduğunu buldu. Apoptozdan farklı olarak, ferroptoz demir aşırı yüklenmesi ve hücre zarlarındaki hasarlı yağların birikmesiyle tetiklenir. Tümör hücrelerine maruz kalan sıradan CD8+ T hücrelerinde demir birikimini ve lipid hasarını teşvik eden genler açılırken koruyucu genler kapanmıştı. Buna karşılık, STING- veya TOX-eksik T hücreleri ters paterni gösterdi: daha fazla koruyucu enzim HO-1 ve GPX4 ifade ettiler, daha düşük demir seviyelerine, daha az lipid peroksidasyona, daha sağlıklı mitokondrilere sahip oldular ve ferroptotik ölüme dirençliydiler. Laboratuvar testleri, ferroptozu kimyasal olarak engellemenin normal T hücrelerini hayatta tuttuğunu, oysa STING veya TOX’un uzaklaştırılmasının onları doğal olarak dirençli hale getirdiğini doğruladı.
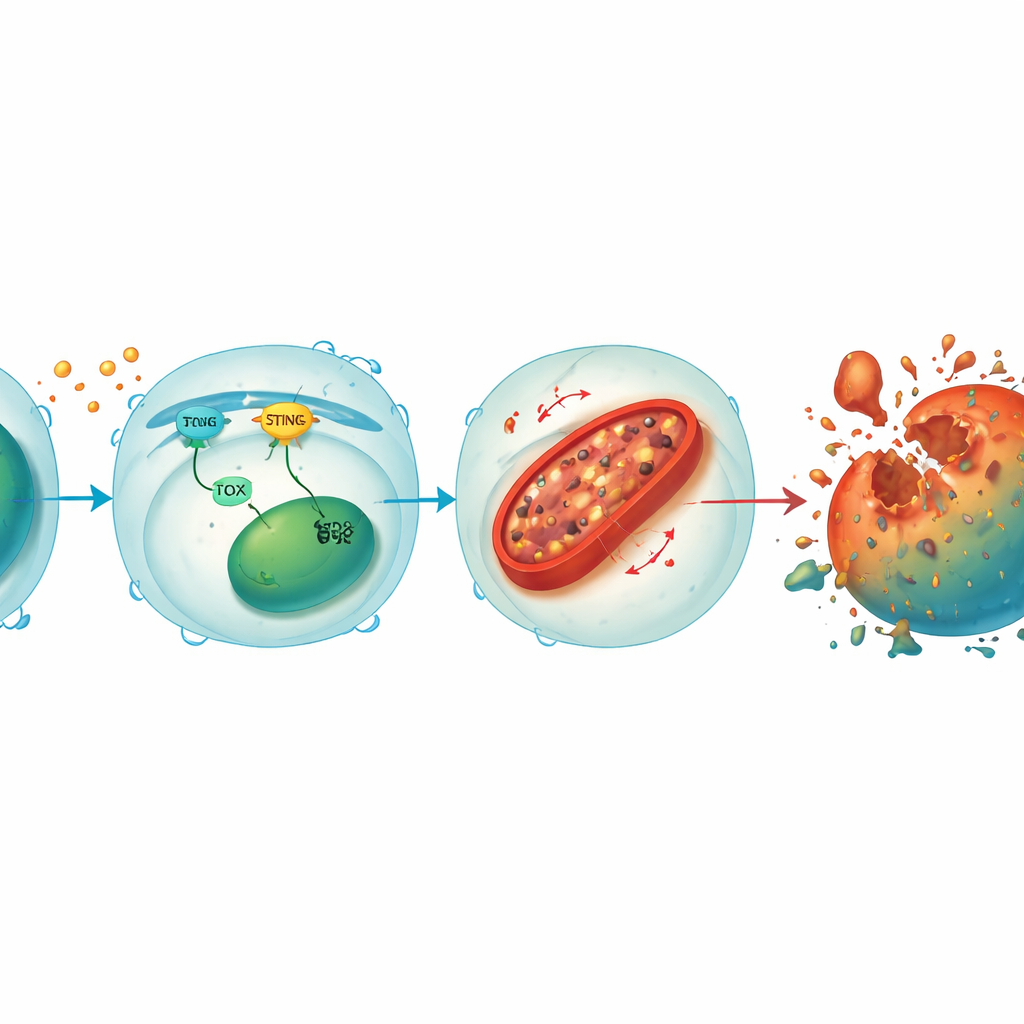
Stres sinyallerini mitokondri hasarına bağlayan bir döngü
Daha derinlemesine incelendiğinde, ekip STING ve TOX’un CD8+ T hücreleri içinde birbirini güçlendiren bir döngü oluşturduğunu keşfetti. Tümör veya viral sinyaller STING’i aktive ettiğinde, TOX’u artıran aşağı akış faktörlerini tetikliyor; TOX ise sırayla STING aktivitesinin sürdürülmesine yardımcı oluyor. Birlikte, normalde hücresel demiri kontrol altında tutmaya yardımcı olan enzim HO-1’i baskılıyorlar. HO-1 baskılandığında, demir mitokondrilerde birikiyor—hücresel enerji santralleri—bu da yüksek düzeyde reaktif oksijen moleküllerine ve zar lipitlerinin oksidasyonuna yol açıyor. Bu mitokondri hasarı enerji üretimini tüketiyor ve sonuçta T hücresini ferroptoza itiyor. Knockout T hücrelerinde STING veya TOX’un yeniden sağlanması demir aşırı yüklenmesi ve hücre ölümünü geri getirdi, oysa HO-1’in daha da azaltılması bile korunan T hücrelerini yeniden savunmasız hale getirdi; bu da HO-1’i bu yıkıcı yolun merkezi frenlerinden biri olarak vurguluyor.
Tümör kaynaklı laktat nasıl tetikleyici olur
Tümör mikroçevresi, kanserin değişmiş metabolizmasının bir yan ürünü olan laktat açısından zengindir. Çalışma, bu laktatın yalnızca metabolik atık olmadığını—T hücrelerinde ferroptoz anahtarını etkin şekilde çevirmeye yardımcı olduğunu gösteriyor. Diğer hücrelere kıyasla CD8+ T hücreleri laktata özellikle duyarlıydı. Laktat, belirli taşıyıcılar aracılığıyla hücre içine girdikçe demir birikimine, mitokondri küçülmesine, mitokondride DNA kaybına ve daha fazla oksidatif hasara neden oldu. Aynı zamanda laktat STING ve TOX aktivitesini artırdı ve HO-1’i daha da baskıladı. STING veya TOX eksik T hücreleri laktat kaynaklı hasara çok daha dirençliydi. Bir ilacı (AZD3965) kullanarak anahtar bir laktat taşıyıcısını engellemek, farelerde CD8+ T hücrelerini ferroptozdan korudu, tümör içindeki varlıklarını artırdı ve tümör büyümesini yavaşlattı; bu, T hücrelerinde genetik olarak STING’in silinmesinin sağladığı faydayı taklit etti.
Bir zaafı terapötik avantaja çevirme
Bu mekanistik bulguların pratik çıkarımları var. Araştırmacılar adoptif hücre tedavisi—laboratuvarda aktive edilmiş T hücrelerin farelere verilmesi—kullandıklarında, STING veya TOX eksik olacak şekilde tasarlanmış T hücrelerinin normal T hücrelerine göre çok daha güçlü tümör kontrolü sağladığını gördüler. Dahası, bu “ferroptoz dirençli” T hücreleri mevcut tedavilerle—PD-1 veya TIM-3 kontrol noktası inhibitörleri, sisplatin kemoterapisi veya STING aktive edici bir ilaç gibi—birleştirildiğinde, tek tek herhangi bir terapiden çok daha belirgin tümör küçülmesi sağlandı. Son olarak, serviks kanseri hastalarından alınan tümör örneklerinde, tümör nüfuzlu lenfositlerde daha yüksek TOX ve daha düşük HO-1 seviyeleri daha kötü sağkalımla ilişkiliydi; bu da bu yolun insanlar üzerindeki klinik sonuçları şekillendirdiğini düşündürüyor.
Gelecekteki kanser bakımına etkileri
Basitçe söylemek gerekirse, çalışma tümörlerin en etkili kanserle savaşan T hücrelerimizi içten paslandırarak demirle beslenen bir hücre ölümü biçimine zorlayabildiklerini ortaya koyuyor. Bir laktat–STING–TOX devresi HO-1’ün sunduğu korumayı düşürüyor, mitokondrileri hasara uğratıyor ve ferroptoza yol açarak etkili CD8+ T hücrelerinin sayısını azaltıyor. Bu devreyi bozmak—STING veya TOX eksik olacak şekilde T hücreleri tasarlamak, HO-1’i artırmak ya da laktat girişini engellemek—T hücrelerini canlı, enerjik ve saldırıya hazır tutuyor. Bu çalışma, T hücrelerinin metabolik ve genetik ayarlaması ile mevcut ilaçları birleştiren bir sonraki nesil immünoterapilere yönelik yolları işaret ediyor; böylece direnç aşılabilir ve daha kalıcı kanser kontrolü sağlanabilir.
Atıf: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Anahtar kelimeler: kanser immünoterapisi, CD8 T hücreleri, ferroptoz, tümör mikroçevresi, STING TOX HO-1 yolu