Clear Sky Science · tr
Seq-Scope-eXpanded: optik çözünürlüğün ötesinde mekansal omikler
Hücreleri Daha Keskin Görmek
Vücudumuz, güçlü mikroskoplarla bile genellikle göremediğimiz yoğun bir etkinlikle dolu sayısız küçük hücreden oluşur. Bu makale, araştırmacıların dokuların iç işleyişini eşi benzeri görülmemiş bir netlikle yakınlaştırmasını sağlayan Seq-Scope-X adlı bir teknolojiyi tanıtıyor; hangi genlerin ve proteinlerin hücrelerin içinde ve arasında kesin noktalarda aktif olduğunu haritalıyor. Bu düzeyde ayrıntı, gelişim, bağışıklık sistemi ve kanser veya karaciğer hasarı gibi hastalıkların incelenme biçimini değiştirebilir.
Molekülleri Yerinde Neden Haritalayalım?
Hücreler izolasyon içinde çalışmaz: mahalleler halinde yaşar, katmanlar oluşturur ve bulundukları yere göre uzmanlaşırlar. Geleneksel gen dizileme yöntemleri dokuları parçalara ayırır, bu mekansal bağlamı kaybettirir. Daha yeni “mekansal omikler” araçları molekülleri yerinde tutuyor, ancak bir ödünleşme vardı. Görüntülemeye dayalı yöntemler çok ince ayrıntı görebilir ama genellikle yalnızca sınırlı sayıda geni izler. Dizilemeye dayalı yöntemler neredeyse tüm genleri aynı anda okuyabilir, ancak ince ayrıntıları bulanıklaştırır; çoğunlukla sinyalleri birkaç mikrometre boyunca yayar—bu da birçok hücresel alt yapının boyutundan büyüktür. Yazarlar bu boşluğu kapatmayı amaçladı: dizilemenin zengin ve önyargısız okumasını korurken, modern mikroskopların keskinliğine ulaşmak veya onu aşmak.
Optik Sınırları Yenmek İçin Dokuyu Germe
Seq-Scope-X’in temel fikri aldatıcı biçimde basit: dokuya nazikçe büyüklük kazandırmak, böylece yapının her orijinal nanometresi çözülmesi daha kolay hale gelir. Ekip önce RNA moleküllerini—veya antikorlara bağlanmış özel DNA etiketlerini—doku diliminin etrafında inşa edilen yumuşak bir hidrojel içine sabitleyor. Ardından orijinal dokuyu sindirip uzaklaştırıyor ve jelı tuzlu bir çözelti içinde şişirerek her şeyi yaklaşık üç kat fiziksel olarak geriyor, göreli konumları neredeyse korunuyor. Bu genişletilmiş jel, yakalama problarıyla kaplı ultra yoğun bir dizileme çipinin üzerine yerleştiriliyor. Montajı dikkatlice ısıtarak, sabitlenmiş moleküller jelden serbest bırakılıp çipe yeniden bağlanıyor; çip daha sonra hangi genlerin veya proteinlerin her küçük koordinatta bulunduğunu ortaya çıkaracak şekilde dizilenebiliyor. 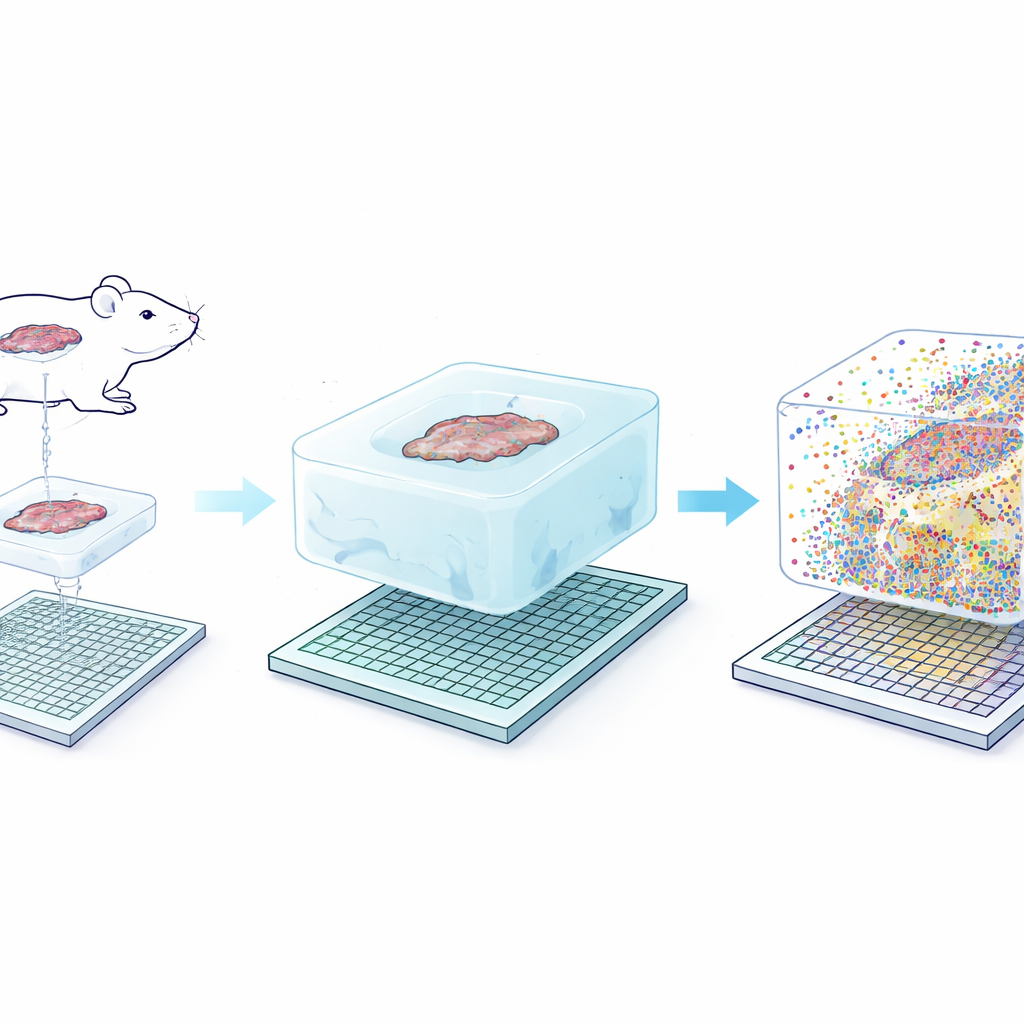
Bulanık Hücrelerden Hücresel Alt Haritalara
Araştırmacılar Seq-Scope-X’i fare karaciğerine uyguladıklarında, yöntemin mekansal çözünürlüğü yaklaşık 0,6 mikrometreden yaklaşık 0,2 mikrometreye kadar keskinleştirdiğini ve milimetrekare başına ölçülebilir pozisyon sayısını neredeyse on kat artırdığını buldular. Pratik olarak, daha önce bulanık lekeler gibi görünen sinyaller artık bireysel hücrelerin net konturlarına dönüştü. Daha da çarpıcı olarak, henüz tam işlenmemiş RNA kümeleri (işlenmemiş/unspliced) çekirdek merkezleriyle sıkıca hizalanırken, olgun RNA (spliced) çevresindeki sitoplazmayı izliyordu. Bu, yazarların yalnızca RNA kullanarak hücre sınırlarını çizmesine ve dokudaki neredeyse her hepatosit için çekirdek ve sitoplazmik gen okumalarını ayırmasına olanak sağladı; önceki dizileme tabanlı yöntemler bunun sadece ipucunu verebiliyordu.
Bölünmüş Kişilikli Hücreler
Bu yeni netlikle ekip, karaciğer hücreleri içinde beklenmedik bir moleküler “çifte hayat” biçimi keşfetti. Karaciğer lobülündeki portal taraftaki kan damarlarından santral tarafa doğru bilinen gradyan boyunca hepatositler farklı metabolik görevlerde uzmanlaşır. Seq-Scope-X, birçok hücrede çekirdekteki gen deseni ile çevreleyen sitoplazmadaki desenin eşleşmediğini gösterdi. Yaklaşık her üç hepatositten biri, çekirdek profili bir bölge ile hizalanmışken sitoplazmik profili komşu bir bölgeyle hizalanmış görünüyordu. MERFISH ve tek molekül RNA flüoresan assayı gibi bağımsız görüntüleme tabanlı yöntemler, bireysel transkriptlerin ya çekirdekte ya da sitoplazmada yoğunlaşabildiğini doğruladı. Birlikte bu bulgular, hepatositlerin zaman içinde metabolik rollerini dinamik olarak değiştirebildiğini; çekirdeğin gelecekteki bir duruma hazırlanırken sitoplazmanın mevcut durumu yansıttığını öne sürüyor. 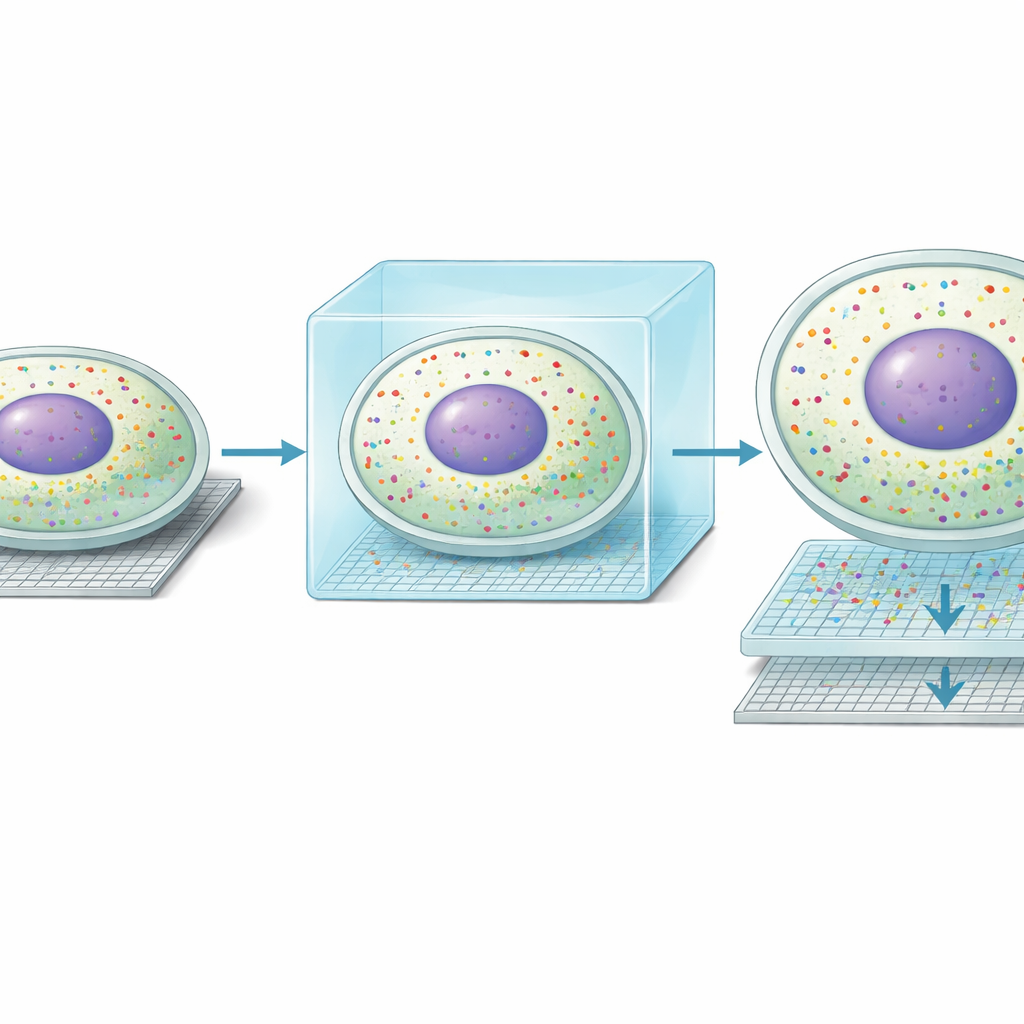
Karaciğerin Ötesinde: Beyin, Bağırsak ve Bağışıklık Dokuları
Yazarlar daha sonra Seq-Scope-X’in diğer organlarda da işe yarayıp yaramadığını test ettiler. Beyinde, farklı nöron tiplerini ve destek hücrelerini temiz biçimde ayırdı ve çekirdek çevresinde subhücresel RNA desenlerini ortaya çıkardı. Kolonda, kript-yüzey ekseni boyunca farklı goblet hücre alt tiplerini ve kolonosit katmanlarını çözdü; yine nükleer imzaları yakaladı. Belki de en çarpıcı şekilde, ekip yöntemi proteinlere uyarlayarak fare dalak ve insan bademcikte DNA barkodlu antikorlar kullandı. Seq-Scope-X, yüzün üzerinde farklı hücre yüzeyi belirtecini tek hücre çözünürlüğünde aynı anda haritalayabildi; sıkıca paketlenmiş T ve B hücre alt kümelerini ve miyeloid hücreleri ayırt etti. Daha genişletilebilir jel kimyasına geçerek, etkin çözünürlüğü gerçek nanoskala doğru ittiler, aynı zamanda doku mimarisini ayrıntılı haritalama için yeterince korudular.
Geleceğe Dair Anlamı
Seq-Scope-X, dizilemeden önce dokuları fiziksel olarak büyütmenin uzun süredir devam eden çözünürlük sınırlarını aşabileceğini, binlerce gen veya protein etiketini aynı anda okurken neredeyse mikroskop seviyesinde ayrıntı sunabileceğini gösteriyor. Bir gözlemci için bunun anlamı şudur: bilim insanları artık hangi hücrelerin nerede olduğunu söylemenin ötesinde, her hücrenin farklı bölgelerinde neler olup bittiğini ortaya koyan “moleküler atlaslar” oluşturabilir. Bu tür haritalar, dokuların yaralanmaya nasıl yanıt verdiğini, bağışıklık hücrelerinin lenfoid organlarda ve tümörlerde nasıl organize olduğunu veya hücre içindeki ince kaymaların hastalığın habercisi olabileceğini açıklamaya yardımcı olabilir. Kapsamı ölçeklendirmek ve bazı boyama panellerini iyileştirmek için daha fazla geliştirme gerekse de, Seq-Scope-X sağlığı ve hastalığı belirleyen mikroskobik manzaralara açılan güçlü yeni bir pencereyi aralıyor.
Atıf: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Anahtar kelimeler: mekansal transkriptomik, doku genişletme, tek hücreli omikler, mekansal proteomik, karaciğer zonasyonu