Clear Sky Science · tr
Bağırsak mikrobiyotası kaynaklı IPA, mukozal iyileşmeyi kolaylaştırmak için bağırsak HMGCS2 aracılı ketojenezi düzenleyerek koliti korur
Neden Bağırsak Bakterileri Yaralı Bağırsak İçin Önemlidir
Bağırsak yüzeyi, inflamatuar barsak hastalığı (İBH) veya agresif tıbbi tedaviler sonrasında zarar gördüğünde, zararlı maddelerin kan dolaşımına sızmasını önlemek için vücut bu iç “deriyi” hızla onarmalıdır. Bu çalışma, dost bağırsak bakterileri tarafından üretilen tek bir molekülün bağırsağın kendi kendini iyileştirmesine nasıl yardımcı olabileceğini ortaya koyuyor ve bağışıklık sistemini geniş çapta baskılamadan kronik bağırsak hastalıklarını tedavi etmenin yeni yollarına işaret ediyor.
Dost Mikroplardan Yararlı Bir Sinyal
Araştırmacılar, İBH’li kişiler ve sağlıklı gönüllülerin dışkı örneklerinden ile birkaç kolit fare modelindeki kimyasal parmak izlerini karşılaştırmakla başladılar. Yüzlerce molekül arasında öne çıkan bir tanesi vardı: indol-3-propiyonik asit (IPA), belirli bağırsak bakterileri tarafından diyetik amino asit triptofandan üretilen bir yıkım ürünü. IPA düzeyleri Crohn hastalığı olan insanlarda ve kolitli farelerde sağlıklı bireylere göre sürekli olarak daha düşüktü. Bu durum, IPA kaybının bağırsak yüzeyi iltihaplandığında ve onarımı başarısız olduğunda işleyen mekanizmalardan biri olabileceğini düşündürdü.
Bağırsak Koruyucu Duvarını Güçlendirmek
IPA’nın sadece hastalığı izleyip izlemediğini yoksa gerçekten koruma sağlayıp sağlamadığını test etmek için ekip, kimyasal kolit ve radyasyon hasarı dahil olmak üzere çeşitli bağırsak yaralanmaları oluşturulmadan önce farelere IPA verdi. Yeterli dozda IPA alan farelerin kolonları daha uzun ve daha sağlıklıydı, mikroskop altında daha az inflamatuar değişiklik vardı ve daha kalın bir mukus tabakası ile daha sıkı hücre birleşimleri görülüyordu. Daha az inflamatuar belirteç sızdırdılar ve koruyucu mukus üreten goblet hücreleri daha fazlaydı. Önemli olarak, bu faydalar yerleşik bir mikrobiyomu olmayan kafesiz (germ-free) farelerde bile görüldü; bu da IPA mevcut olduğunda diğer mikroplara ihtiyaç duymadan doğrudan bağırsak yüzeyinde etkili olabileceğini gösterdi.
Kök Hücreleri Özel Bir Enerji Türüyle Beslemek
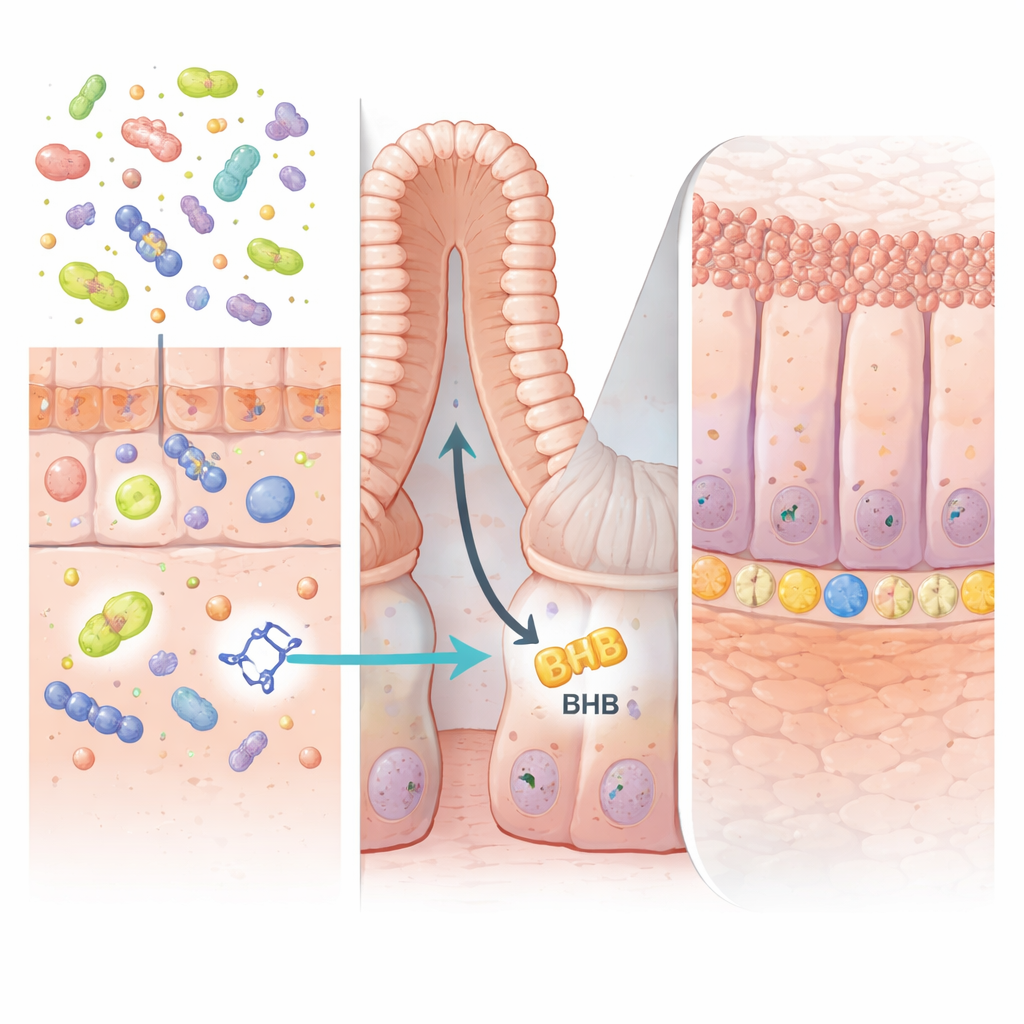
IPA’nın etkisinin anahtarı, kök hücrelerin oturduğu ve sürekli olarak yüzeyi yenilediği küçük cepler olan bağırsak “kriptilerinin” derinliğinde yattı. Yazarlar, IPA’nın bağırsak epitel hücrelerinde PPARα adlı bir proteini aktive ettiğini gösterdi. Bu da HMGCS2 adı verilen bir enzimin üretimini artırıyor; HMGCS2 ketojenezi—enerji açısından zengin molekül β‑hidroksibütiratın (BHB) üretim sürecini—sürdürüyordu. Bağırsak duvarındaki yükselmiş BHB, LGR5-pozitif kök hücreleri uyararak hasarlı dokuyu daha hızlı rejenerasyon için genişletti. Farelerde intestinal hücrelerden seçici olarak HMGCS2 enzimi veya PPARα çıkarıldığında, IPA artık kök hücre aktivitesini artıramadı veya kolite karşı koruma sağlayamadı; bu da keton üreten yolun vazgeçilmez olduğunu doğruladı.
Bakteri Fabrikalarından İnsan Dokularına
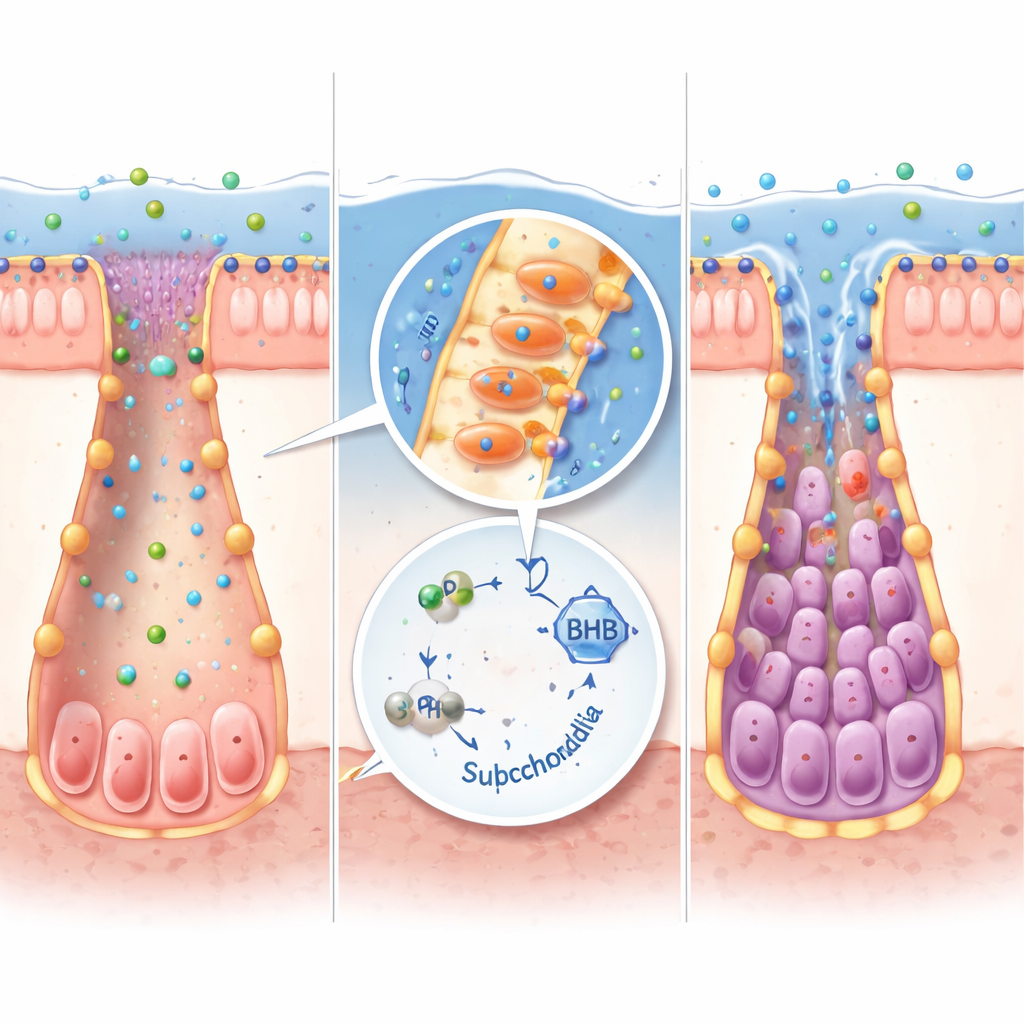
Tüm bağırsak bakterileri IPA üretemez. Büyük mikrobiyom veri setlerini yeniden analiz ederek araştırmacılar, birkaç İBH kohortunda azalmış olan önemli bir IPA üreticisi olarak Peptostreptococcus russellii’yi tanımladılar. Laboratuvar kültürlerinde bu bakteri triptofandan IPA’ya verimli şekilde dönüştürdü. Kafesiz fareler P. russellii ile kolonize edildiğinde IPA düzeyleri yükseldi, keton üreten genler açıldı, kök hücre belirteçleri arttı ve kolit şiddeti genel bir mikrobiyal transplantasyon alan farelere göre düştü. Aynı IPA–keton yolu, fare ve insan dokularından büyütülen mini bağırsak organoidlerinde de çalıştı; burada IPA veya BHB eklenmesi, inflamatuar hasardan sonra kök hücrelerin toparlanmasına yardımcı olurken pro-inflamatuar sinyalleri azaltıyordu.
Gelecekteki Tedavi İçin Ne Anlama Gelebilir
Toplu halde ele alındığında, çalışma basit ama güçlü bir olay zincirini özetliyor: belirli bağırsak bakterileri diyetik triptofandan IPA üretir; IPA bağırsak hücrelerinde bir metabolik anahtarı aktive eder; bu anahtar BHB üretimini artırır; ve BHB, bağırsak yüzeyini yeniden inşa eden kök hücreleri canlandırır. İBH veya bağırsak bariyerine zarar veren diğer durumları olan kişiler için IPA’yı geri kazandıran veya etkilerini güvenli biçimde taklit eden —beslenme, hedefe yönelik probiyotikler veya tasarım ilaçlar aracılığıyla— terapiler gerçek mukozal iyileşmeyi geniş bağışıklık baskısı olmadan teşvik edebilir. Hastalarda daha fazla çalışmaya ihtiyaç duyulsa da, bu mikroorganizma–metabolit–kök hücre ekseni bağırsakları içeriden onarmak için umut verici yeni bir yaklaşım sunuyor.
Atıf: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Anahtar kelimeler: bağırsak mikrobiyomu, bağırsak kök hücreleri, inflamatuar barsak hastalığı, mikrobiyal metabolitler, mukozal iyileşme