Clear Sky Science · tr
CD38, mitofaji yoluyla MAVS’ı parçalayarak nazofaringeal karsinom hücrelerinde tip I interferon salgısını engelliyor ve CD8+ T hücre kaynaklı antitumör bağışıklığını zayıflatıyor
Kanser tedavisi açısından neden önemli
Nazofaringeal karsinom, burun arkasında gelişen ve özellikle Doğu ve Güneydoğu Asya’da yaygın olan bir kanser türüdür. Vücudun kendi T hücrelerini serbest bırakan immün tabanlı ilaçlar bazı hastaların prognozunu değiştirdi, ancak çoğu hasta yine de fayda görmüyor. Bu çalışma, tümör hücrelerinin içinde gizli bir frenin varlığını ortaya koyuyor: CD38 adlı bir molekül, hücre içi bir alarm sistemini sessizce kapatıyor ve kanser öldürücü CD8 T hücrelerinin saldırısını zayıflatıyor. Bu frenin anlaşılması ve devre dışı bırakılması, mevcut immünoterapilerin çok daha fazla hasta için işe yaramasını sağlayabilir.
Tümör hücrelerinde gizli bir anahtar
Araştırmacılar, birçok immün hücrede bulunan ancak nazofaringeal karsinom hücrelerinde de mevcut olan bir protein olan CD38’e odaklandı. Önceki çalışmalar CD38’i PD-1 ve PD-L1 hedefli popüler kontrol noktası ilaçlarına dirençle ilişkilendirmişti. Burada ekip, tümör hücreleri içindeki CD38’in CD8 T hücrelerinin bu hücreleri tanıma ve yok etme yeteneğini doğrudan değiştirip değiştirmediğini sorguladı. İnsan tümör hücrelerini CD38’li veya CD38’siz olarak aktive edilmiş insan CD8 T hücreleriyle birlikte yetiştirerek, CD38’i çıkarıldığında T hücrelerinin çok daha etkili olduğunu buldular: anahtar saldırı moleküllerini daha yüksek düzeyde salgıladılar, daha iyi hayatta kaldılar ve daha fazla tümör hücresini öldürdüler. CD38 geri eklendiğinde T hücresi fonksiyonu düştü; bu da CD38’i tümör-kaynaklı bir immün saldırı baskılayıcısı olarak işaretliyor.
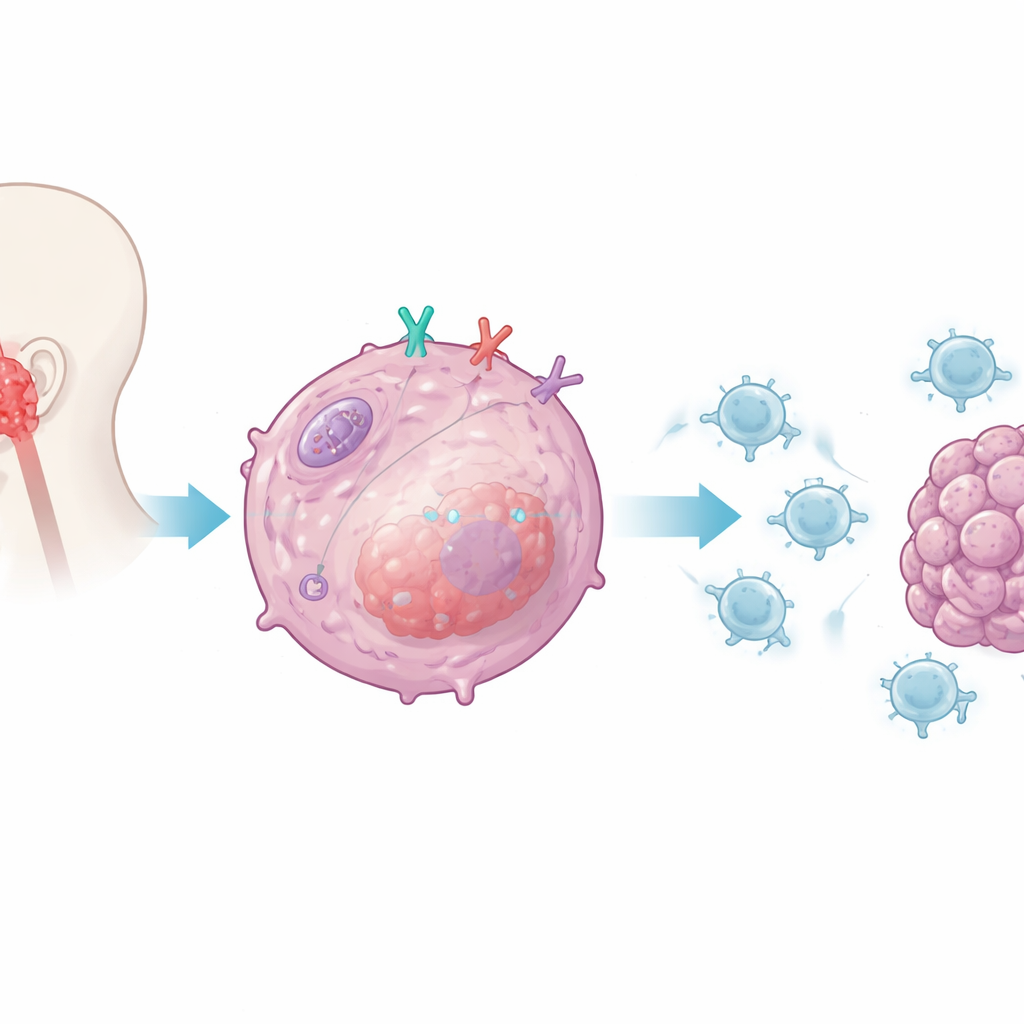
Hücresel iç alarmı kısma
Araştırma ekibi daha sonra CD38’in bu baskılayıcı sinyali nasıl ilettiğini inceledi. Odaklandıkları hedef, normalde virüse benzer genetik materyali algılayıp tip I interferonları—güçlü immün uyarıcı haberci moleküller—tetikleyen tümör hücresinin doğuştan gelen alarm sistemiydi. CD38 eksik tümör hücrelerinde, araştırmacılar interferon-beta ve CD8 T hücrelerini tümöre çeken kemokinlerde güçlü bir artış gözlemledi. CD38’in özellikle RIG-I adlı iç sensör ve onun adaptör proteini MAVS tarafından kontrol edilen yolu baskıladığını gösterdiler; MAVS mitokondrilerde, hücrenin enerji fabrikalarında bulunur. CD38 bulunduğunda bu yolun aktivasyonu ve aşağıdaki sinyal molekülleri zayıflıyordu; CD38 çıkarıldığında ise sinyal ve interferon üretimi yükselerek tümörün immün sistem tarafından daha görünür hale gelmesini sağlıyordu.
CD38, önemli bir sinyal merkezini nasıl yok ediyor
Daha derine indiklerinde, bilim insanları CD38’in mitokondride MAVS ile fiziksel olarak etkileştiğini ve MAVS’ın RIG-I ile ortak çalışmasını bozduğunu, böylece sinyal iletimini zayıflattığını buldular. Daha çarpıcı olarak, yüksek CD38 düzeyleri MAVS proteininde azalmaya yol açtı ancak MAVS’ın genetik ifadesi değişmedi; bu aktif bir yok oluşu işaret ediyordu. Farklı inhibitörlerle yapılan testler, bu kaybın hücrenin geri dönüşüm mekanizması olan otofajiye ve özellikle mitokondrilere yönelik bir otofaji biçimine bağımlı olduğunu gösterdi. CD38, mitokondri “öz-çilmesini” (mitofaji) belirten işaretleri artırdı, çeşitli mitokondri proteinlerini azalttı ve MAVS’ın daha sonra parçalanan otofagozom yapılar içine paketlenmesini teşvik etti. Mitokondri otofajisini engellemek MAVS’ı korudu ve interferon sinyalini geri getirdi; bu da CD38’in MAVS’ı hücrenin atık akışına sürükleyerek alarmı devre dışı bıraktığını gösteriyor.
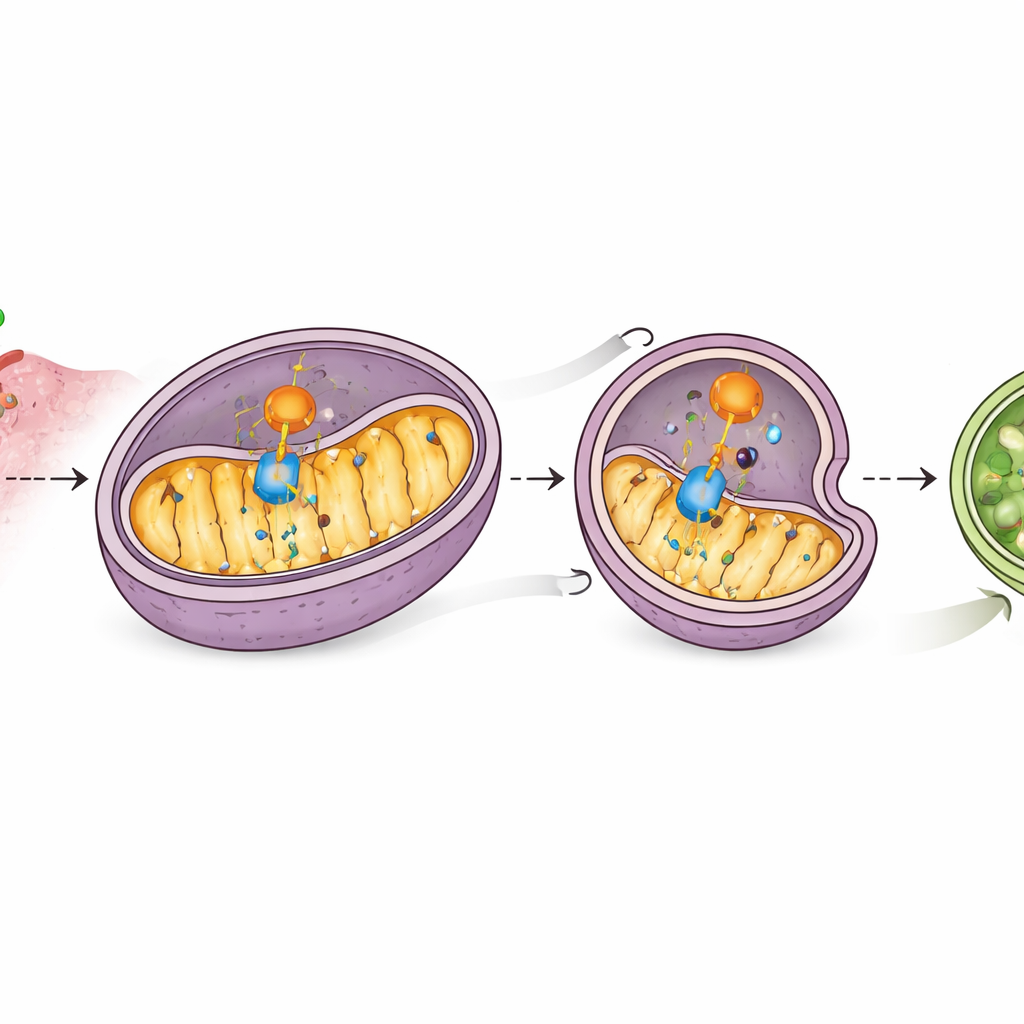
Mitokondrileri kendi kendini yok etmeye yönlendiren bir yardımcı
Çalışma ayrıca, hedefe yönelik mitokondri temizliğinde bir reseptör görevi gören mitokondri içi bir protein olan PHB2’yi tanımladı. Kütle spektrometrisi ve bağlanma deneyleri, CD38’in PHB2 ile etkileştiğini ve PHB2’nin mitokondrilerdeki varlığını artırdığını; burada PHB2 de çekirdek otofaji makinesini işe çağırıyordu. PHB2 ayrıca MAVS’a bağlanıyor ve CD38 bu temasları güçlendiriyordu. PHB2 azaltıldığında CD38 artık mitokondri otofajisini etkili şekilde tetikleyemedi, MAVS düzeyleri geri döndü ve interferonla ilişkili genler yeniden aktifleştirildi. Bu, CD38’in PHB2’yi devreye soktuğu, PHB2’nin MAVS’ı tuttuğu ve birlikte MAVS’ı parçalanmaya gidecek mitokondrilere yönlendirdikleri bir olay zincirini ortaya koyuyor; sonuç interferon alarmının susturulmasıdır.
Hayvan modellerinden kanıt
Canlı organizmalardaki etkisini test etmek için araştırmacılar CD38’den yoksun olacak şekilde tasarlanmış fare tümörleri kullandılar. Bağışıklığı sağlam farelerde bu tümörler daha yavaş büyüdü, daha fazla CD8 T hücresi içerdi ve antitümör yanıtların bir göstergesi olan interferon-gama üreten hücre oranı daha yüksekti. Tip I interferon reseptörünü engellemek bu avantajı ortadan kaldırdı ve interferon sinyalinin güçlendirilmiş bağışıklık için gerekli olduğunu doğruladı. Nazofaringeal tümör taşıyan insanlaştırılmış farelerde CD38’i azaltmak benzer şekilde büyümeyi yavaşlattı ve CD8 T hücresi infiltrasyonunu artırdı; ancak tümör hücrelerinde MAVS da azaltıldığında bu fayda kayboldu. Bu in vivo bulgular, tümör hücreleri içindeki CD38–PHB2–MAVS ekseninin vücudun T hücre yanıtının gücünü şekillendirdiği fikrini pekiştiriyor.
Gelecek terapiler için ne anlama geliyor
Genel olarak çalışma, nazofaringeal karsinom hücrelerindeki CD38’in antitümör bağışıklığının içsel bir sabote edicisi olarak hareket ettiğini gösteriyor. CD38, seçici bir mitokondri geri dönüşümü biçimini tetikleyerek MAVS’ı tüketiyor, tip I interferon üretimini zayıflatıyor, antijen sunumunu düşürüyor ve nihayetinde CD8 T hücresi saldırısını köreltiyor. Mevcut CD38 engelleyici bileşikler ağırlıklı olarak enzim aktivitesini hedefliyor ve proteini ortadan kaldırmıyor ya da MAVS’ı geri getirmiyor. Yazarlar, CD38 düzeylerini azaltmaya veya CD38’in PHB2 ya da MAVS ile ortaklığını bozacak yeni stratejilerin tümör içindeki interferon alarmını yeniden uyandırabileceğini öne sürüyor. Mevcut kontrol noktası inhibitörleriyle birleştiğinde bu yaklaşımlar, daha fazla nazofaringeal — ve muhtemelen diğer — kanserin immün soğuktan immün yanıt verir hale gelmesini sağlayabilir.
Atıf: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Anahtar kelimeler: nazofaringeal karsinom, tümör immünoterapisi, tip I interferon, CD8 T hücreleri, mitofaji