Clear Sky Science · tr
Fosfoproteomik ve kinaz-altı bir etkileşimleri kullanarak EGF sinyal yolunun çıkarımını kıyaslama
Laboratuvarın ötesinde neden önemli
Hücrelerimiz çevrelerinden gelen sinyalleri sürekli dinler ve bunlara yanıt verir. Bu sinyallerin en önemlilerinden biri epidermal büyüme faktörü (EGF) olup hücrelerin nasıl büyüdüğünü, bölündüğünü ve hayatta kaldığını kontrol etmeye yardımcı olur. Bu iletişim sistemi bozulduğunda kanserler ve diğer hastalıkları tetikleyebilir. Bu çalışma, görünüşte basit ama sonuçları büyük olan bir soruyu soruyor: bugünün güçlü ölçüm teknolojilerini ve bilgisayar modellerini kullandığımızda, EGF sinyal yolunu ders kitabı diyagramlarından ne kadar daha iyi anlayabiliriz?
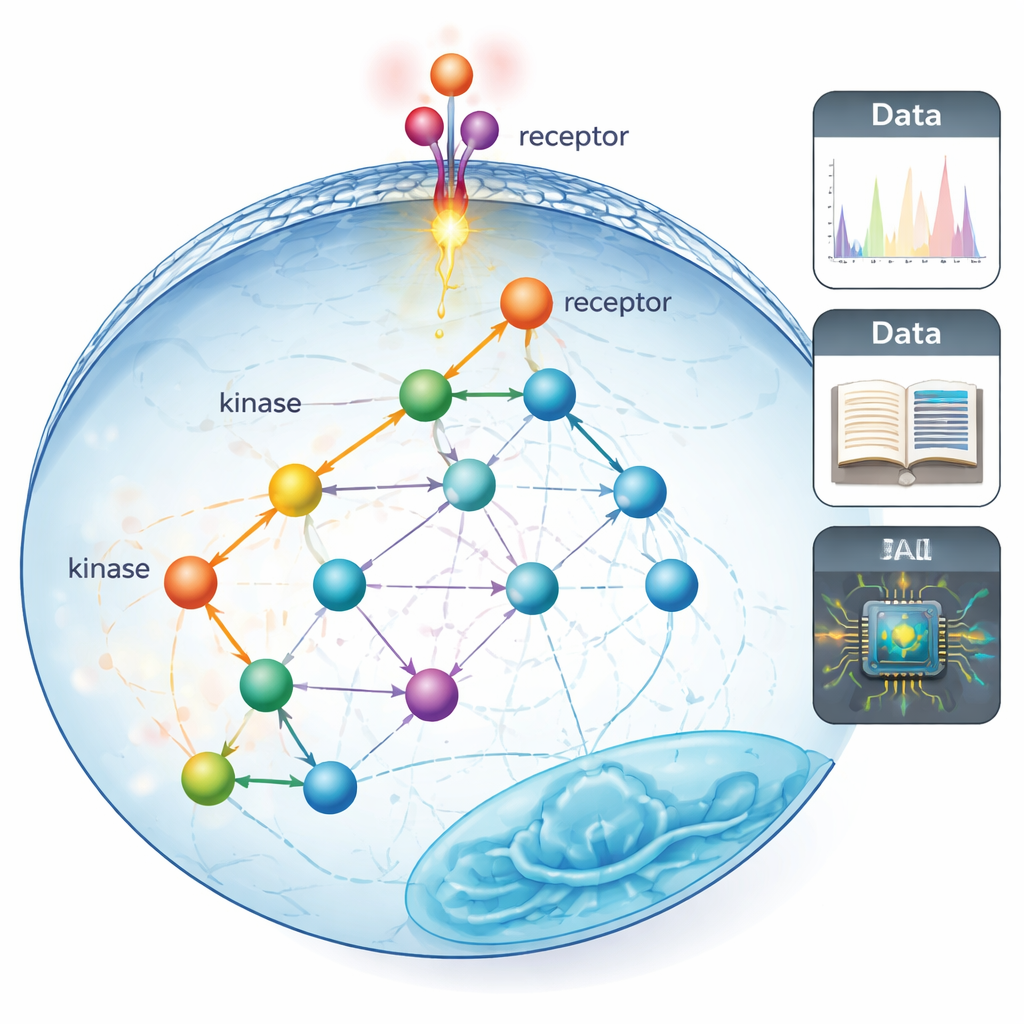
Doğrusal çizgilerden gerçek hayattaki devre şemalarına
Geleneksel “sinyal yolları” genellikle hücre yüzeyinden çekirdeğe mesaj taşıyan düzenli, neredeyse doğrusal protein zincirleri şeklinde çizilir. Bu haritalar, yalnızca bir seferde birkaç proteini inceleyebilen yavaş, hedefe yönelik deneylerle on yıllar boyunca oluşturuldu. Yazarlar, bunun bize dar, sokak lambası tarzı bir görüş bıraktığını savunuyor: çalışması kolay olan birkaç protein hakkında çok şey biliyoruz, oysa gerçek hücrelerde muhtemelen var olan daha geniş bağlantı ağı hakkında çok daha az bilgiye sahibiz.
Aynı anda binlerce moleküler anahtarı dinlemek
Bu sınırlı görüşün ötesine geçmek için ekip, tek bir deneyde on binlerce küçük kimyasal etiket olan fosfat gruplarını proteinler üzerinde izleyebilen bir kütle spektrometresi tekniği olan fosfoproteomik kullandı. Bu etiketler kinaz adı verilen enzimler tarafından konulur ve sinyal için hızlı açık–kapalı anahtarları olarak görev yapar. Araştırmacılar önce literatürden küratörlükle derlenmiş bulguları, protein dizilerini okuyan bir yapay zekâ modelinin tahminlerini ve kinaz tercihlerini gösteren geniş deneysel taramaları birleştirerek bugüne kadar yapılmış en kapsamlı “kim kimi fosforile edebilir” haritalarını oluşturdular. Bu, ölçülebilir bölgelerin bilinen veya şüphelenilen kinaz–substrat ilişkilerinin kapsamını yaklaşık %5 civarından %70–80’e kadar büyük ölçüde genişletti.
Birçok deneyde EGF sinyalini stres-testine sokma
Ardından, akciğer, meme, deri ve beyin kanserlerinde önemli bir yol olan klasik EGF yanıtına odaklandılar. Grup, yayımlanmış üç ileri düzey veri setini, böbrek kökenli hücrelerde alınmış üç yeni, çok derin zaman çözümlemeli ölçüm ile ve farklı uyarıcıların kullanıldığı iki kontrol çalışmasıyla birleştirdi. Bu deneylerin her birinde veri seti başına 40.000’den fazla fosforile olma bölgesi ölçüldü ve EGF uyarımını izleyen dakikalarda bunların nasıl yükseldiği veya düştüğü takip edildi. Genel desenler hücre tipleri ve teknolojiler arasında biraz farklılık gösterse de, EGF yolundaki kilit fosforilasyon bölgeleri tekrar tekrar aktive oldu; bu da çekirdek sinyalin çeşitli deneyler arasında bile sağlam olduğunu doğruluyor.
Kinazlar arasındaki gizli konuşmayı yeniden inşa etmek
Hangi kinazların daha aktif veya daha az aktif hale geldiğini çıkardıktan sonra yazarlar, bunlar arasındaki temel “konuşmayı” yeniden kurmaya çalıştı: hangi kinazların muhtemelen diğerlerini aktive ettiği veya etkilediği. Kinaz–substrat haritalarını kinaz–kinaz ağlarına dönüştürdüler ve basit sıralama düzenlerinden EGF reseptöründe köklenen yönlendirilmiş bir ağa benzemesi için sonucu zorlayan daha karmaşık bir yaklaşıma kadar üç hesaplamalı strateji uyguladılar. Ortaya çıkan çıkarılmış yolları birkaç tür “gerçek” veri ile karşılaştırdılar: bir veritabanından dikkatle küratörlüğü yapılmış bir EGF haritası, tek tek kinazların aşırı eksprese edildiği büyük ölçekli deneyler ve zaman içinde davranışları güçlü şekilde korele olan kinaz bölgesi çiftleri.
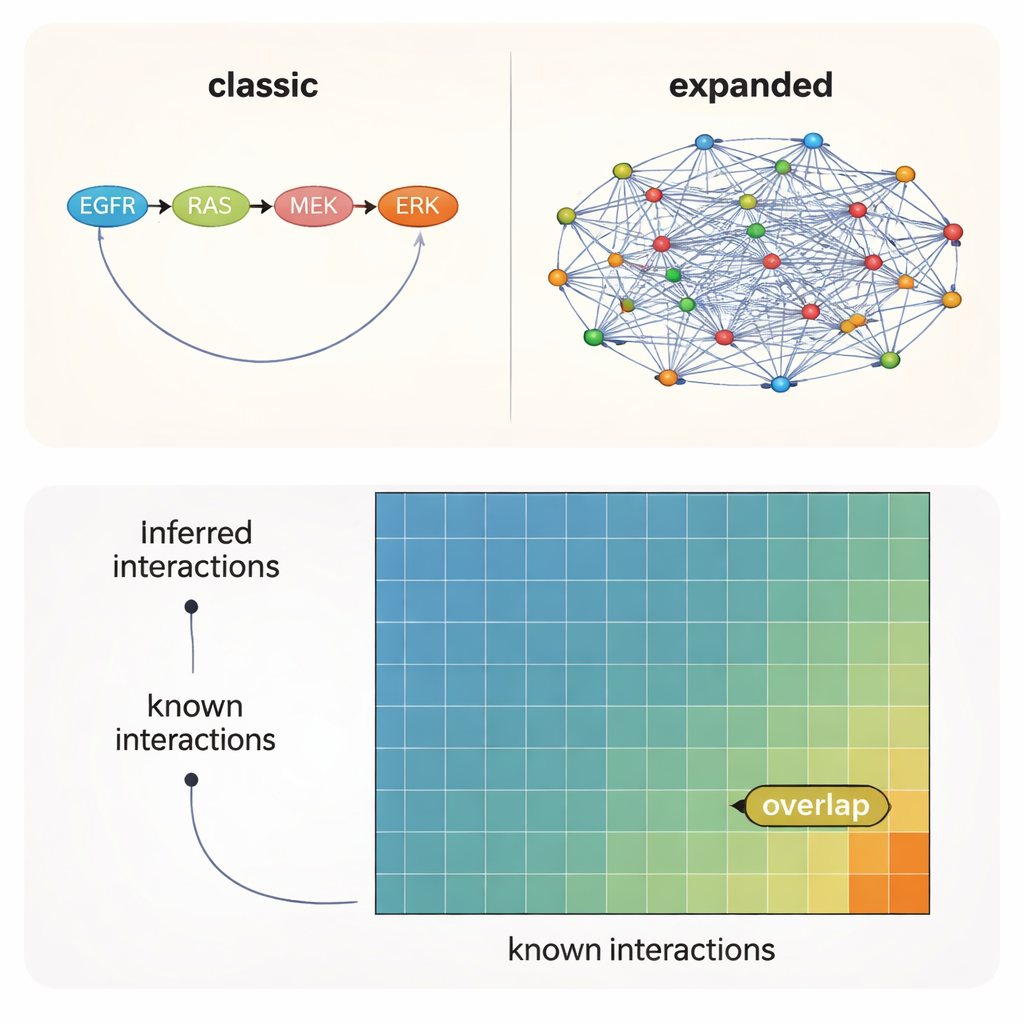
En mantıklı bağlantılar hâlâ resmi haritanın dışında
Tüm testler boyunca bir mesaj netti: başlangıç bilgisi seçimi—algoritmaya hangi başlangıç ağını verdiğiniz—kullandığınız belirli yöntemden veya hatta deneysel bağlamdan daha fazlasıyla önemliydi. Literatürden oluşturulan ağlar bilinen etkileşimlerin en fazlasını geri getirdi; oysa daha geniş öngörücü kaynaklar henüz resmî olarak belgelenmemiş birçok ek, makul bağlantıya işaret etti. Yine de en iyi koşullar altında bile veriler ve modeller tarafından önerilen etkileşimlerin sadece yaklaşık %10–12’si referans setlerin herhangi birinde vardı. Başka bir deyişle, desteklenen kinaz–kinaz bağlantılarının yaklaşık %90’ı haritalanmamış bölgede yer alıyor.
Gelecekteki tedaviler için anlamı
Uzman olmayanlar için çıkarılacak ders, ders kitaplarındaki iyi bilinen EGF yolunun muhtemelen buzdağının sadece görünen kısmı olduğudur. Modern fosfoproteomik ve gelişmiş hesaplamalı yöntemlerin birleşimi çok daha zengin ve karmaşık bir sinyal ağı ortaya koyuyor. Bu yeni önerilen bağlantıların birçoğu, kanser hücrelerinin ilaçlardan kaçmak için sinyalleri yeniden yönlendirdiği gözden kaçmış yolları veya daha akıllı ilaç kombinasyonları tasarlamak için yeni fırsatları temsil edebilir. Çalışma her yeni bağlantının gerçek olduğunu kanıtlamıyor, ancak araştırmacıların bu fikirleri test etmeleri için bir yol haritası ve açık araçlar sağlıyor; nihai amaç, EGF sinyalinin merkezi rol oynadığı hastalıklarda daha hassas ve etkili terapilere ulaşmaktır.
Atıf: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Anahtar kelimeler: EGF sinyalleşmesi, fosfoproteomik, protein kinazlar, hücre sinyal ağları, kanser biyolojisi