Clear Sky Science · tr
Mycobacterium tuberculosis, konakçı ATP6V1E1 fosforilasyonunu düzenleyerek hücre içi hayatta kalmayı destekliyor
Veremle savaşta bunun önemi
Verem, her yıl bir milyondan fazla insanın ölümüne yol açarak dünyanın en ölümcül bulaşıcı hastalıklarından biri olmaya devam ediyor. Bağışıklık hücrelerimiz, normalde saldıran mikropları sindiren güçlü “asitli geri dönüşüm kutuları” ile donatılmıştır. Bu makale, verem bakterisi Mycobacterium tuberculosis (Mtb)’nin hücrelerimiz içindeki bu asitleşme sistemini nasıl sabote ettiğini ortaya koyuyor ve bu hileyi hedef alan bir ilacın enfekte hayvanların enfeksiyonu daha etkili bir şekilde temizlemesine yardımcı olabileceğini gösteriyor.
Hücrenin mikroplar için asit banyosu
Verem bakterileri akciğerlere solunduğunda hızla makrofaj adı verilen bağışıklık hücreleri tarafından yutulur. Bakteriler, lizozomlarla kaynaşması gereken zar keseciklerine düşer—lizozomlar, güçlü asidik ortamda en iyi çalışan sindirici enzimlerle dolu küçük keseciklerdir. Bu asitleşme, protonları lizozomlara itmek ve iç pH’yı düşürmek için hücresel yakıt kullanan vakuolar ATPaz (V-ATPaz) adlı moleküler bir pompa tarafından oluşturulur. Uygun asitleşme Mtb’nin parçalanması için hayati önemdedir, ancak geçmiş on yıllık çalışmalar bu patojenin bir şekilde keseciklerini daha az asidik tuttuğunu ve böylece hayatta kaldığını göstermiştir.
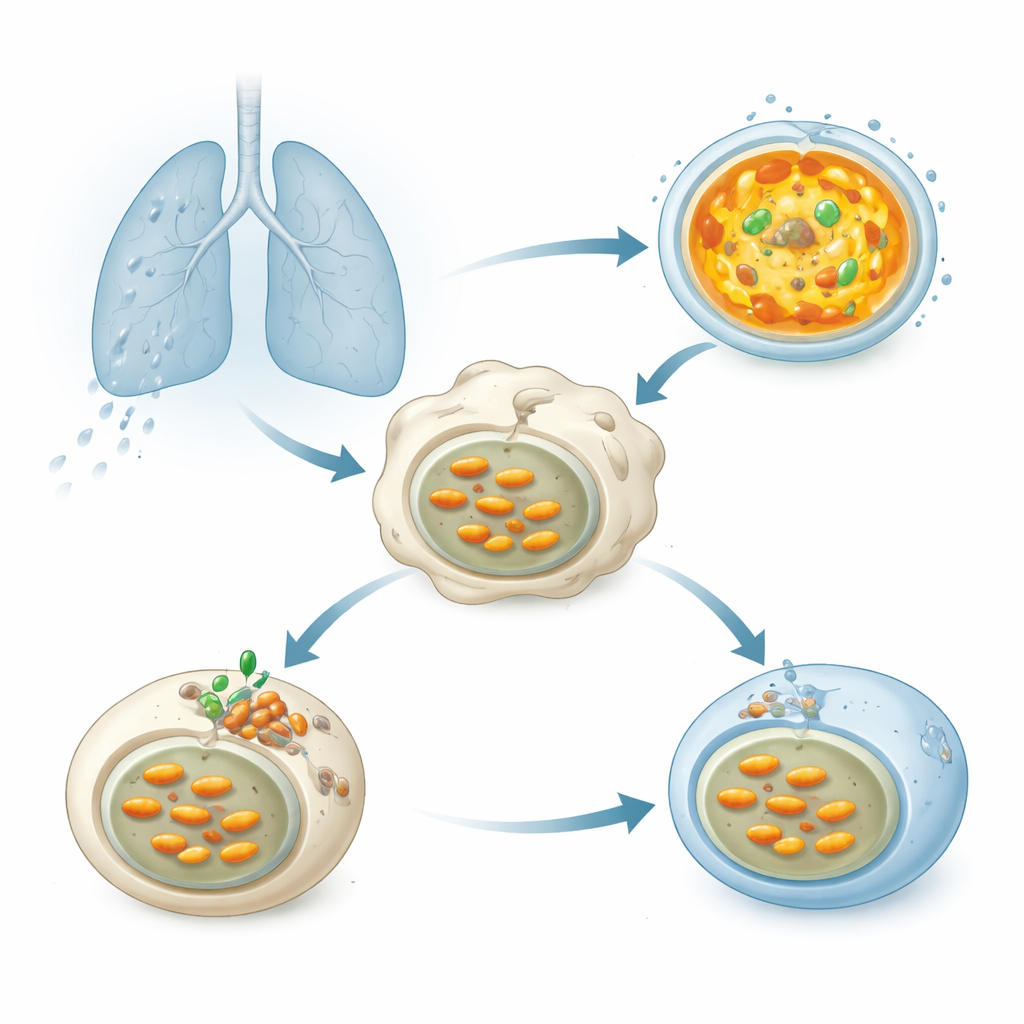
Asitleşmeyi engelleyen gizli bir bakteriyel yardımcı
Araştırmacılar, Mtb’nin salgılayabildiği 200’den fazla proteini tarayarak bunların insan hücrelerinde lizozomal asitleşmeyi zayıflatıp zayıflatmadığını incelediler. Öne çıkan bir tanesi vardı: Chp2 (diğer adıyla Rv1184) adlı bir enzim. Hücreler Chp2 ürettiğinde, lizozomları asit duyarlı boyalarla daha zayıf parlıyordu; bu, daha yüksek ve daha az düşmanca bir pH’ya işaret ediyordu. Chp2’si eksik olarak tasarlanmış Mtb suşları artık asitleşmeyi baskılamıyordu; enfekte makrofajlarda ve farelerde bu mutant bakteriler daha etkili temizlendi ve daha hafif akciğer hasarına neden oldu. Mutant suşa Chp2 yeniden kazandırıldığında hem asitleşme engeli hem de daha yüksek bakteri yükü geri geldi; bu da Chp2’yi Mtb’nin konak hücrelerde sürmesini sağlayan bir virülans faktörü olarak tanımladı.
Kontrol düğmesi gibi davranan konak pompa alt birimi
Chp2’nin asitleşmeye nasıl müdahale ettiğini anlamak için ekip bağlanabileceği konak bileşenlerini aradı. Chp2’nin doğrudan V-ATPaz’ın belirli bir parçasına, pompanın yapısını stabilize etmeye yardımcı olan ATP6V1E1 (kısaca E1) adlı bir alt birime tutunduğunu buldular. Hücrelerde E1 miktarını artırmak lizozomal asitleşmeyi güçlendirdi ve Mtb’nin hayatta kalmasını zorlaştırdı; E1’i azaltmak ise ters etki yaptı. Sadece bir çalışan E1 kopyasına sahip farelerin lizozomları daha az asidikti, akciğerlerindeki bakteri yükleri daha yüksekti ve enfeksiyon sonrası doku hasarı daha şiddetliydi; bu, E1’in vereme karşı önemli bir konak savunucusu olduğunu gösterdi.
Pompadaki kinaz etiketi asidi azaltıyor
Yazarlar daha sonra E1 üzerindeki kimyasal “etiketlerin” pompanın aktivitesini ayarlayıp ayarlamadığını sordular. E1’de iki özel tirozin (Tyr56 ve Tyr57) üzerine fosfat grupları eklemenin bir fren gibi davrandığını keşfettiler: fosforilasyonun taklit edilmesi asitleşmeyi azalttı ve V-ATPaz’ın tam montajını engelledi, fosforilasyonu önlemek ise ters etki yarattı. Bir dizi enzim taramasıyla bu etiketi yerleştiren konak proteininin BMX adlı bir kinaz olduğunu belirlediler. BMX genetik olarak veya küçük moleküllü bir inhibitörle bloke edildiğinde, E1 fosforilasyonu düştü, pompa lizozomal zarlar üzerinde daha verimli monte oldu, lizozomlar daha asidik hale geldi ve makrofaj içindeki Mtb hayatta kalması azaldı.
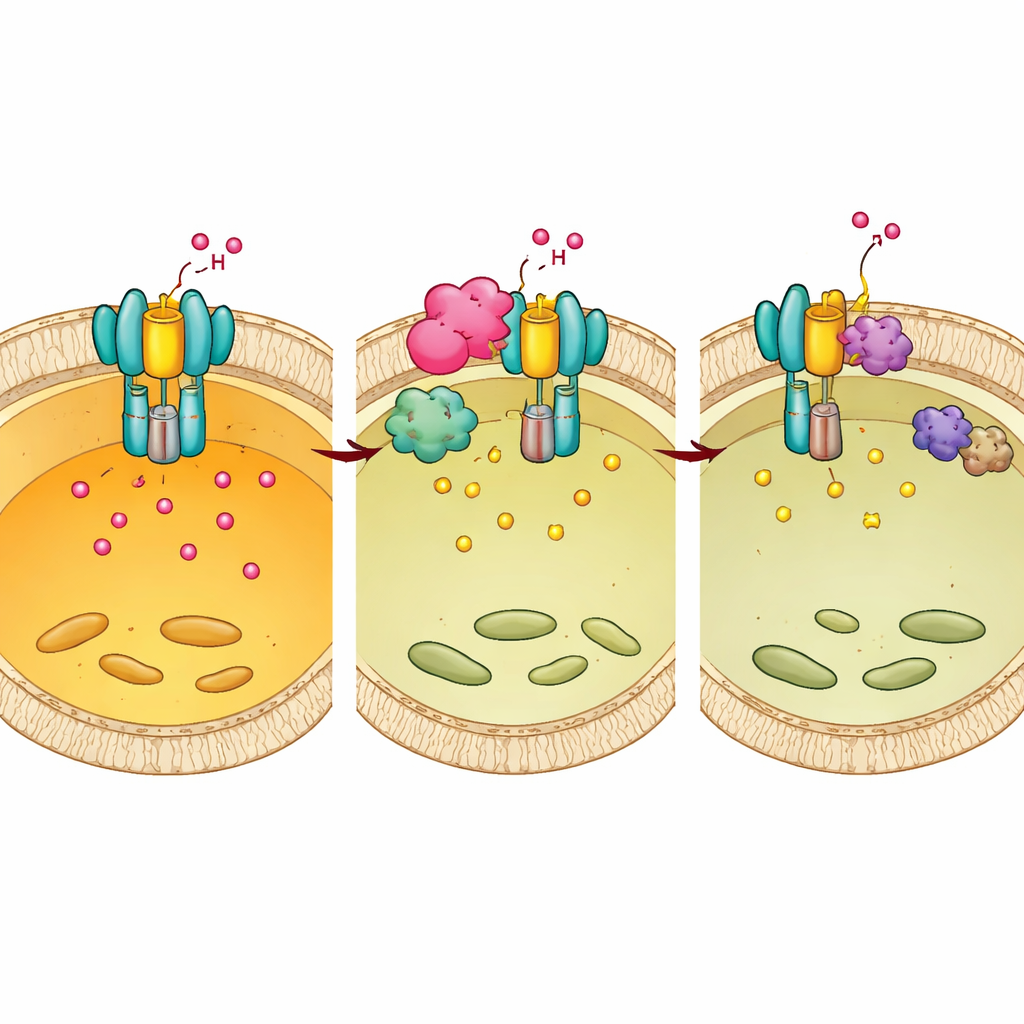
Mtb’nin konak anahtarını kendi lehine nasıl yeniden kabloladığı
Chp2 ile BMX’in birlikte çalıştıkları ortaya çıktı. Yapısal ve biyokimyasal deneyler, Chp2’nin E1 ile BMX’i lizozomal yüzeyde yakın temasa getiren bir iskele (scaffold) gibi davrandığını ve Tyr56/57’de E1 fosforilasyonunu artırdığını gösterdi. Bu ekstra etiketleme, pompanın tam montajını bozuyor, lizozomal pH’yı yükseltiyor ve Mtb’nin içinde kalabileceği daha ılımlı bir ortam yaratıyor. BMX engellendiğinde, hem kültürlenmiş hücrelerde hem de enfekte farelerde Chp2’nin sağladığı hayatta kalma avantajı ortadan kalktı. Önemli olarak, enfeksiyon sonrası farelere BMX inhibitörüyle tedavi uygulamak normal hayvanlarda bakteri yüklerini ve akciğer patolojisini azalttı; ancak zayıflamış E1’e sahip farelerde aynı etki görülmedi; bu da ilacın etkinliğinin E1 kaynaklı asitleşmeyi geri kazandırmakla ilişkili olduğunu gösteriyor.
Pathojen hilesini tedavi fikrine dönüştürmek
Günlük ifadeyle bu çalışma, verem bakterilerinin hücrelerimize, çöp öğütücüsündeki “asit pompasını” hafifçe kısmaya karışan bir yardımcı protein soktuğunu ve böylece mikropların yok edilmeyi atlatmasına izin verdiğini gösteriyor. Pompanın ana kontrol düğmesi olan alt birim (E1) ile onu çeviren konak enzimi (BMX) belirlenerek, ilaç müdahalesi için kesin bir nokta ortaya kondu. Farelerde BMX’in inhibe edilmesi, hücrenin iç asit banyosunu etkili biçimde yeniden etkinleştiriyor ve bakteri temizlenmesini iyileştiriyor. Bu bulgular, hücrelerimizi Mtb’ye karşı daha düşmanca hale getiren konak yönelimli tedavilerin kapısını aralıyor; bu tür yaklaşımlar antibiyotiklerle birlikte çalışarak ilaç direncine sahip veremle mücadeleye yardımcı olabilir.
Atıf: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Anahtar kelimeler: verem, lizozomlar, konak yönelimli tedavi, Mycobacterium tuberculosis, V-ATPaz