Clear Sky Science · tr
Preoptik kisspeptin-nNOS-GnRH (KiNG) nöronal ağı, farelerde aktivasyon‑inhibisyon yoluyla LH ritmikliğini düzenliyor
Bu beyin öyküsü kısırlık açısından neden önemli
Ovulasyon ve doğurganlık, ana hormonu darbeler ve aralıklı doruklar halinde salan çok küçük bir beyin hücresi grubuna bağlıdır. Bu zamanlama bozulduğunda üreme başarısız olabilir. Bu çalışma, fare beyninde bir etkinleştirici sinyal ile etkinliği sessizce kapatan ikinci bir sinyalin birlikte nasıl çalıştığını ve bu hormon ritimlerini nasıl biçimlendirdiğini ortaya koyuyor. Bu gizli zamanlama devresinin anlaşılması, belirli kısırlık biçimlerini açıklamaya ve üreme bozukluklarının tedavisine yönelik yeni yollar önermeye yardımcı olabilir.
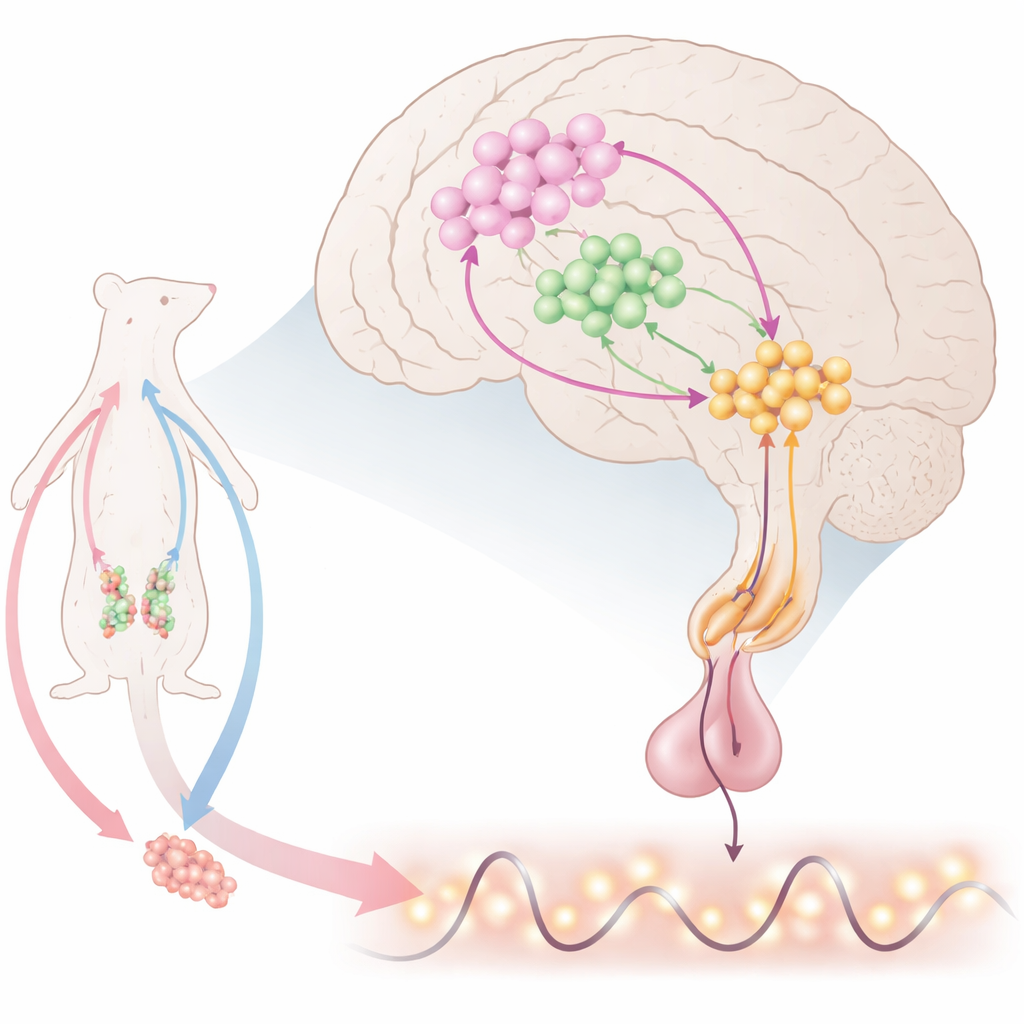
Üreme için beynin zamanlayıcısı
Beynin derinliklerinde, özel sinir hücreleri gonadotropin salgılatıcı hormon (GnRH) salgılar; bu hormon hipofizi uyararak luteinizan hormon (LH) ve folikül uyarıcı hormonun (FSH) salınmasını sağlar. Bunlar da yumurtalıklar ve testisleri kontrol eder. GnRH sürekli sızmaz; onun yerine düzenli darbeler ve dişilerde büyük bir preovülatuvar doruk şeklinde görülür. Bilim insanları birçok sinyalin GnRH hücrelerine ulaştığını bilir, ancak darbelerle birlikte dorukları da üreten tam bileşim belirsiz kaldı. Bu çalışma, GnRH hücrelerinin önde bulunduğu hipotalamusun küçük bir ön bölgesine odaklanıyor; burada GnRH hücreleri, GnRH’yi uyaran kisspeptin üreten nöronlar ve kısa mesafede difüze olabilen gaz halinde bir sinyal olan nitrik oksit (NO) yapan nöronlarla iç içe geçer.
İki sinyal arasında açma‑kapama ortaklığı
Araştırmacılar, kisspeptin, NO üreten (nNOS) nöronlar ve GnRH hücrelerinden oluşan üç parçalı bir “KiNG” ağı öneriyor. Kisspeptin, GnRH ve LH salımını tetikleyebilen güçlü bir uyarıcıdır, fakat sürekli uyarı sistemi aslında kapatır; bu durum dahili bir frenin gerekliliğini işaret eder. Yüksek duyarlıklı moleküler problar, genetik araçlar ve fare beyin dilimlerinde kayıtlar kullanarak ekip, kisspeptinin GnRH nöronlarını doğrudan uyarmaktan daha fazlasını yaptığını gösteriyor. Kisspeptin aynı zamanda preoptik alandaki, özellikle OV/MePO adlı bölgede bulunan yakınlardaki nNOS hücrelerini etkinleştirir. Kisspeptin düzeyleri yükseldiğinde bu nNOS hücreleri NO patlamaları üretir; bu da çevredeki hücrelerde, GnRH nöronları dahil, ikinci bir haberci olan cGMP üretimini tetikler. Bu NO–cGMP sinyali GnRH ateşlenmesini azaltır ve kisspeptin sürüşüne içsel bir kapama anahtarı sağlar.
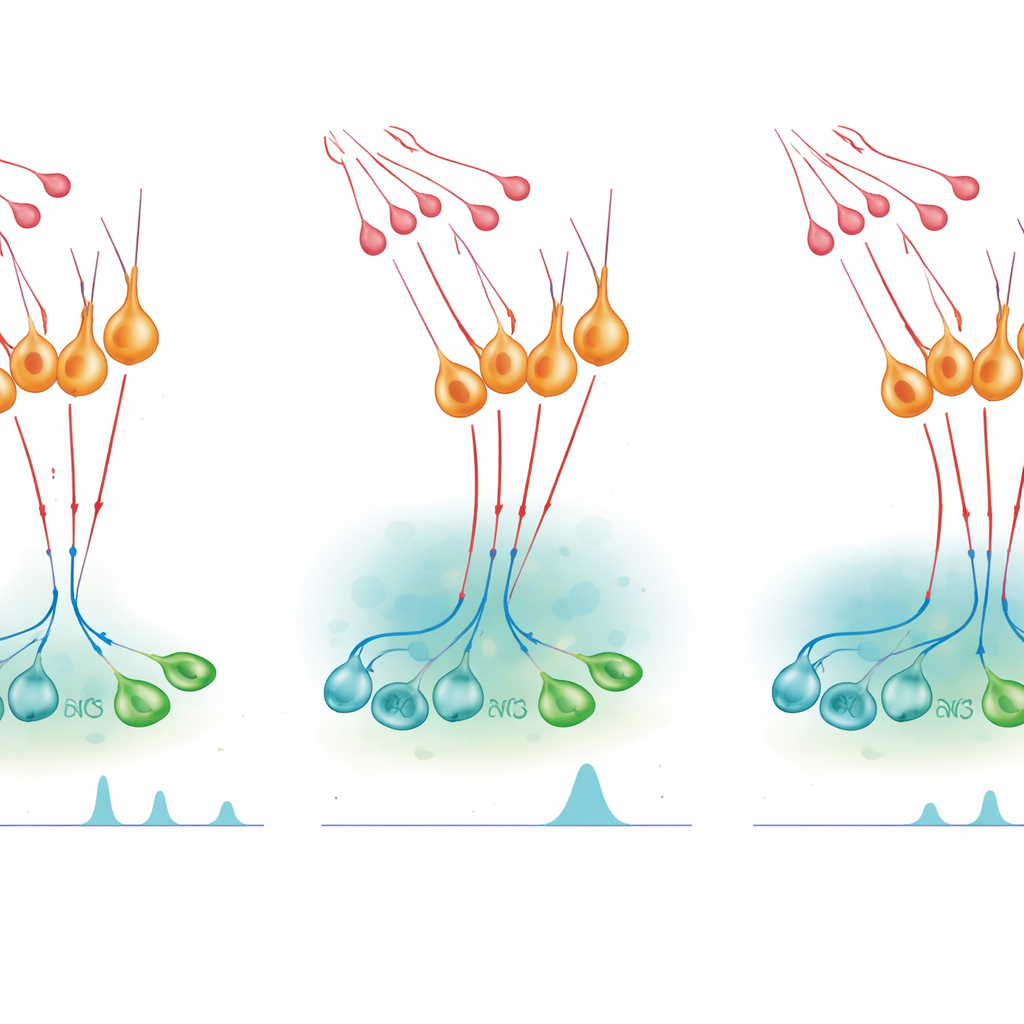
Hormon doruklarını açmak ve kısıtlamak
Bu mikrodevrenin hormon salımını nasıl etkilediğini test etmek için ekip, canlı farelerde nNOS nöronlarını açıp kapatmak üzere, aksi halde etkisiz bir ilaçla etkinleşen tasarlanmış reseptörler içeren kemogenetik anahtarlar kullandı. Dişi döngüsünün normal olarak sessiz bir evresinde nNOS hücrelerini yapay olarak aktive etmek, kan LH’sında doruk benzeri bir artış oluşturmak için yeterliydi; erkeklerde de aynı şey gözlendi. NO üretimini bloke etmek bu etkiyi ortadan kaldırdı ve bu nöronlardan kaynaklanan NO’nun doruk için gerekli olduğunu gösterdi. Ancak, bilim insanları nNOS hücrelerini inhibit ettiklerinde veya bunların kisspeptine duyarlılığını azalttıklarında, verilen bir kisspeptin dozu abartılmış ve uzamış bir LH artışı üretti. NO sentezini engelleyen farmakolojik ilaçlar benzer şekilde artırıcı etki gösterirken, cGMP sinyalini uzatan bir ilaç kisspeptin yanıtını kısalttı ve sonraki LH salımını azalttı. Bu deneyler birlikte NO’nun hem GnRH nöronlarını senkronize ederek dorukları oluşturmasına yardımcı olduğunu hem de kisspeptinin ne kadar uzun süre onları ateşte tutabileceğini sınırladığını gösteriyor.
Over döngüsü boyunca esnek bir ritim
Araştırma ayrıca bu açma‑kapama dengesinin dişi döngüsü boyunca değiştiğini gösteriyor. Hassas bir RNA tespit yöntemi kullanılarak, yazarlar ovulasyondan bir gün önce, östrojen düzeylerinin yüksek olduğu ve LH doruğunun gerçekleştiği dönemde daha fazla nNOS nöronunun kisspeptin reseptörünü ifade ettiğini buldu. Daha sessiz evrelerde daha az nNOS hücresi kisspeptine yanıt veriyor ve GnRH darbelerini durdurmaksızın nazikçe sınırlayan küçük, lokal NO miktarları üretiyor. Doruk gününde, daha güçlü kisspeptin girdisi ve artmış reseptör ifadesi NO üretimini büyük ölçüde artırır, NO daha uzaklara yayılabilir ve birçok GnRH hücresini aynı anda kısa süreliğine susturabilir. NO sinyali azaldıkça bu hücreler birlikte geri döner ve ovulasyon için gerekli büyük, koordineli LH doruğunu oluşturur.
İnsan sağlığı için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma GnRH hücrelerini başlatan aynı sinyalin—kisspeptinin—aynı zamanda gecikmeli bir fren sistemini NO aracılığıyla devreye soktuğunu gösteriyor; bu, hormonal patlamaların güçlü ama kontrolsüz olmamasını sağlar. KiNG ağı bu nedenle üreme zamanlaması için hem gaz hem de fren görevi görür; döngünün çoğunda GnRH darbelerini ayarlar ve ovulasyonu tetikleyen doruğu şekillendirir. Kisspeptin ve NO yollarında genetik değişiklikler üreme sorunları olan kişilerde bulunduğundan, bu hassas dengedeki devrenin anlaşılması kısırlığın ve ilgili durumların tanı ve tedavisine yönelik yeni yaklaşımlar için yol gösterici olabilir.
Atıf: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Anahtar kelimeler: üreme hormonları, hipotalamus, kisspeptin, azot oksit, ovulasyon zamanlaması