Clear Sky Science · tr
Histon laktileşmesi pankreas kanserinde nötrofil infiltrasyonu ve bağışıklıktan kaçış için CXCL1 ekpresyonunu artırır
Bu kanser çalışması neden önemli
Pankreas kanseri, kısmen diğer tümörlerde işe yarayan modern immünoterapilere sıklıkla direnç göstermesi nedeniyle en ölümcül kanserlerden biridir. Bu çalışma, pankreas tümörlerinin bağışıklık sistemini sessizce etkisiz hâle getirmek için kendi şeker metabolizmalarını nasıl yeniden düzenlediklerini ve bu süreci engellemenin vücudun savunmalarına — ve mevcut ilaçlara — savaşma yolunu nasıl yeniden açabileceğini ortaya koyuyor.
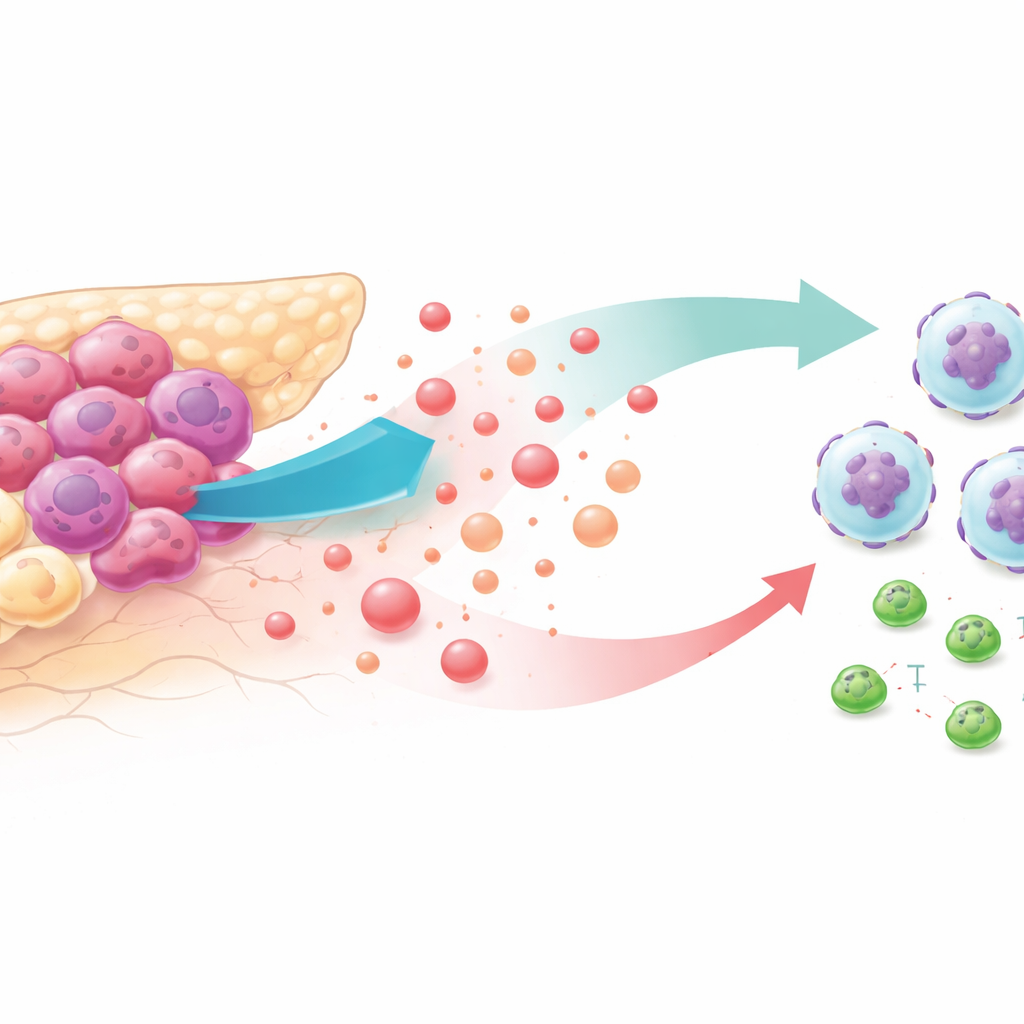
Şeker yiyen tümörler ve düşmanca bir çevre
Kanser hücreleri, oksijen bol olsa bile glukozu şiddetli bir hızla yakmalarıyla ünlüdür. Bu “yüksek glikoliz” yaşam tarzı tümör çevresini bir zamanlar metabolik atık olarak görülen laktatla doldurur. Hasta tümör veritabanları ve fare modellerini analiz ederek, araştırmacılar en yoğun glikolize sahip pankreas kanserlerinin nötrofillerle dolu olduğunu — bu bağlamda tümörlerin büyümesine yardımcı olan beyaz kan hücreleri — ve kanser öldürücü CD8 T hücrelerinin daha az olduğunu buldular. Bu profili gösteren hastaların yaşam sürelerinin daha kısa olma eğiliminde olması, değişmiş metabolizma ile bağışıklıktan kaçış arasında sıkı bir bağ olduğunu düşündürüyor.
Tümörler laktatı nasıl yanlış yardımı çağırmak için kullanıyor
Glikolizin nötrofilleri nasıl çektiğini anlamak için ekip, pankreas kanseri hücre hatlarında ve farelerde ilaçlar veya genetik yöntemlerle tümör glikolizini azalttı. Şeker yıkımı engellendiğinde, tümör hücreleri CXCL1 adlı kimyasal sinyali çok daha az saldı ve bu sinyalin dolaşımdaki düzeyleri farelerde ve hasta örneklerinde düştü. Laboratuvar göç testlerinde, nötrofiller yüksek glikolitik kanser hücrelerinden alınan ortama hevesle hareket etti, ancak glikoliz engellenmiş hücre ortamına doğru hareket etmedi — araştırmacılar saflaştırılmış CXCL1 ekleyene kadar. Canlı farelerde, glikoliz azaltılmış tümörlerde CXCL1’in yerine konması nötrofil sayısını yeniden yükseltti ve glikoliz inhibisyonunun tümöre karşı etkisini zayıflattı.
Laktat tarafından yönlendirilen yeni bir epigenetik anahtar
Çalışma daha sonra DNA paketlenme düzeyine odaklandı. Genlerimiz, gen etkinliğini açıp kapatan kimyasal etiketler işlevi gören makara benzeri proteinler olan histonların etrafına sarılır. Yazarlar, pankreas kanserinde glikoliz tarafından üretilen laktatın H3K18 olarak bilinen bir histon pozisyonuna özgü bir “laktil” etiketi eklediğini gösteriyor. Histon H3K18 laktileşmesi olarak adlandırılan bu modifikasyon, tümör dokularında normal pankreasa göre belirgin şekilde yüksekti. Glikoliz engellendiğinde, özellikle CXCL1 geninin kontrol bölgesine yakın yerlerde H3K18 laktileşmesi azaldı ve CXCL1 üretimi düştü. Laktatın yeniden eklenmesi hem histon etiketini hem de CXCL1 ekspresyonunu geri getirdi. Hasta örnekleri arasında daha fazla H3K18 laktileşmesine sahip tümörler ayrıca daha yüksek CXCL1 gösteriyordu; bu moleküler işaretin tümör yanlısı bir immün manzarayla bağlantısını destekliyor.
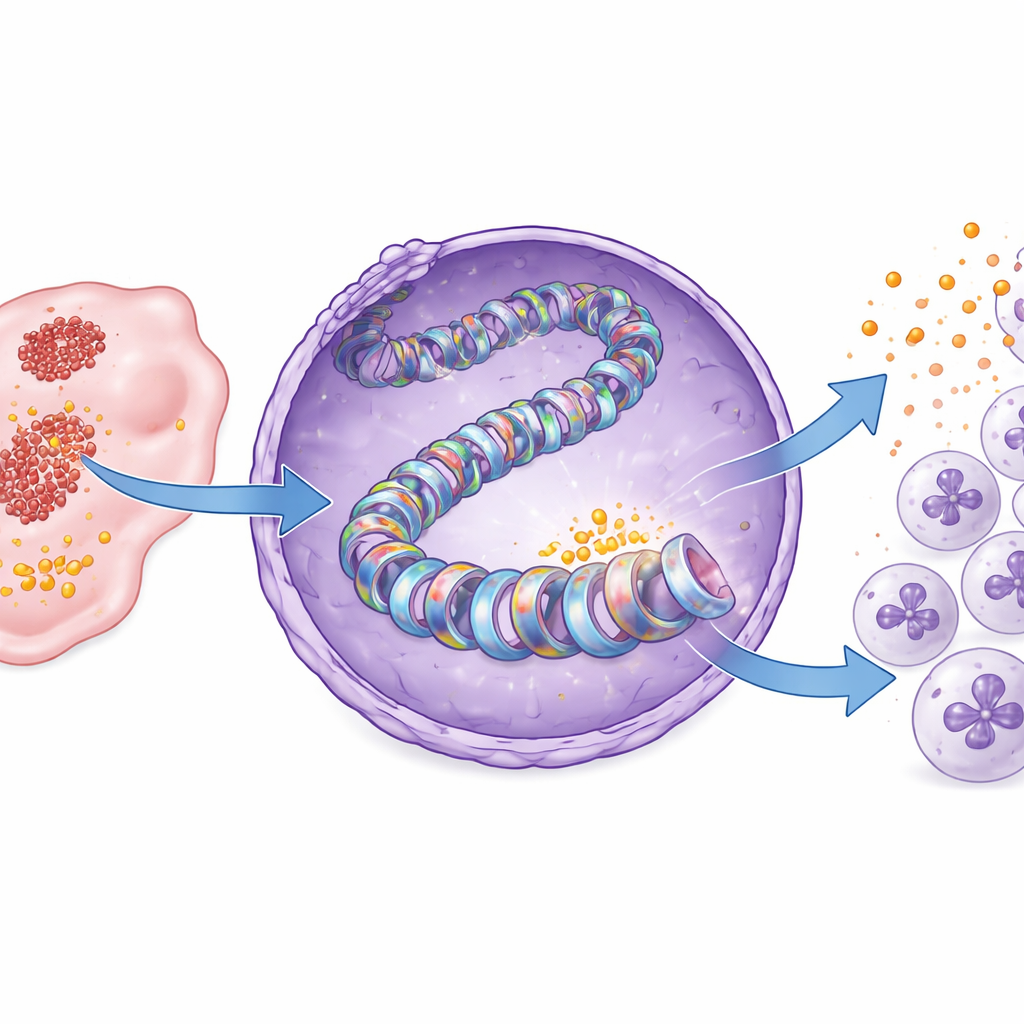
Enzimi tanımlamak ve ilaçla hedeflenebilir bir zayıf nokta
Histon etiketleri yazan özelleşmiş enzimler vardır. Bilinen histon modifiye edici proteinlerin inhibitörlerini tarayarak, araştırmacılar pankreas kanserinde H3K18 laktileşme işaretinin ana yazıcısı olarak PCAF adlı enzimi belirlediler. Yapısal modelleme, PCAF’ın etiketleme için kullanılan aktive laktat formu olan laktil-CoA ile bağlanabileceğini öne sürdü ve biyokimyasal testler saflaştırılmış PCAF’ın doğrudan histon H3’e laktil grupları ekleyebildiğini doğruladı. Bromosporin adlı küçük bir molekülle PCAF engellenmesi, kanser hücrelerinde ve fare tümörlerinde H3K18 laktileşmesini ve CXCL1 üretimini azalttı. Sonuç olarak, daha az nötrofil tümörlere girdi, daha fazla CD8 T hücresi birikti ve tümör büyümesi yavaşladı; bunların hepsi farelerde belirgin kilo kaybı veya toksisite olmadan gerçekleşti.
Kombinasyon terapisiyle soğuk bir tümörü ısıtmak
Anti–PD-1 antikorları gibi standart immün kontrol noktası ilaçları pankreas kanserinde sınırlı başarı gösterdiğinden, ekip laktat–PCAF–CXCL1 yolunu çökertmenin bu tümörleri daha duyarlı hâle getirip getirmeyeceğini test etti. Hem subkutan hem de pankreatik ortotopik fare modellerinde, bromosporin ile anti–PD-1 terapisi birlikte uygulandığında tek başına her bir tedaviden daha fazla tümör küçülmesi sağlandı, nötrofil infiltrasyonu azaldı, etkin CD8 T hücreleri arttı ve sağkalım anlamlı şekilde uzadı. Bu, tümörün nötrofiller için çalan metabolik “sirenini” kesmenin immünolojik olarak “soğuk” bir tümörü, kontrol noktası terapisinin daha iyi hedefleyebileceği daha “sıcak” bir hale getirmeye yardımcı olduğunu gösteriyor.
Gelecekteki tedavi için ne anlama geliyor
Basitçe ifade etmek gerekirse, çalışma bir zincirleme reaksiyonu açığa çıkarıyor: pankreas tümörleri şekeri yakar, laktat salar, bu laktatı DNA paketleme proteinlerinde bir epigenetik anahtarı çevirme amacıyla kullanır, CXCL1’i artırır ve böylece katil T hücrelerinden saklanmalarına yardımcı olan nötrofilleri çağırır. Bu zinciri PCAF adımında bir ilaçla kesmek yalnızca tümörleri yavaşlatmakla kalmaz, farelerde mevcut immünoterapinin etkisini de artırır. Güvenliği sağlamak ve bu yolu insanlarda hedeflemenin en iyi yolunu bulmak için daha fazla çalışma gerekse de, bu bulgular umut verici bir stratejiyi vurguluyor: tümörün metabolizmasını ve genetik anahtarlarını yeniden programlayarak bağışıklık sistemine adil bir savaş şansı vermek.
Atıf: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Anahtar kelimeler: pankreas kanseri, tümör metabolizması, histon laktileşmesi, tümör mikroçevresi, kanser immünoterapisi