Clear Sky Science · tr
Akut Nekrotizan Ensefalopatinin genetik sürücüsü RANBP2, İnfluenza A virüs enfeksiyonuna karşı iltihabi yanıtı düzenliyor
Grip Beyne Zarar Verdiğinde
Çoğu insan gribi bir haftalık ateş, öksürük ve yatak istirahati olarak düşünür. Yine de nadir durumlarda, özellikle çocuklarda, sıradan bir grip enfeksiyonu aniden akut nekrotizan ensefalopati (ANE) adı verilen hayati tehlike arz eden bir beyin bozukluğuna dönüşebilir. Aileler ve doktorlar uzun zamandır hangi kişilerin bu yıkıcı komplikasyonu geliştireceğini genlerin etkileyebileceğini düşünüyorlardı. Bu çalışma, tek bir hücresel kapı bekçisi proteini olan RANBP2'nin normalde gribin kontrol altında tutulmasını nasıl sağladığını ve vücudun kendi iltihabi yanıtının kontrolden çıkmasını nasıl önlediğini ortaya koyuyor.
Nadir ama Yıkıcı Bir Grip Komplikasyonu
ANE genellikle ateşli bir hastalığı takiben aniden ortaya çıkar, çoğunlukla influenza ile ilişkilidir ve hızla nöbetlere, komaya ve kalıcı nörolojik hasara yol açabilir. Dünyada bilinen ANE vakalarının yaklaşık yarısı, özellikle H1N1 suşu olmak üzere influenza A virüsü ile bağlantılıdır. RANBP2 geninde belirli değişiklikleri miras alan çocuklar, ANE1 olarak bilinen durumda çok daha yüksek bir riskle karşılaşır. Ancak şimdiye kadar bilim insanları bu proteinin grip enfeksiyonu sırasında gerçekte ne yaptığını veya neden bu değişikliğin beyindeki iltihabı bu kadar şiddetli hale getirdiğini anlamamıştı.
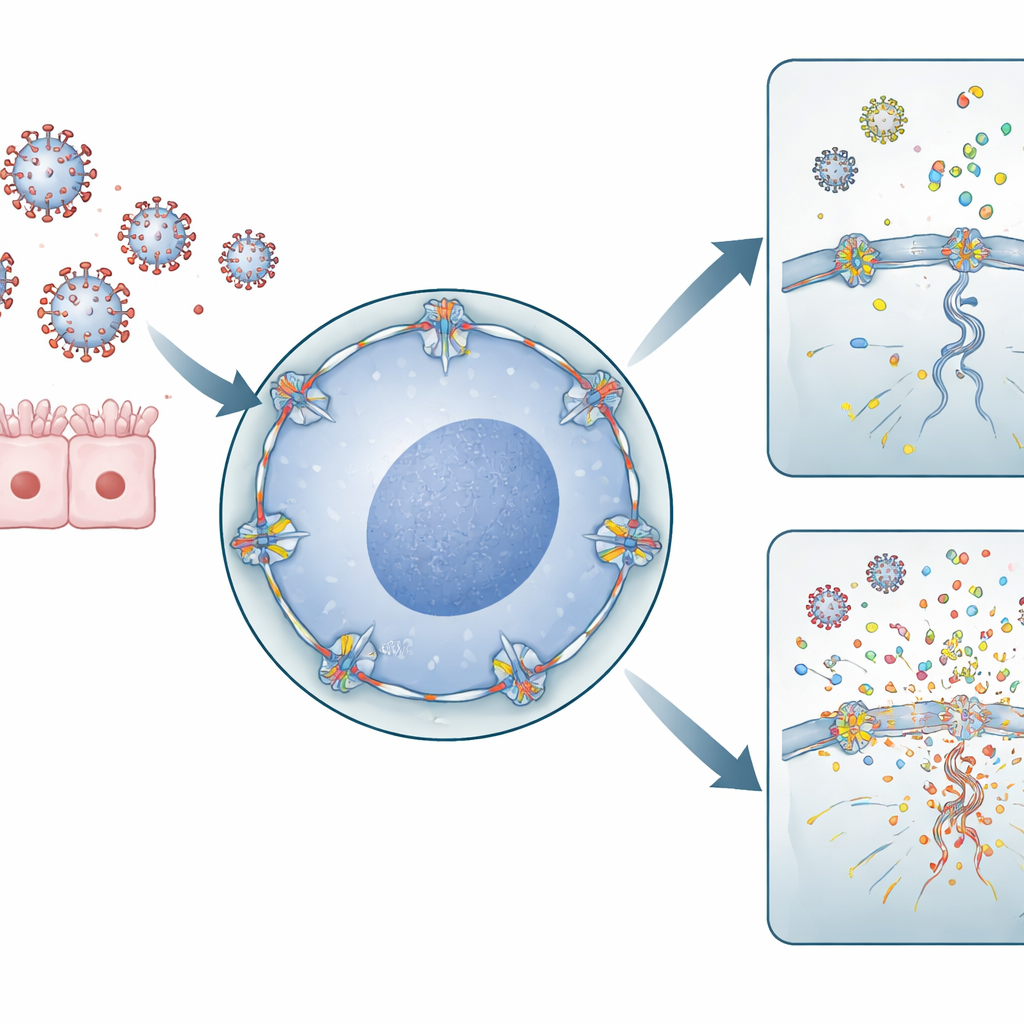
Hücresel Kapılar ve Viral Genomlar
İnfluenza A virüsü, bir RNA virüsü için sıra dışı bir yaşam tarzına sahiptir: genetik materyalini kopyalamak için hücrenin çekirdeğine girmesi gerekir. Bunu yapmak için çekirdek zarı üzerindeki çekirdek gözeneklerinden geçer—çekirdek ile çevreleyen sitoplazma arasındaki trafiği kontrol eden büyük kapılar. RANBP2 bu gözeneklerin dış tarafında bulunan önemli bir bileşendir. Yazarlar, insan akciğer kaynaklı hücreler ve immün hücreler kullanarak RANBP2 düzeylerini düşürdü veya ANE ile ilişkili mutasyonu tanıttı. RANBP2 eksik veya yanlış yerleşmiş olduğunda, grip genomlarının çekirdek içinde daha fazla kopyalandığını ve viral gen parçalarının dengesiz bir şekilde sitoplazmaya aktarılmasını buldular. İlginç bir şekilde, bu fazla viral RNA daha fazla enfektif virüs partikülü üretmedi, fakat viral materyalin hücre içinde nerede ve nasıl biriktiğini değiştirdi.
Viral Döküntü Alarm Sistemini Beslediğinde
İmmün sistem, sitoplazmadaki yabancı viral RNA parçalarını tehlike sinyalleri olarak algılayan moleküler sensörlere dayanır. Araştırma ekibi, normal RANBP2 olmayan hücrelerde fazladan viral RNA parçalarının sitoplazmada biriktiğini ve bu sensörlerin tanımaya ayarlı olduğu tam tür örüntüleri oluşturduğunu gösterdi. Akciğer kaynaklı hücrelerde bu, IL‑6 ve IL‑1β gibi daha yüksek düzeyde iltihabi molekülleri tetikledi. Kan bağışçılarından alınan birinci dereceden insan makrofajlarında—ön hat immün hücreleri—RANBP2 kaybı CXCL8, CXCL10, CCL2, CCL3 ve CCL4 dahil olmak üzere belirgin bir pro‑iltihabi kemokin artışına yol açtı. Bu kimyasal haberciler ek immün hücreleri toplar ve aktive eder, enfeksiyona karşı genel tepkiyi güçlendirir.
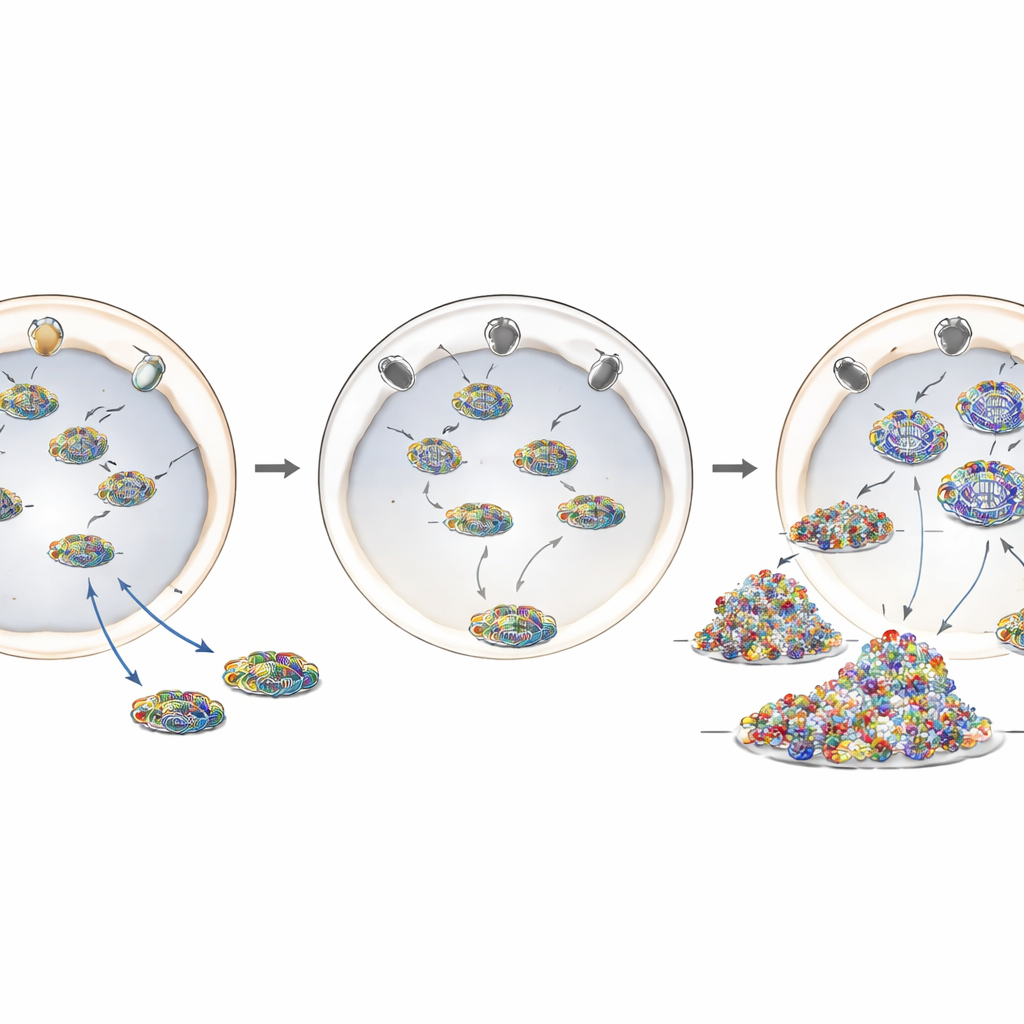
Bir Koruyucuyu Yanlış Yere Gönderen Hastalık Mutasyonu
ANE1’i daha yakından modellemek için araştırmacılar CRISPR‑Cas9 genom düzenlemesi kullanarak insan RANBP2 genine en yaygın hastalık ilişkili değişiklik olan T585M’i eklediler. Bu düzenlenmiş hücrelerde RANBP2 protein düzeyleri büyük ölçüde normaldi, ancak konumu değildi: çekirdek zarı etrafında parlak bir halka oluşturmak yerine, proteinin büyük kısmı hücre iç kısmına yer değiştirmişti. Bu mutasyonu taşıyan hücreler, gen kopyasından bağımsız olarak, RANBP2 azaltılmış hücreler gibi davrandı. Artmış influenza genom replikasyonunu desteklediler, sitoplazmada daha fazla viral materyal gösterdiler ve enfeksiyon sonrası daha güçlü bir iltihabi yanıt sergilediler. Bu, RANBP2’nin koruyucu rolü için toplam miktarından ziyade nükleer gözeneklerde doğru şekilde konumlanmasının hayati olduğunu düşündürüyor.
Risk Altındaki Çocuklar İçin Neden Önemli
Bulgular bir arada değerlendirildiğinde, RANBP2’yi influenza genetik materyalinin çekirdeğe girişini ve çekirdekten çıkışını ince ayarla düzenleyen hücresel bir koruyucu olarak tanımlıyor. RANBP2 yok veya yanlış yerleşmiş olduğunda, viral RNA aşırı şekilde kopyalanır ve düzensiz biçimde dışa aktarılır, sitoplazmayı moleküler artıklarla doldurarak immün sinyallemeyi büyük ölçüde yoğunlaştırır. Çoğu doku için bu, daha şiddetli ancak atlatılabilir bir grip nöbeti anlamına gelebilir. Ancak ANE1’li savunmasız çocuklarda, böyle kontrolsüz iltihap—özellikle beyne ulaşırsa—normal enfeksiyonları takiben görülen ani, ciddi nörolojik hasarı açıklamaya yardımcı olabilir. Bu yolun anlaşılması, risk altındaki hastaları erken tespit etmeye ve bağışıklık yanıtı koruyucu olmaktan yıkıcıya dönmeden önce anti‑iltihabi tedavileri uyarlamaya yönelik gelecekteki stratejilere rehberlik edebilir.
Atıf: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Anahtar kelimeler: influenza, akut nekrotizan ensefalopati, RANBP2, hiperinflamasyon, nükleer gözenek