Clear Sky Science · tr
KIAA1199 yüksek kolorektal kanser hücreleri tarafından fonksiyonel olarak yeniden programlanan hepatositler, pro‑metastatik Egr1+ nötrofillerin birikimini destekliyor
Kolon Kanseri Karaciğeri Hedeflediğinde
Çoğu insan kanserin yayılmasını, kötü huylu hücrelerin basitçe ayrılıp yeni organlara sürüklenmesi olarak düşünür. Bu çalışma daha rahatsız edici bir senaryoyu gösteriyor: kolorektal (kolon) tümörleri, herhangi bir kanser hücresi ulaşmadan çok önce karaciğeri sessizce yeniden düzenleyerek gelecekteki tümörlerin kolayca kök salabileceği “toprak” hazırlıyor. Bu gizli hazırlık evresini anlamak, kolorektal kanserde ölümün ana nedeni olan karaciğer metastazlarını başlamadan durduracak tedavilere kapı açabilir.
Tümörler Gelmeden Önceki Sinsi Kurulum
Kolorektal kanser sıkça karaciğere yayılır, ama yalnızca bazı tümörler bunu agresif biçimde yapar. Yazarlar yüksek riskli kolorektal kanserlerde bol bulunan KIAA1199 adlı moleküle odaklandı. Fare modellerinde ve hasta örneklerinde, KIAA1199 yüksek tümörler sadece daha hızlı büyümekle kalmadı; aynı zamanda karaciğeri “pre‑metastatik niş”e, gelen kanser hücrelerine olağanüstü derecede dost bir mikroçevreye dönüştürdü. Karaciğer tümörleri deneysel olarak ayrı bir kaynaktan aşılandığında bile, KIAA1199‑yüksek kolon tümörlerine sahip hayvanlar çok daha fazla karaciğer metastazı geliştirdi ve daha çabuk öldü. Bu durum, yalnızca dolaşan kanser hücrelerinin değil, primer tümörün sinyallerinin de karaciğeri önceden yeniden şekillendirdiğini gösterdi.
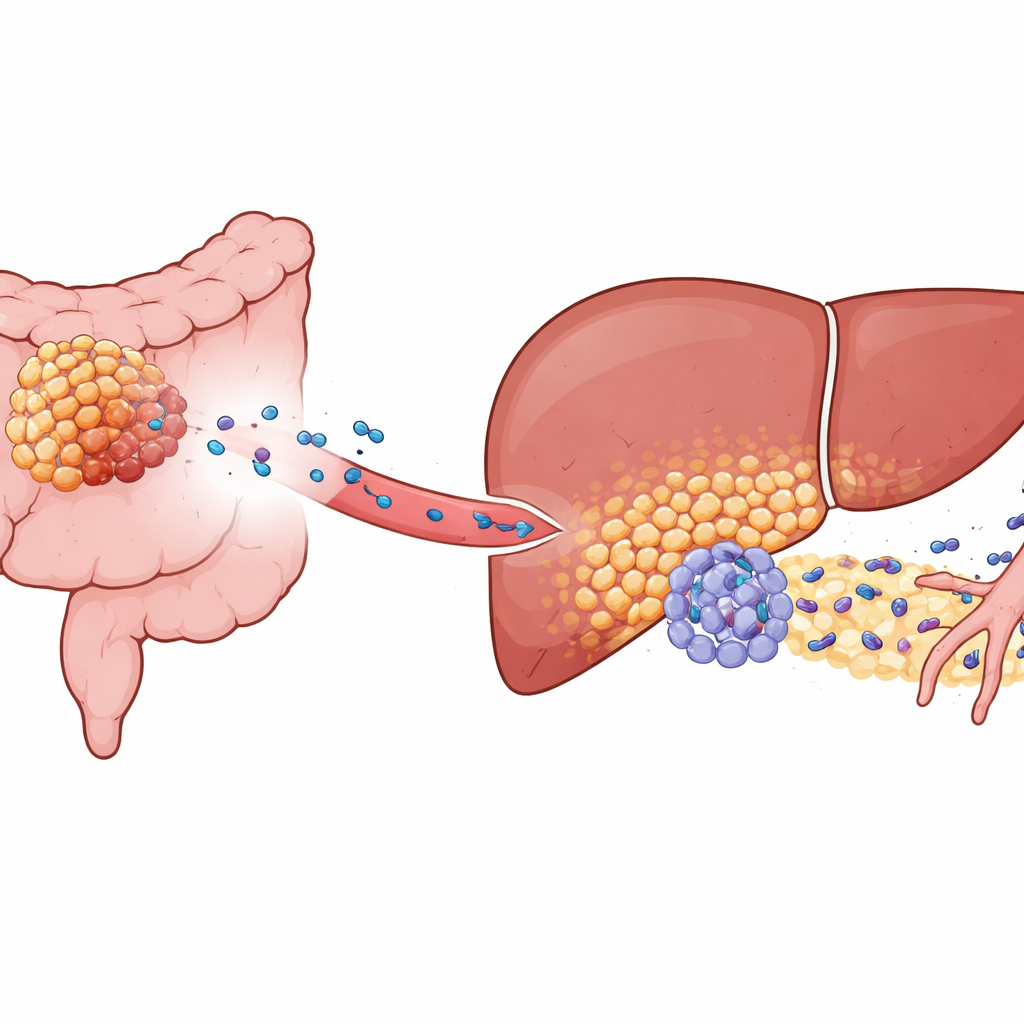
Tümör Yardımcılarına Dönüştürülen Karaciğer Hücreleri
Daha derine inen araştırmacılar, karaciğer dokusunu yüksek çözünürlükte incelemek için tek hücre dizilemesi ve mekânsal haritalamayı kullandılar. Normalde karaciğerin işçi hücreleri olan hepatositlerin belirgin bir alt kümesinin “fonksiyonel olarak yeniden programlandığını” keşfettiler. Bu hücreler yalnızca KIAA1199‑yüksek tümörler var olduğunda ortaya çıktılar. Metabolizmayı sessizce yönetmek yerine, değişmiş hepatositler daha malign‑benzeri bir metabolik profile geçti ve genellikle inflamasyon ve stres yanıtlarını kontrol altında tutan koruyucu düzenleyici PPARγ'yi baskıladı. PPARγ baskılandığında bu hepatositler SAA2 adlı bir proteini yüksek düzeyde üretmeye başladı ve özellikle karaciğer dokusunun invaze eden tümör hücreleriyle buluştuğu sınırda çevrelerine saldılar.
Sıradan Savunmacıları Pro‑Metastatik Nötrofillere Dönüştürmek
Enfeksiyonlarla savaşmalarıyla bilinen beyaz kan hücreleri nötrofiller de bu hazırlıklı karaciğerde garip davrandı. Yazarlar, işlevlerini yeniden şekillendiren bir transkripsiyon faktörünün adını taşıyan “Egr1+” imzasına sahip özel bir alt küme buldu. Nötrofillerin kan dolaşımından zaten değişmiş olarak gelmek yerine, yeniden programlanmış hepatositler tarafından yerel olarak yeniden eğitilmiş gibi göründükleri anlaşıldı. Hepatositlerden salınan SAA2, yakınlardaki nötrofillerdeki FPR2 adlı reseptöre bağlanarak içsel PI3K‑AKT sinyal yolunu açtı ve Egr1 aktivitesini stabilize etti. Sonuç, uzun ömürlü, yüksek derecede aktif bir nötrofil oldu; bu hücreler bol miktarda yeni damar oluşumunu tetikleyen güçlü bir faktör olan VEGFA salgıladı. Bu Egr1+ nötrofiller, tam da yeni ve hassas damarların filizlendiği tümör–karaciğer arayüzünde kümelendi.
Tümör Hücrelerini Kabul Eden Kan Damarları İnşa Etmek
Çalışma, bu yeniden eğitilmiş nötrofillerin sadece seyirci olmadığını—karaciğerin damar yapısını aktif biçimde yeniden düzenlediklerini—gösteriyor. Hücre kültüründe, Egr1+ nötrofillerin salgıladığı faktörler endotel hücrelerini büyümeye, göç etmeye ve yeni damarları andıran tüp‑benzeri yapılar oluşturmaya yöneltti. Farelerde Egr1+ nötrofillerin eklenmesi karaciğer metastazlarını artırdı ve ölümleri hızlandırdı. Zincirdeki kilit adımları—nötrofillere yönelik SAA2–FPR2 sinyalini veya aşağı akıştaki PI3K‑AKT yolunu—engellemek, nötrofil hayatta kalmasını ve VEGFA üretimini kesti, damar oluşumunu ve metastatik yayılımı azalttı. Benzer şekilde, hepatositlerde PPARγ aktivitesini diyabet ilacı rosiglitazon ile geri kazandırmak SAA2 seviyelerini düşürdü, Egr1+ nötrofillerin ortaya çıkışını engelledi ve preklinik modellerde karaciğer metastazını belirgin şekilde azalttı.
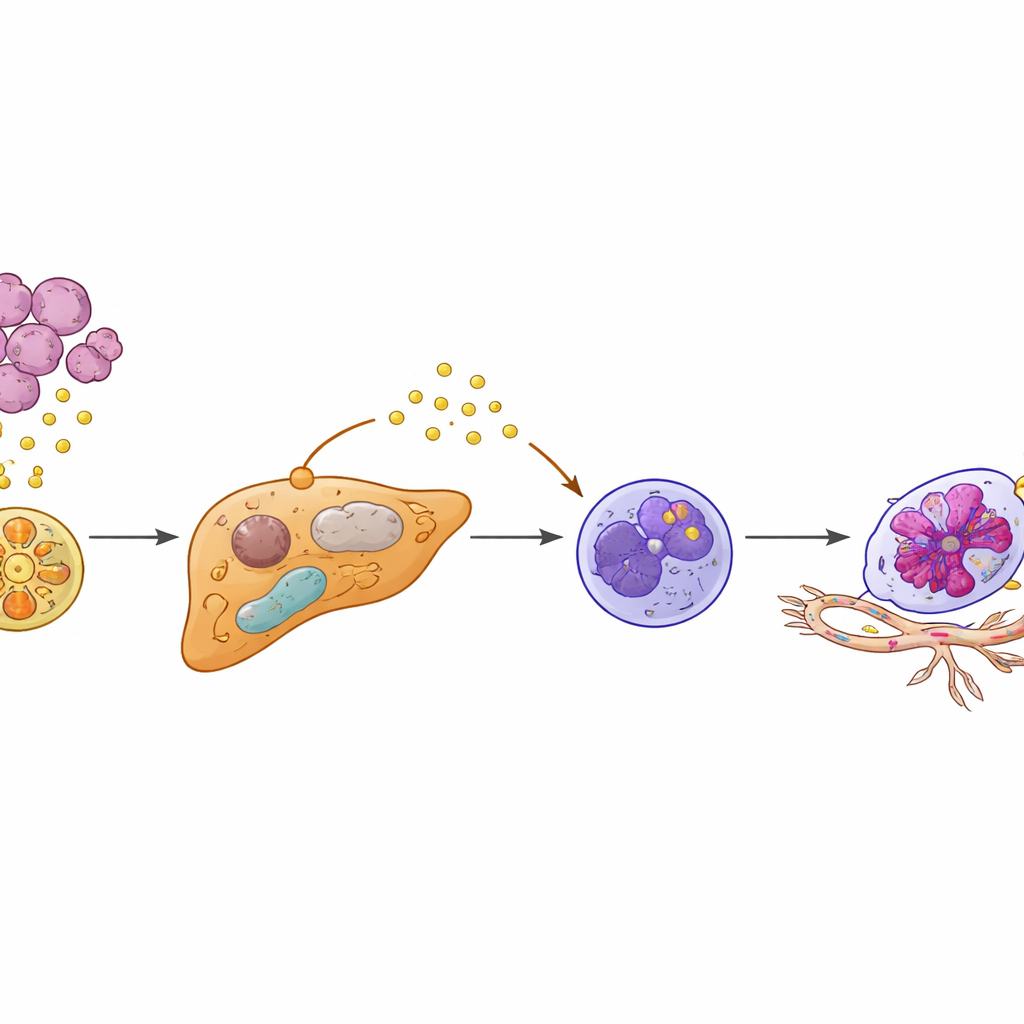
Mekanizmadan Tahmine ve Önlemeye
KIAA1199 tümörlerde ve SAA2 karaciğerde bu kaskadın en üstlerine yakın yer aldığından, yazarlar bu proteinlerin hastaları yüksek karaciğer metastazı riski açısından işaretleyip işaretleyemeyeceğini test ettiler. Birkaç hasta kohortunda, her iki belirteci de yüksek kan düzeylerinde taşıyan kişiler çok daha yüksek oranda ve daha erken tarihlerde karaciğer metastazı geliştirdiler. Basit bir birleşik KIAA1199–SAA2 skoru, riski tahminlemede tek başına herhangi bir belirteçten daha iyi performans gösterdi ve bir hastanın önümüzdeki iki yıl içinde karaciğere yayılma olasılığını tahmin eden klinik bir “nomogram” içine paketlendi. Bulgular bir tablo çiziyor: KIAA1199‑yüksek kolon kanserleri, hepatositleri yeniden kablolayan vezikül‑taşınan sinyaller gönderiyor; hepatositler de yakınlardaki nötrofilleri uzun ömürlü, damar‑inşa eden ortaklara çeviriyor. Bu KIAA1199–PPARγ/SAA2–Egr1 eksenine—metabolik ilaçlar, immünomodülatör ajanlar veya her ikisi aracılığıyla—hedeflenmesi, yalnızca mevcut karaciğer metastazlarını tedavi etmekle kalmayıp, onların yerleşmesini önleme potansiyeline işaret ediyor.
Atıf: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Anahtar kelimeler: kolorektal kanser karaciğer metastazı, pre‑metastatik niş, nötrofiller, hepatositlerin yeniden programlanması, tümör mikroçevresi