Clear Sky Science · tr
Medyal gangliyonik eminans ve hipotalamusta histon 3.3 lizin 4 metilasyonunun azaltılması nörogelişimsel bozukluk fenotiplerini yeniden oluşturur
Minik Kimyasal Etiketler Beyin ve Vücudu Nasıl Şekillendirir
Bazı genetik değişiklikler neden hem öğrenme güçlüklerine hem de çocuklukta çok küçük olup erişkinlikte obezite gibi sıra dışı büyümeye yol açar? Bu çalışma, beyindeki DNA paketleyici proteinlerdeki küçük kimyasal etiketlere bakıyor ve bunları yalnızca iki kilit bölgede bozmanın farelerde nöbetler, anksiyete benzeri davranışlar, bellek sorunları ve vücut boyutunda çarpıcı değişiklikler gibi etkileri nasıl tetiklediğini gösteriyor.
Genomun Karartma Düğmelerindeki Anahtarlar
Her beyin hücresinin içinde DNA, histon adı verilen makaraya benzeyen proteinlerin etrafına sarılmıştır. Bu histonlara eklenen kimyasal işaretler, gen gruplarını açıp kapatan karartma düğmeleri gibi davranır. H3K4 olarak adlandırılan bir bölgeye eklenen bu işaretlerden biri, genlerin açılmasıyla güçlü biçimde ilişkilidir. İnsan genetik çalışmaları, bu işareti ekleyen veya çıkaran enzimlerde doğuştan kusur taşıyan kişilerin sıklıkla entelektüel gerilik, epilepsi ve anormal vücut büyümesi içeren nörogelişimsel bozukluklara sahip olduğunu göstermiştir. Ancak hangi beyin hücrelerinin bu bozulmaya en duyarlı olduğu ve bunların işlev bozukluğunun beyin uyarılganlığı ile bütün vücut metabolizması arasındaki bağı nasıl kurduğu belirsiz kaldı.
İki Kritik Beyin Merkezini Hedeflemek
Araştırmacılar, histon proteininden mutant bir versiyonun (H3.3K4M) yalnızca iki embriyonik beyin bölgesinden köken alan hücrelerde açıldığı fareler geliştirdiler: birçok inhibitör “fren” hücresini üreten medial gangliyonik eminans ve iştah, hormonlar ve enerji dengesi üzerinde rol oynayan gelişen hipotalamus. Bu mutasyon, histonların kendisini ortadan kaldırmadan H3K4 metilasyonunu spesifik olarak engelliyor. Testler, mutant proteinin hedeflenen alanlarda yaygın olduğunu ve normal H3K4 işaretlerinin buralarda güçlü biçimde azaldığını, toplam histon düzeylerinin ise sabit kaldığını doğruladı. Bu tasarım, H3K4 ile ilişkili bir genin yalnızca bir kopyasının kusurlu olduğu, tamamen eksik olmadığı pek çok insan durumunu taklit ediyor.
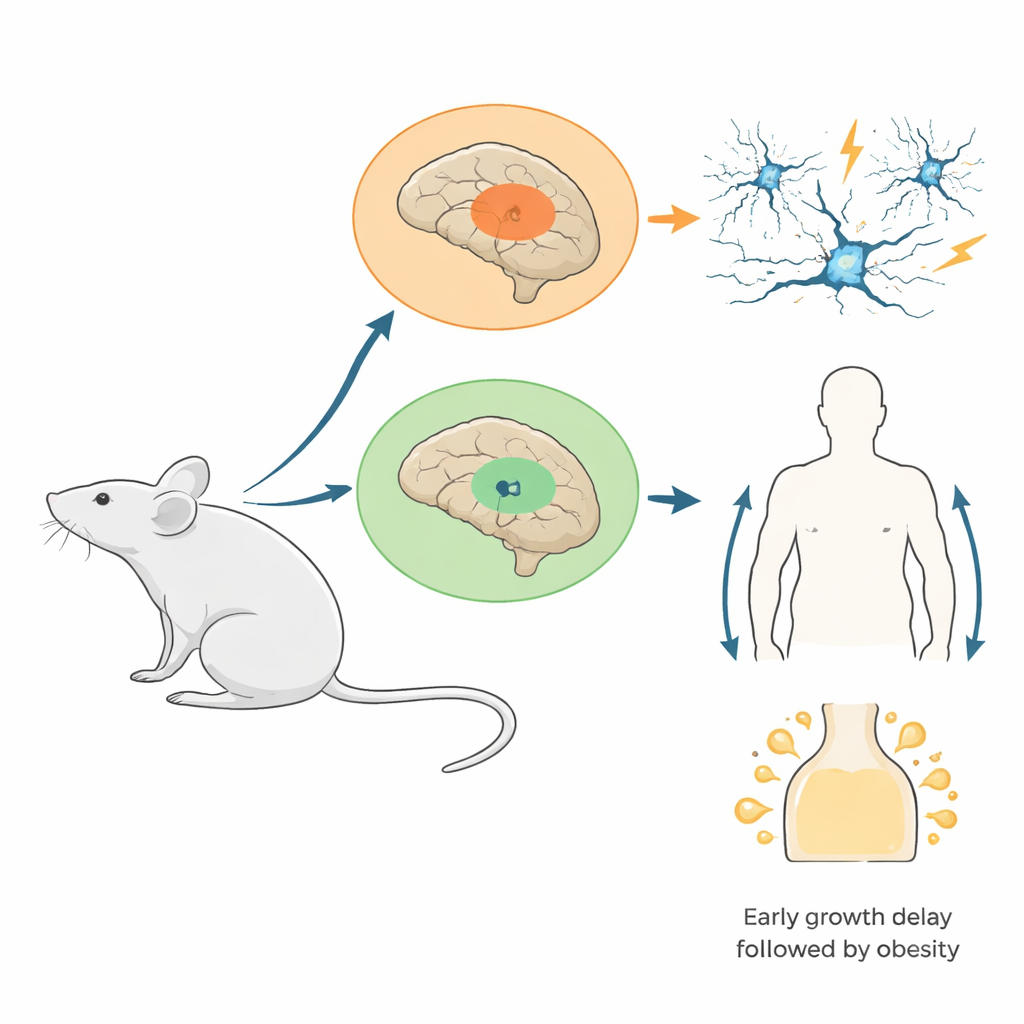
Eksik Fren Hücrelerinden Nöbet Eğilimli Devrelere
Bu fareler büyüdükçe, beyin devreleri üzerindeki sonuçlar belirginleşti. Genç mutantlarda korteks ve hipokampusta özellikle sinirsel ritimleri sıkı tutan hızlı ateşleyen bir türde olmak üzere daha az inhibitör internöron vardı. Ayrıntılı kayıtlar, kalan internöronların mevcut olduğunu ama elektriksel özelliklerinde daha fazla değişkenlik gösterdiğini, bunun da olgunlaşmalarının bozulduğunu düşündürdü. Beyin dilimlerinde hipokampus uyarıldığında, bilgi işlemeyle ilişkilendirilen yüksek frekanslı “gamma” osilasyonları daha zayıf ve daha yavaş oldu ve anormal patlama benzeri olaylar ortaya çıktı. Canlı hayvanlarda birçok mutant, özellikle dişiler, spontan nöbetler geliştirdi ve ilaçla indüklenen nöbetlere çok daha hassastı. Gelişimin erken döneminde ekip, hücre kaybını çoğunlukla internöronların kortekse göçündeki yetersizliğe bağladı; bu, artmış hücre ölümü veya azalmış hücre bölünmesine bağlı değildi.
Nöbetle İlişkili Hücrelerde Gen Aktivitesinin Yeniden Kablosu
Bu fiziksel değişiklikleri gen kontrolüne bağlamak için ekip, tek-nükleus dizileme kullanarak bireysel hücrelerden hem gen aktivitesini hem de DNA erişilebilirliğini okudu. Embriyonik medial gangliyonik eminansda mutantlarda değişen genlerin çoğu aşağıya doğru düzenlenmişti ve bunların arasında hücreleri belirli inhibitör kaderlere yönlendiren kilit düzenleyiciler vardı. Yetişkin internöronlarda alt tipler arasındaki denge kaydı ve bağlantı kurmaya ve ateşleme hızını belirlemeye yardımcı olan potasyum akımlarını kontrol eden gen grupları düzensiz regüle edildi. Ağ analizi, epilepsi ve beyin ritimlerini etkilediği bilinen potasyum kanal genlerinin koordineli bozulmasını vurguladı; bu, bir histon işaretinin kaybı, internöron kimliğinin değişmesi ve nöbet duyarlılığı arasında doğrudan moleküler bir bağ sağlıyor.
Hipotalamik Dengesizlik ve İki Aşamalı Büyüme Eğrisi
Hipotalamus, vücut büyümesi merkezli tamamlayıcı bir hikâye anlattı. Yavrularda mutant fareler daha küçük doğdu ve önemli bir kısmı erken dönemde öldü. Hayatta kalanlar ise daha sonra daha çok yemek yiyip yağ depoladı ve leptin hormonunun yüksek düzeylerini geliştirdi; bu durum obeziteyi ve muhtemel leptin direncini işaret ediyor. Embriyonik hipotalamusun tek hücre analizinde, daha fazla bölünen progenitör hücre bulundu ama özellikle beslenmeyi algılayan ve büyüme hormonunu düzenleyen ana çekirdekler için kader tayin edilmiş hücre sayısı azaldı. Yetişkin hipotalamusta hücresel karışım yeniden şekillendi: astrositler keskin şekilde artarken oligodendrositler azaldı ve tanyositler olarak adlandırılan özel bariyer hücreleri ile komşu glia, dolaşımdaki hormonlar ve besinlerle beyin arayüzündeki düzenli dizilimlerini kaybetti. Bu yapısal ve gen ifadesi değişiklikleri muhtemelen beynin enerji depolarını algılama ve iştahı kontrol etme biçimini bozuyor.
İnsan Nörogelişimsel Bozukluklarının Davranışsal Yankıları
Farelerin davranışı birçok nörogelişimsel durumda görülen semptomları yansıttı. Artmış anksiyete benzeri davranış, değişmiş yürüyüş, ev ortamında azalmış spontan hareket ve hafıza, nesne tanıma ve ani sesleri süzme görevlerinde zayıf performans sergilediler. Bazı testler artmış dürtüsellik benzeri eylemler gösterdi. Çoklu ölçümlerde dişiler genellikle erkeklerden daha şiddetli etkilenmiş göründü; bu durum, cinsiyete özgü hormon sistemleri ve gen düzenlemesinin histon işaretleriyle etkileşerek duyarlılığı şekillendirebileceğine işaret ediyor.
İnsan Sağlığı İçin Ne Anlama Gelir
Bulgular bir arada, yalnızca iki embriyonik beyin merkezinde bir histon işareti setinin zayıflatılmasının, daha az inhibitör “fren”, kararsız beyin ağları, nöbetler, bozulmuş beslenme devreleri ve anormal vücut büyümesi gibi geniş bir sorun kümesini yeniden üretmek için yeterli olduğunu gösteriyor. Uzman olmayanlar için ana mesaj şudur: H3K4 metilasyonu gibi epigenetik işaretler belirsiz ekler değil, gelişmekte olan beyin hücrelerinin doğru zamanda, doğru yerde doğru tipte olmalarına yardımcı olan hassas kontrol düğmeleridir. Bu düğmeler yanlış ayarlandığında, birçok nadir genetik sendromda olduğu gibi, sonuç bilişsel, davranışsal ve metabolik semptomların sıkı bağlantılı bir kombinasyonu olabilir. Bu ortak kökenleri anlamak, nihayetinde yalnızca nöbet veya obezite gibi tek bir semptomu değil, bunların ortaya çıkmasına yol açan bağlantılı sistemi düzeltmeye yönelik tedavilerin yolunu açabilir.
Atıf: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Anahtar kelimeler: epigenetik, internöronlar, hipotalamus, nöbetler, obezite