Clear Sky Science · tr
Faz ayrışması ile fibrilleşmenin ayrılması biyomoleküler kondensatların aktivitesini korur
Beyin sağlığı için neden önemli
Alzheimer dahil birçok beyin hastalığı, zaman içinde proteinlerin sert, lifli yumaklar halinde kümelenmesini içerir. Aynı proteinler hücre içinde kimyayı düzenlemeye yardımcı olan daha yumuşak, damla benzeri yapılar da oluşturabilir; bunlar küçük, sıvı iş istasyonlarına benzer. Bu çalışma hayati bir soruyu soruyor: bu damlacıkların zararlı şekilde liflere sertleşmesini, faydalı gündelik işlevlerini yok etmeden engelleyebilir miyiz? Yazarlar, L-arginin adlı yaygın bir hücre metabolitinin Alzheimer ile ilişkili önemli bir protein olan Tau için tam da bunu yapabildiğini gösteriyor.
Serbest yüzen proteinden küçük damlacıklara
Hücre içinde bazı proteinler sıvı içerde her zaman eşit dağılmaz. Bunun yerine biyomoleküler kondensatlar denilen damlacıklar halinde toplanıp çok yumuşak jeller veya yoğun sıvılar gibi davranabilirler. Ekip, normalde mikro tübülleri—sinir hücreleri içinde yol işlevi gören boş filamentleri—oluşturmaya ve stabilize etmeye yardım eden Tau proteini üzerinde odaklandı. Tau aynı zamanda birçok nörodejeneratif hastalığı işaretleyen yumaklarda bulunan amiloid fibrilleri oluşturmasıyla kötü şöhretlidir. Tau damlacıklarının zaman içinde nasıl evrildiğini incelemek için araştırmacılar, deneysel olarak uygun bir zaman ölçeğinde aktif kondensatlardan amiloid fibrillere yaşlanan, sert katkılar gerektirmeyen SynTag-Tau adını verdikleri mühendislik bir Tau versiyonu ürettiler.
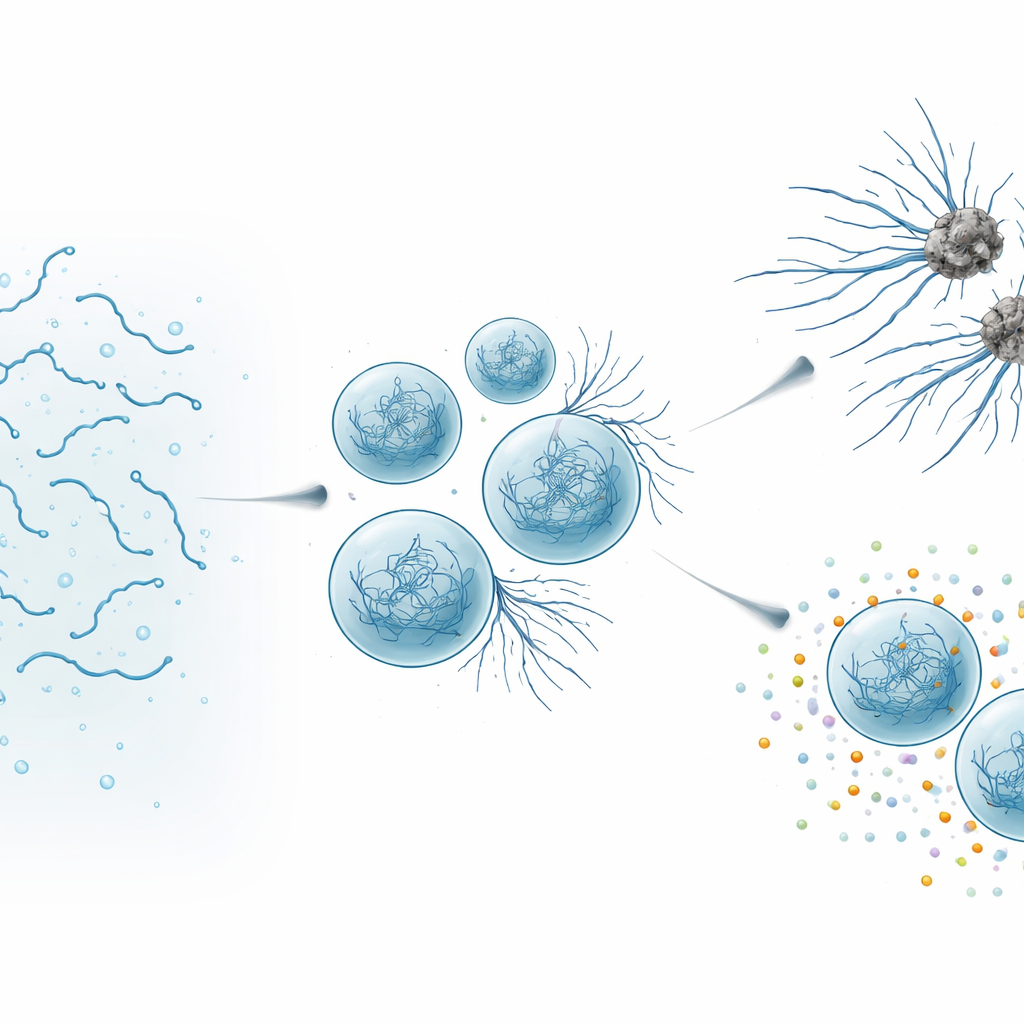
Yararlı damlacıklar zararlı hale geldiğinde
Yüksek çözünürlüklü mikroskopi ve biyofiziksel ölçümler kullanarak yazarlar SynTag-Tau damlacıklarının saatler içinde nasıl değiştiğini izlediler. Taze damlacıklar sıvı gibi davranıyordu: kolayca kaynaşıyor, molekülleri hızlı hareket ediyor ve düzenli yapı belirtisi yoktu. Zamanla damlacıklar yavaşladı ve sertleşti; ince lifler yüzeylerinden çevredeki çözeltiye doğru büyümeye başladı. Hassas optik yöntemler, bu liflerin amiloide özgü sıkı paketlenmiş “çapraz–beta” mimarisine sahip olduğunu gösterdi. Önemli olarak, yoğun damlacık ile çevreleyen sıvı arasındaki arayüz; fibrillerin ilk ortaya çıktığı bir sıcak nokta gibi davrandı. Damlacıklar yaşlandıkça ve daha fazla lif çıkarmaya başladıkça Tau’nun normal görevi zarar gördü: kondensatlar tubulini (mikrotübülün yapı taşı) çekmede zayıfladı ve sonunda mikrotübül montajını destekleme yeteneğini tamamen kaybetti.
Dengeyi değiştiren küçük moleküller
Araştırmacılar daha sonra basit metabolitlerin damlacıkların kendisini bozmadan sıvıdan liflere geçişi yavaşlatıp önleyip önleyemeyeceğini sordular. Birkaç doğal küçük molekülü tarayarak, pozitif yüklü amino asitler L-arginin ve L-lizin’in SynTag-Tau damlacıklarından amiloid fibril oluşumunu güçlü şekilde geciktirdiğini veya engellediğini, fakat gerçekçi düşük millimolar konsantrasyonlarda damlacık oluşumunu kapatmadığını buldular. Buna karşılık, glutamat ve aspartat gibi negatif yüklü amino asitler fibril oluşumunu hızlandırdı ve genel protein bozucu kimyasallar ya yardıma yaramadı ya da damlacıkları kendileri bozdu. L-argininin floresan bir analogu, bu molekülün dışarıda olmaktansa Tau kondensatlarının içinde bulunmayı tercih ettiğini göstererek, etkinin en çok ihtiyaç duyulan yerde gerçekleştiğini düşündürdü.
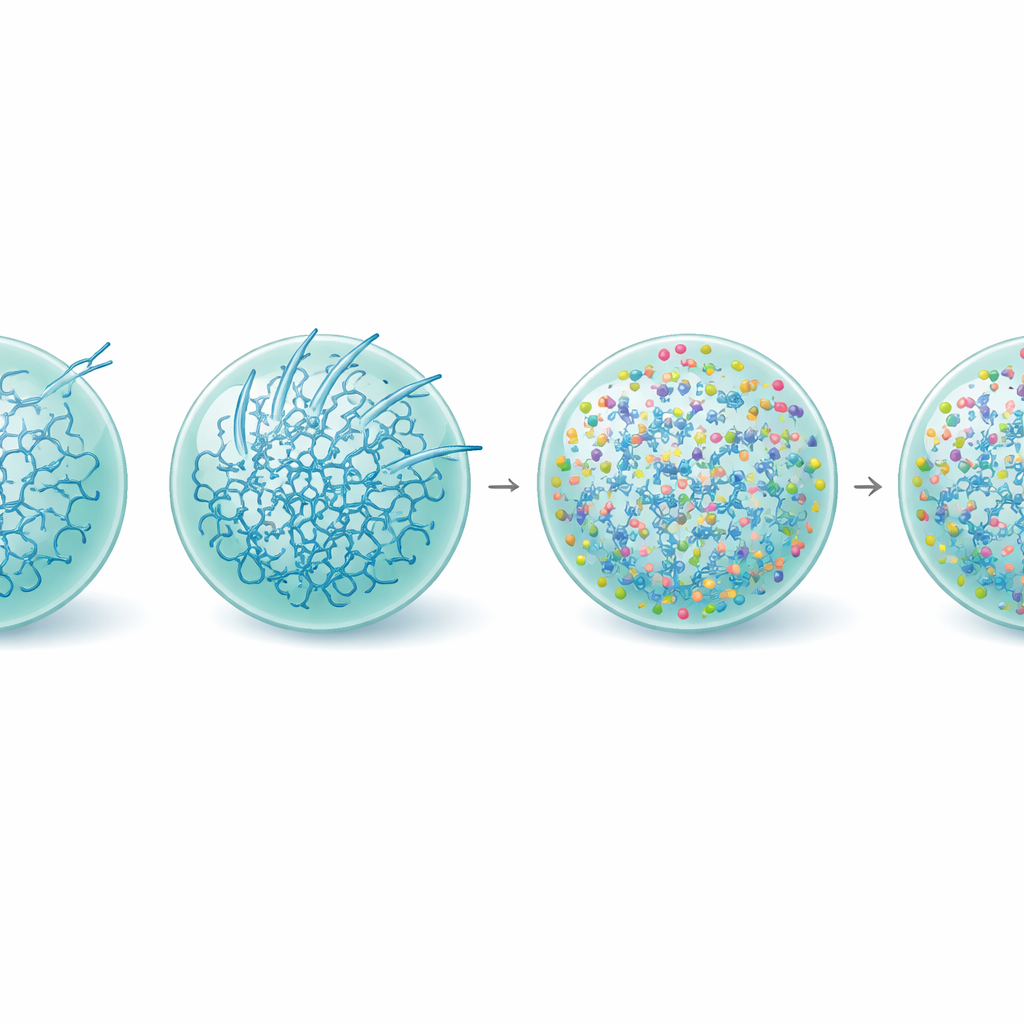
Damlacığı sertleştirmek, işlevi kurtarmak
Daha derine inerek ekip, L-argininin Tau damlacıklarının iç yaşamını nasıl yeniden şekillendirdiğini inceledi. Protein yapısı ölçümleri, L-arginin varlığında amiloide bağlı sert beta zengini biçimleri benimseyen Tau moleküllerinin fraksiyonunun, daha eski damlacıklarda bile azaldığını gösterdi. Video tabanlı nanorheoloji—kondensatlar içindeki küçük boncukların hareketini izleme—L-argininin Tau damlacıklarını aslında daha viskoelastik hale getirdiğini; yani iç ağın daha güçlü ve daha bağlantılı olduğunu, buna rağmen sıvımsı özelliklerini koruduğunu ortaya koydu. Bu güçlenmenin sistemi metastabil, işlevsel bir durumda tuttuğu ve özellikle damlacık yüzeyinde fibril oluşumu için gereken enerjik bariyeri yükselttiği görülüyor. Tutarlılık gösteren şekilde, L-arginin ile muamele edilen kondensatlar, tedavi edilmeyen damlacıklar inaktif hale geldikten çok sonra bile tubulini eşit şekilde toplamaya devam etti ve mikrotübül büyümesini destekledi.
Gelecekteki terapiler için ne anlama geliyor
Bu çalışma, protein damlacığı oluşumunu yönlendiren güçlerin ile zararlı lif oluşumunu yönlendiren güçlerin ilişkili ama ayrılabilir olduğunu gösteriyor. L-arginin gibi bir metabolitle kondensatlar içindeki kimyayı ayarlayarak, faydalı sıvımsı durumu korumak ve hastalıkla ilişkili amiloid liflere geçişi geciktirmek veya engellemek mümkün olabilir. Bu çalışma özel olarak mühendislik bir Tau sistemi kullanıyor olsa da bir ilke kanıtı sunuyor: kondensat stabilitesini seçici olarak güçlendiren küçük moleküller bir gün biyomoleküler kondensatların normal düzenleyici rollerini engellemeden hücreleri toksik protein agregatlarının yavaş birikiminden korumaya yardımcı olabilir.
Atıf: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Anahtar kelimeler: Tau proteini, biyomoleküler kondensatlar, amiloid fibriller, L-arginin, nörodejenerasyon