Clear Sky Science · tr
Pan-RAF inhibitörü exarafenib, BRAF sınıf II/III NSCLC hedef alıyor ve ARAF-KSR1 direncini ile kombinasyon stratejilerini ortaya koyuyor
Bu araştırma akciğer kanseri hastaları için neden önemli
Çoğu kişi belirli genetik değişiklikleri hedef alan kanser ilaçlarını duymuştur. Ancak BRAF adlı gende daha az görülen mutasyonları taşıyan birçok akciğer kanseri hastası için mevcut hedefe yönelik ilaçlar genellikle etkili olmuyor. Bu çalışma, daha geniş bir BRAF kaynaklı tümör yelpazesini hedeflemek üzere geliştirilen yeni deneysel ilaç exarafenib’i tanıtıyor ve kanser hücrelerinin ondan kaçınma yollarını açıklayarak bu tümörleri daha uzun süre kontrol altında tutabilecek kombinasyon tedavilerini ortaya koyuyor.
Gözden kaçan mutasyonların gizli çoğunluğu
Araştırmacılar öncelikle temel bir soruyu sordular: ileri evre kanserlerde, özellikle de küçük hücre dışı akciğer kanserinde (NSCLC), farklı BRAF mutasyon türleri ne kadar yaygın? 160.000’den fazla hastayı içeren çok geniş bir sıvı-biyopsi veritabanında dolaşımdaki tümör DNA’sı parçalarını analiz ettiler. Akciğer kanserinde BRAF mutasyonlarının yaklaşık %4–5 oranında görüldüğünü buldular; bu oran dünya çapında hâlâ binlerce insana denk geliyor. Kritik olarak, bu akciğer tümörlerinin yaklaşık üçte ikisi, mevcut onaylı BRAF ilaçlarının etkili şekilde hedeflemediği Sınıf II ve Sınıf III BRAF mutasyonlarını taşıyordu. Özellikle Sınıf II’ye sahip hastalar, daha tanıdık Sınıf I mutasyonlu hastalara göre daha kısa yaşam eğilimi gösteriyordu; bunun muhtemel nedeni Sınıf I hastaların yerleşik hedefe yönelik tedavilere erişimi olması, oysa Sınıf II/III hastaların çoğunlukla standart kemoterapi veya immünoterapi almasıydı.
Tüm yolu hedef alan yeni nesil bir ilaç
BRAF, hücre yüzeyinden çekirdeğe büyüme sinyallerini ileten proteinler dizisinde (MAPK yolu) yer alır. Mevcut birçok BRAF ilacı yalnızca tek bir mutant formu bloke edecek şekilde tasarlanmış olup normal hücrelerde ilişkili proteinleri istemeden uyarabiliyor. Exarafenib farklı inşa edildi: tekli veya çiftli formlarda birkaç RAF ailesi üyesini (ARAF, BRAF ve CRAF) kapatmak üzere tasarlanmış bir “pan‑RAF” inhibitörüdür ve çoğu diğer hücresel enzimi korumayı amaçlar. Yüzlerce insan kinazı üzerinde yapılan biyokimyasal testlerde exarafenib üç RAF proteinini güçlü biçimde bloke etti ancak hedef dışı etkileri sınırlı kaldı; bu da önceki pan‑RAF bileşiklerine kıyasla daha temiz bir güvenlik profili öneriyor.
Zor tedavi edilen tümör modellerinde güçlü etkiler
Araştırma grubu exarafenib’i farklı BRAF ve RAS mutasyonlarını taşıyan hücre hattı ve fare modelleri dizisinde, gerçekçi hasta kaynaklı tümörleri de içerecek şekilde test etti. Hücre kültürlerinde exarafenib, klasik BRAF V600E kanser hücrelerinde olduğu kadar Sınıf II ve Sınıf III mutasyonlu hücreler ile güncel olarak iyi hedefe yönelik seçenekleri bulunmayan birçok RAS-mutant hücresinde de büyümeyi durdurdu ve MAPK sinyalini kapattı. Bu değişiklikleri taşıyan akciğer tümörlü farelerde exarafenib, doza bağlı olarak tümörleri küçülttü veya büyümeyi yavaşlattı ve ilaç düzeyleri, yolak baskılanması ve tümör yanıtı arasında net ilişkiler gösterdi. İleri evre BRAF-mutant akciğer kanseri bulunan iki hastadan elde edilen erken klinik veriler — biri nadir bir BRAF füzyonuna sahip, diğeri ise Sınıf II nokta mutasyonlu — kısmi yanıtlar ve belirgin semptom rahatlaması gösterdi; bu da preklinik bulguların klinik açıdan anlamlı olduğunu destekliyor.
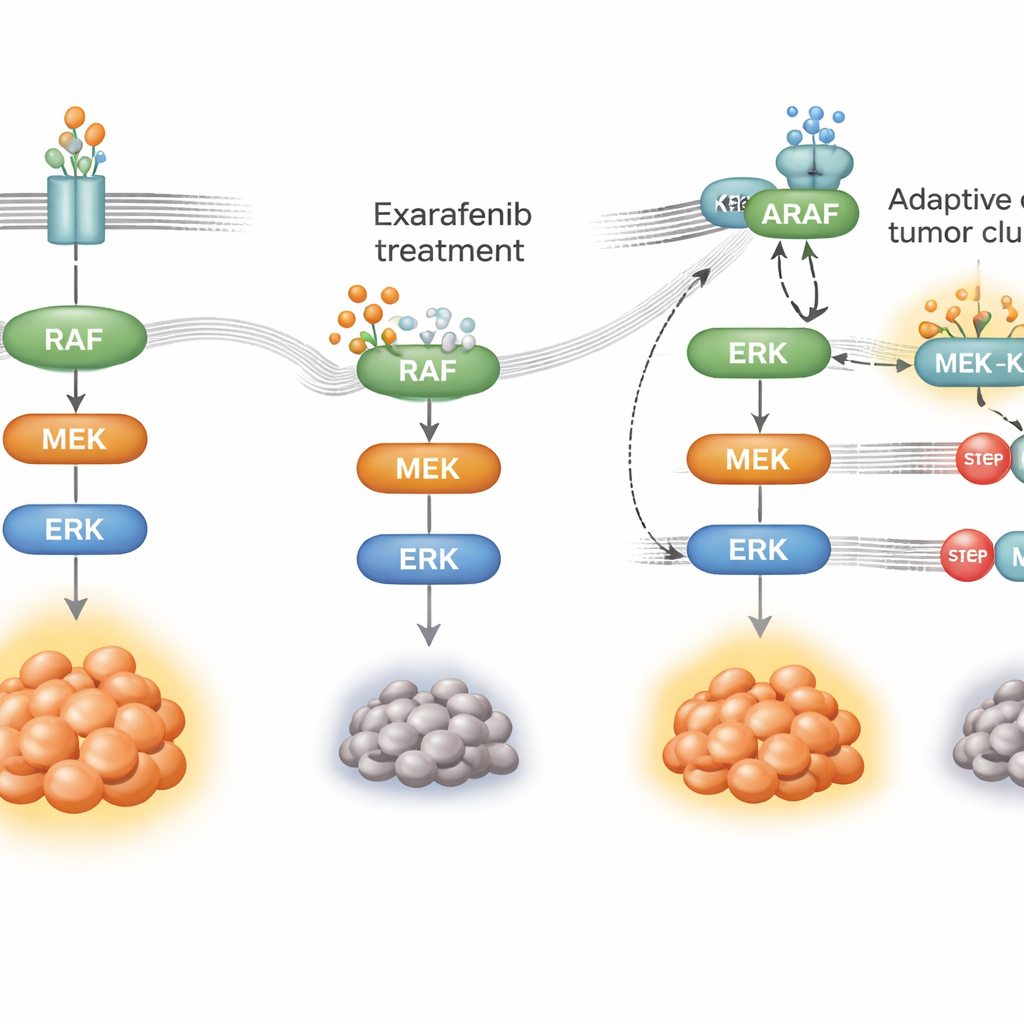
Kanser ilacı nasıl aşmayı öğreniyor
Hiçbir hedefe yönelik terapi sonsuza dek etkili olmaz; kanser hücreleri uyum sağlar. Tümörlerin exarafenib’e nasıl direnç geliştirebileceğini görmek için araştırmacılar BRAF‑mutant akciğer kanseri hücrelerini aylarca ilaca maruz bıraktı ve dirençli popülasyonlar ortaya çıktı. Bu hücreler hâlâ aynı büyüme yoluna dayanıyordu ama bunu kullanma biçimlerini yeniden kablolu hale getirmişlerdi. Başlıca mutant BRAF’a bağımlı olmak yerine, yukarı akışta bir anahtar olan RAS’ın etkinliğini artırdılar ve ARAF adlı başka bir aile üyesini, iskelet proteini KSR1 ile birlikte kullanmaya yöneldiler. İlaç baskısı altında ARAF ve KSR1 sıkı kompleksler oluşturarak exarafenib bağlı olsa bile MAPK iletimini sürdürmeye yardımcı oldu. Bilim insanları ARAF veya KSR1’i seçici olarak susturduğunda veya RAS aktivitesini azalttıklarında, dirençli hücreler tekrar exarafenib’e duyarlı hale geldi ve hayatta kalma sinyalleri çöktü.
Direncin önüne geçmek için kombinasyon stratejileri
Bu mekanistik haritayla donanmış ekip, hem orijinal hem de baypas yolları tarafından paylaşılan boğaz noktalarını bloke edebilecek eş ilaçları aradı. Exarafenib’i MEK veya ERK inhibitörleriyle eşlemenin — MAPK iletimi içinde önemli aşağı akış adımları — birçok hücre ve fare modelinde güçlü bir sinerji ürettiğini buldular; bu modeller arasında doğuştan daha az duyarlı olanlar veya direnç kazanmış tümörler de vardı. Bu kombinasyonlar yolak baskısını daha uzun süre sürdürdü, daha fazla hücre ölümü tetikledi ve hayvanlarda genellikle tek başına yüksek doz exarafenib’e eşdeğer ya da daha iyi etki gösterdi; belirgin ek toksisite gözlemlenmedi. RAS’ı doğrudan hedefleyen ajanlar da, dirençte RAS’ın açıkça etkin olduğu modellerde exarafenib’in etkisini artırdı ve bu da başka bir klinik olarak umut verici taktiği işaret ediyor.
Hastalar için bunun anlamı
Sınıf II veya Sınıf III BRAF mutasyonları taşıyan NSCLC’li kişilerde — ya da karmaşık BRAF füzyonları ve eşzamanlı RAS mutasyonları bulunan hastalarda — şu anda onaylı hedefe yönelik tedaviler bulunmuyor ve sonuçlar daha yaygın değişikliklere sahip hastaların gerisinde kalıyor. Bu çalışma, exarafenib’in RAF kaynaklı sinyallemeyi geniş biçimde kapatarak bu boşluğu doldurabileceğine dair güçlü bir bilimsel gerekçe sunuyor. Ayrıca tümörlerin ARAF‑KSR1 baypası yoluyla uyum sağlayabileceğini açıklıyor ve özellikle RAF ile MEK inhibitörlerinin kombinasyonu veya RAS inhibitörlerinin eklenmesi yoluyla yolak üzerinde birden fazla seviyeden müdahale etmenin daha derin ve daha kalıcı tümör kontrolü sağlayabileceğini gösteriyor. Birlikte bu bulgular, geniş ve daha önce yeterince hizmet verilmeyen bir akciğer kanseri hasta grubuna yönelik hedefe yönelik, kombinasyonlu tedavileri klinik denemelere taşımaya yönelik bir yol haritası çiziyor.
Atıf: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Anahtar kelimeler: BRAF-mutant akciğer kanseri, pan-RAF inhibitörü, MAPK sinyal iletimi, ilaç direnci, hedefe yönelik tedavi kombinasyonları