Clear Sky Science · tr
Hücre içi elektron kristalografisiyle tek hücre yapısal biyolojisi
Hayatın Şekli: Hücre Hücre Görmek
Proteinler her hücreyi canlı tutan küçük makineler gibidir; ancak bunların nasıl çalıştığını gerçekten anlamak için bilim insanlarının üç boyutlu biçimlerini ince ayrıntıyla görmesi gerekir. Geleneksel olarak bu, büyük miktarlarda proteinin saflaştırılması ve hücre dışında büyük, kırılgan kristallerin yetiştirilmesini gerektirir—bu sıklıkla yavaş ve başarısızlığa açık bir süreçtir. Bu çalışma, X-ışınları yerine elektronlar kullanarak tek bir hücre içindeki tek bir kristalden doğrudan protein yapısını okumanın yeni bir yolunu sunuyor. Bu, yüksek çözünürlüklü yapısal biyolojinin sıradan laboratuvarlarda ve hatta tek tek hücre düzeyinde yapılabileceği bir geleceğe işaret ediyor.
Canlı Hücrelerin İçinde Gizlenmiş Kristaller
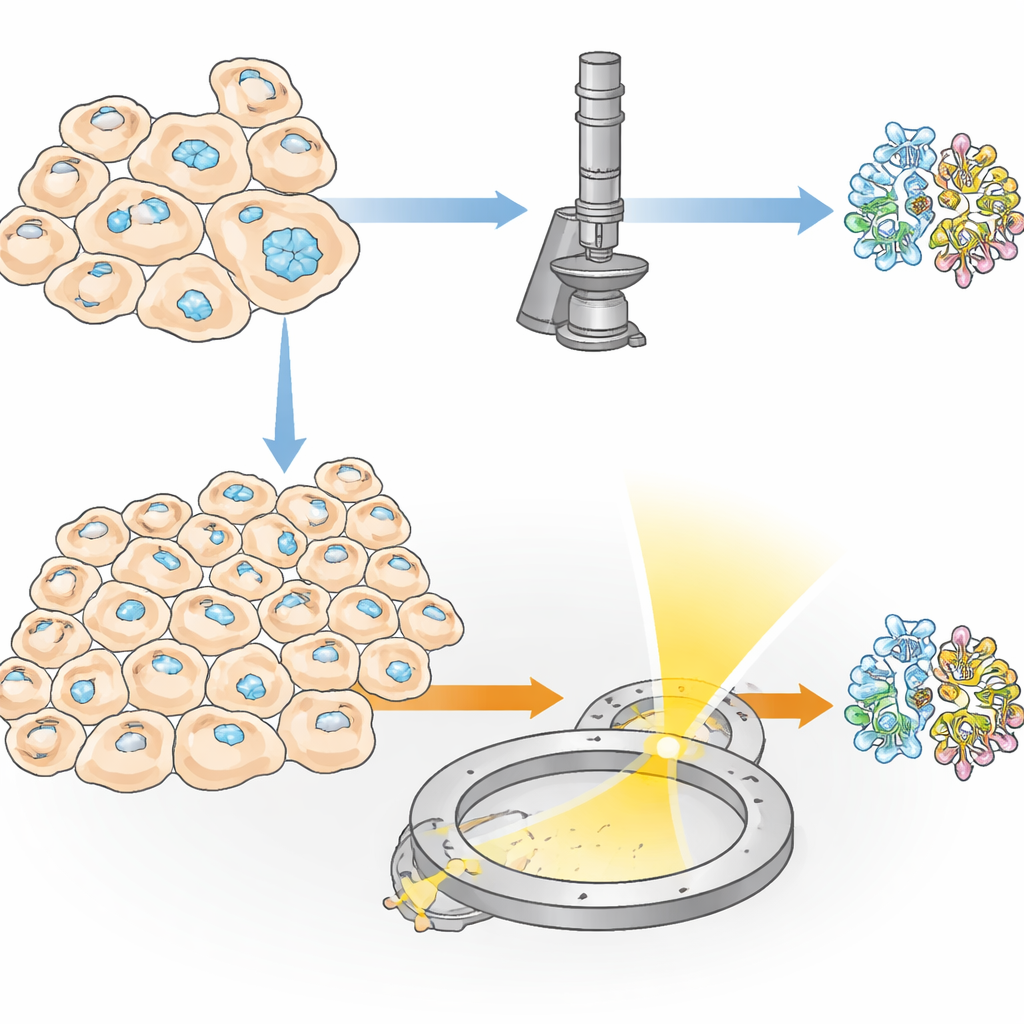
Bazı proteinler, depolama, koruma ya da hücrelerin strese yanıt vermesine yardımcı olma gibi amaçlarla canlı hücrelerin içinde doğal olarak küçük kristaller halinde toplanır. Araştırmacılar ayrıca hücreleri, seçtikleri bir proteinin yüksek miktarlarda üretilmesi için mühendislik yaparak böyle kristaller üretmeye zorlayabilirler. Bu “hücre içi” kristalleşmenin iki büyük avantajı vardır: protein doğal benzeri ortamından çıkmaz ve şeker süslemeleri ya da küçük bağlı moleküller gibi hassas özellikler, standart deney tüpü kristalleşmesinde sıklıkla kaybolduğu şekillerde korunabilir. Ancak önemli bir engel kalmıştır: birçok deneyde yalnızca çok küçük bir hücre fraksiyonu gerçekten kristal oluşturur, bu yüzden geleneksel X-ışını yöntemleri on binlerce kristal ve dolayısıyla çok büyük sayıda hücre gerektirir.
Yeni Bir Yol: X‑Işınları Yerine Elektronlar
Yazarlar IncelluloED adını verdikleri bir yöntem tanıtıyor; bu yöntem hücre içi kristalleşmeyi üç boyutlu elektron kırınımıyla birleştiriyor. Elektronlar, X-ışınlarına göre maddeyle çok daha güçlü etkileşir; bu da hem daha küçük hem de sayıca daha az kristalden faydalı verilerin elde edilebileceği anlamına geliyor. Ekip, normalde stres altında mantar hücreleri arasındaki çok küçük gözenekleri tıkamaya yardımcı olan altıgen kristaller oluşturan HEX‑1 adlı bir mantar proteini seçti. Bu proteini böcek hücrelerinde üreterek yeni hattın test vakası olarak hizmet eden düzenli mikroskobik kristaller yarattılar.
Tek Bir Kristali Ayrıntılı Bir Haritaya Dönüştürmek
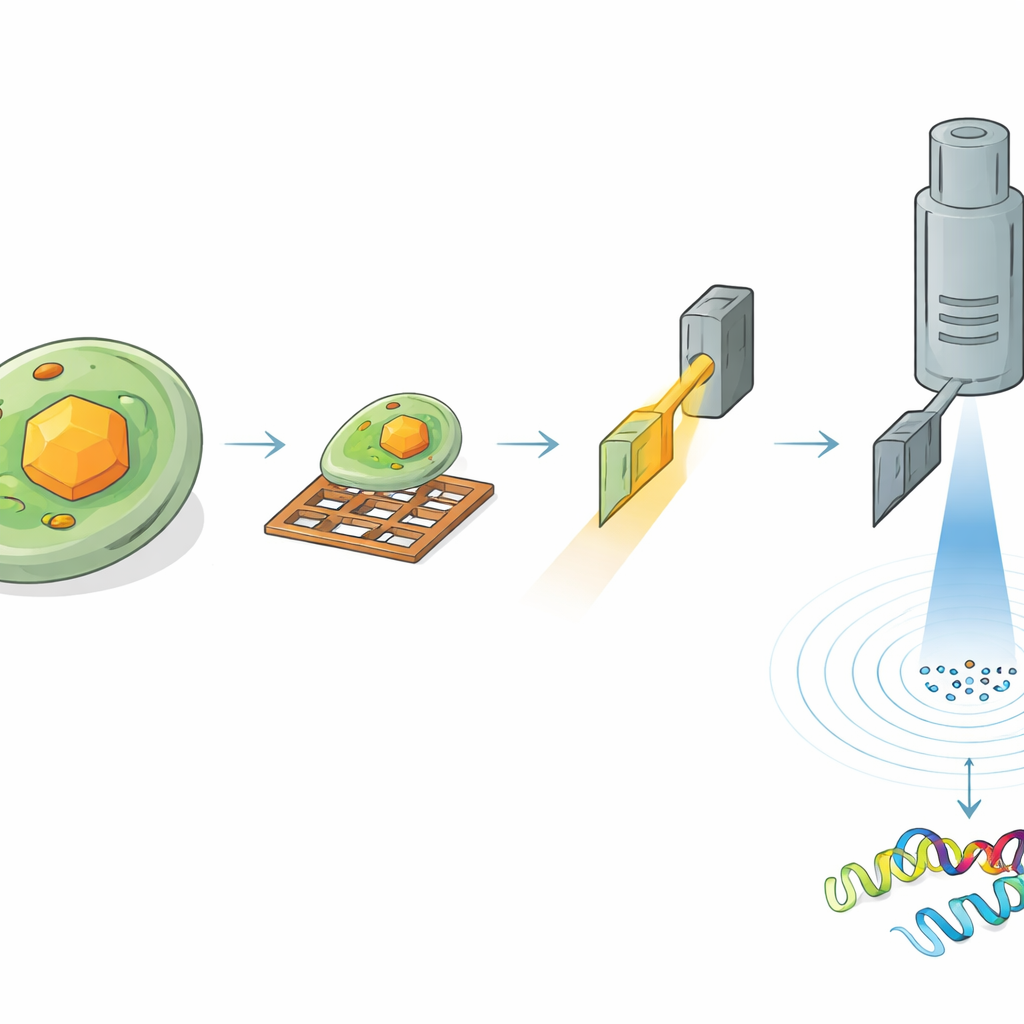
HEX‑1’in hücre içindeki yapısını okumak için araştırmacıların örneğin doğru bölgesini bulup dikkatlice inceltmeleri gerekiyordu. Önce kristal içeren hücreleri küçük metal ızgaralar üzerinde dondurdular ve yüzeyi ince bir platinyum tabakasıyla kapladılar. Kriyojenik ışık mikroskobu kullanarak, ızgaranın geniş alanlarını tarayıp kristal içeren hücreleri buldular ve kristallerin yüzey altındaki üç boyutlu konumlarını ölçtüler. Ardından aynı örneği taramalı elektron mikroskobunu odaklanmış iyon ışınıyla birleştiren özel bir cihaza taşıdılar. Önceki ışık görüntüleri yol göstericiliğinde, çevre materyalleri öğüterek seçilen bir kristalden geçen ve elektronların geçişi için ideal olan sadece birkaç yüz nanometre kalınlığında ultra ince bir dilim veya lamella çıkardılar.
Elektronlar Mikroskobik Hacimlerden Atomik Ayrıntılar Açığa Çıkarıyor
Hazırlanan lamellalar daha sonra kriyo sıcaklıkta çalışan yüksek uç bir elektron mikroskobuna aktarıldı. Kristal dilim mikroskopta yavaşça döndürülürken, kontrollü bir elektron demeti ondan geçerek atomların konumlarını şifreleyen bir dizi kırınım deseni—narince nokta düzenleri—oluşturdu. Yaklaşık 1,6 kübik mikrometre hacmindeki bir kristal hacminden ekip, HEX‑1’in tam 3B yapısını 1,9 ångström çözünürlükte yeniden inşa etti; bu, proteinin çoğu yan zincirini modellemeye yetecek kadar keskinti. Yaklaşık 0,8 kübik mikrometre kadar daha küçük hacimler de yalnızca biraz daha düşük çözünürlükle neredeyse aynı yapıyı verdi. Önemli olarak, ortaya çıkan modeller, 60.000’den fazla kristal gerektiren ve toplam kristal hacmi kabaca yedi milyon kat daha büyük olan geleneksel seri X-ışını yaklaşımıyla elde edilenlerle yakından eşleşti.
Bu, Yapısal Biyolojiyi Nasıl Değiştirir
Yan yana karşılaştırmalar, tek bir hücre içi elektron-kırınım kristalinden belirlenen yapının esasen X-ışınlarıyla on binlerce kristalin ortalamasından elde edilenle aynı olduğunu gösterdi. Farklılıklar küçük ve çoğunlukla esnek döngülere sınırlıydı; buralarda doğal hareket beklenir. Araştırmacılar ayrıca kullanılmış elektron dozlarının ciddi radyasyon hasarından kaçınmak için yeterince düşük olduğunu ve işledikleri her kristalin yüksek kaliteli veri ürettiğini gösterdiler. İnce lamellaların hazırlanması hâlâ ustalık ve zaman gerektirse de, gerekli cihazlar—kriyo-ışık mikroskopları, odaklanmış iyon ışını sistemleri ve kriyo-elektron mikroskopları—şimdi birçok araştırma merkezinde yaygın hale geldi.
Çok Sayıda Hücreden Tek Hücrelik Yapısal Laboratuvara
Bu çalışma, proteini asla saflaştırmadan tek bir hücre içindeki yalnızca bir kristalden atom düzeyinde bir protein yapısını belirlemenin artık mümkün olduğunu gösteriyor. IncelluloED, yalnızca birkaç hücre kristal oluşturduğunda veya proteinlerin önemli ortakları ya da kimyasal grupları kaybetmeden izole edilmesinin zor olduğu durumlarda özellikle güçlü olabilir. İş akışı daha fazla otomatikleştikçe ve diğer proteinlere genişletildikçe, yapıların hücreden hücreye nasıl değiştiğini keşfetmeye, hastalıkla ilişkili değişiklikleri doğal ortamında incelemeye ve hatta ilaç keşfini doğrudan canlı hücrelerde desteklemeye olanak sağlayabilir. Aslında, çalışma “tek hücre yapısal laboratuvarı” vizyonunu gerçeğe çok daha yakınlaştırıyor.
Atıf: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Anahtar kelimeler: elektron kırınımı, hücre içinde kristalografisi, tek hücre yapısal biyolojisi, protein yapısı, cryo-EM