Clear Sky Science · tr
DoxA'nın yapısal analizi ve P450-redoks partner optimizasyonu ile doksorubisinin biyosentezinin metabolik mühendisliği
Bir kanser ilacının köken hikâyesi neden önemlidir
Doksorubisin, lösemiden meme tümörlerine kadar çeşitli kanserlerin tedavisinde kullanılan modern kemoterapinin en önemli ilaçlarından biridir. Buna rağmen onlarca yıllık kullanıma karşın bu ilacın üretim yolu şaşırtıcı derecede dolambaçlıdır: endüstri genellikle onu ilgili bir bileşikten inşa eder, üretici mikroorganizmanın işi tamamlamasına izin vermez. Bu çalışma, üretici bakterinin son kimyasal adımları neden verimli şekilde tamamlamakta zorlandığını ortaya koyuyor ve hücre içi mekanizmalarını yeniden tasarlayarak tam doksorubisin verimini keskin şekilde artırmanın yollarını gösteriyor; bu da daha güvenilir ve potansiyel olarak daha ucuz tedariklerin önünü açıyor.
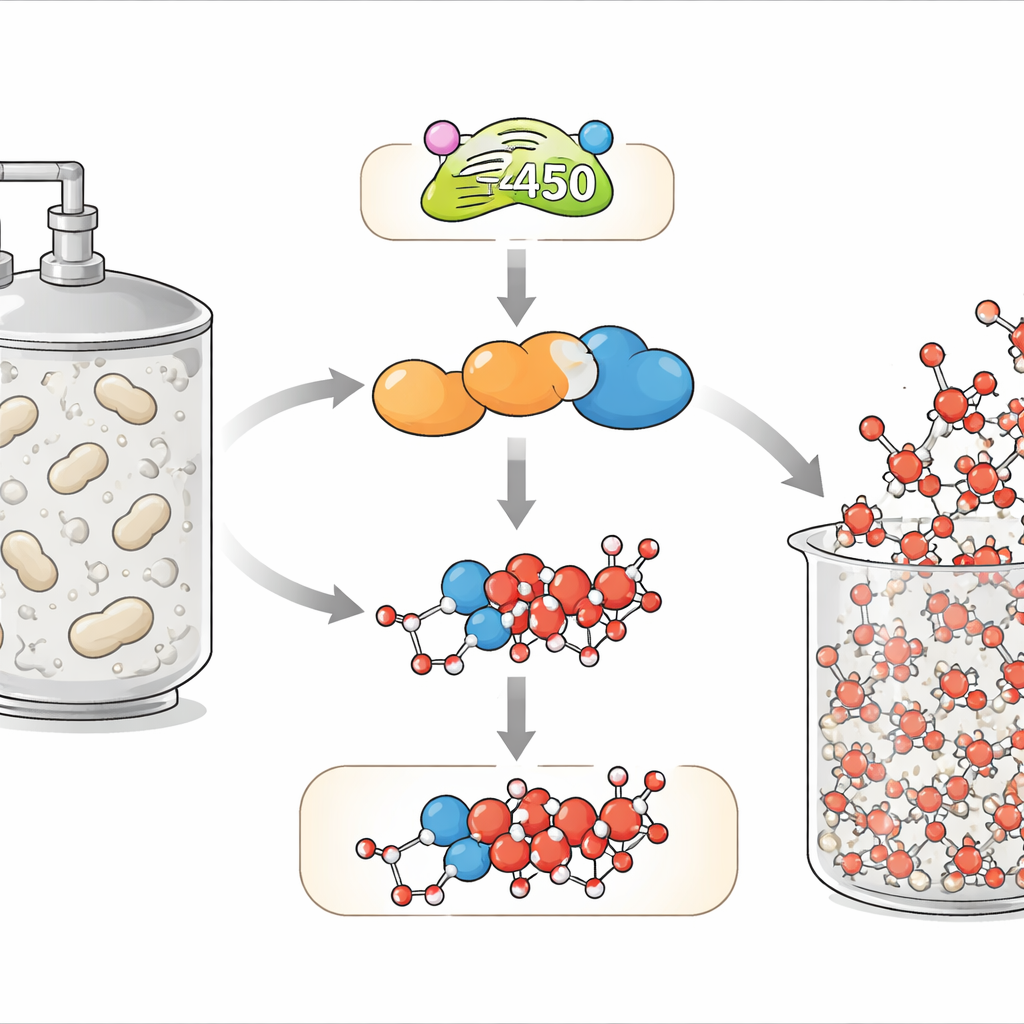
Toprak bakterilerinden hayat kurtaran ilaca
Doksorubisin, toprak bakterileri Streptomyces cinsince üretilen doğal moleküller ailesi olan antrasiklinlerin bir üyesidir. Bu bileşikler, DNA baz çiftleri arasına giren sert, düz bir karbon iskeleti ve DNA oluklarına yerleşen bir şeker birimi paylaşır. Bu özellikler birlikte hücrenin DNA ile ilgili makinelerini kilitler ve nihayetinde hücre ölümünü tetikler — hızlı bölünen kanser hücrelerine karşı etkili olur. Klasik üretici Streptomyces peucetius doğal olarak çoğunlukla daunorubisin adında bir öncül ilaç üretir ve yalnızca daha etkili olan doksorubisini sınırlı miktarda yapar; aradaki fark yalnızca tek bir ekstra oksijen taşıyan gruptur. Bu küçük yapısal değişiklik etkinliği dramatik olarak artırır ama mikro-organizma için verimli şekilde gerçekleştirmesi şaşırtıcı derecede zordur.
Hücre içindeki doğru elektrik bağlantısını bulmak
İlacın iskeletinde son üç oksidasyon adımını gerçekleştiren kritik enzim DoxA olarak adlandırılır ve sitokrom P450 ailesinin bir üyesidir. Mini bir kimyasal fabrika gibi, DoxA oksijeni aktive etmek ve ilaç molekülüne yeni oksijen atomları eklemek için sürekli bir elektron akışına ihtiyaç duyar. Bakteri içinde bu elektronlar redoks partnerleri olarak bilinen yardımcı proteinler aracılığıyla sağlanır. S. peucetius genomu birkaç aday içerdiği için hangilerinin gerçekten DoxA ile eşleştiği belirsizdi. Normal bir saf suş, daunorubisin açısından zengin bir mutant ve doksorubisin açısından zengin bir mutantta gen aktivitesi ve metabolizmayı karşılaştırarak araştırmacılar doğal partnerler olarak bir ferredoksin (Fdx4) ve bir ferredoksin redüktazı (FdR3) belirlediler. Bu üçlüyü test tüpü reaksiyonlarında yeniden kurmak, DoxA'nın doğru elektron aktarım zincirine bağlandığında en iyi şekilde çalıştığını doğruladı; bu, doğru güç adaptörünü bir cihaza takmaya benzetilebilir.
Enzimin kendi yarattığı yavaşlamasını gidermek
Doğru elektrik bağlantısına rağmen DoxA, daunorubisin'i doksorubisin'e dönüştüren son adımda genellikle tıkanma eğilimindedir. Önceki çalışmalar ürünün kendisinin enzimi tıkayabileceğini öne sürmüştü. Ekip, işlevi belirsiz olan komşu bir gen olan dnrV'ye yöneldi. Biyokimyasal testler DnrV proteininin doksorubisin de dahil olmak üzere çeşitli antrasiklin moleküllerine kimyasal olarak değiştirmeden sıkı şekilde bağlandığını gösterdi. DnrV'yi DoxA reaksiyonlarına eklemek, kimyanın akışını büyük ölçüde iyileştirerek öncüleri son ilaca tam dönüşüme uğratılmasını sağladı ve yıkıcı yan reaksiyonları önledi. Pratik açıdan DnrV, taze üretilen doksorubisini emen içsel bir sünger gibi davranır; böylece ilacın enzimi tıkamasını veya üreten hücre içinde DNA'ya zarar vermesini engeller.
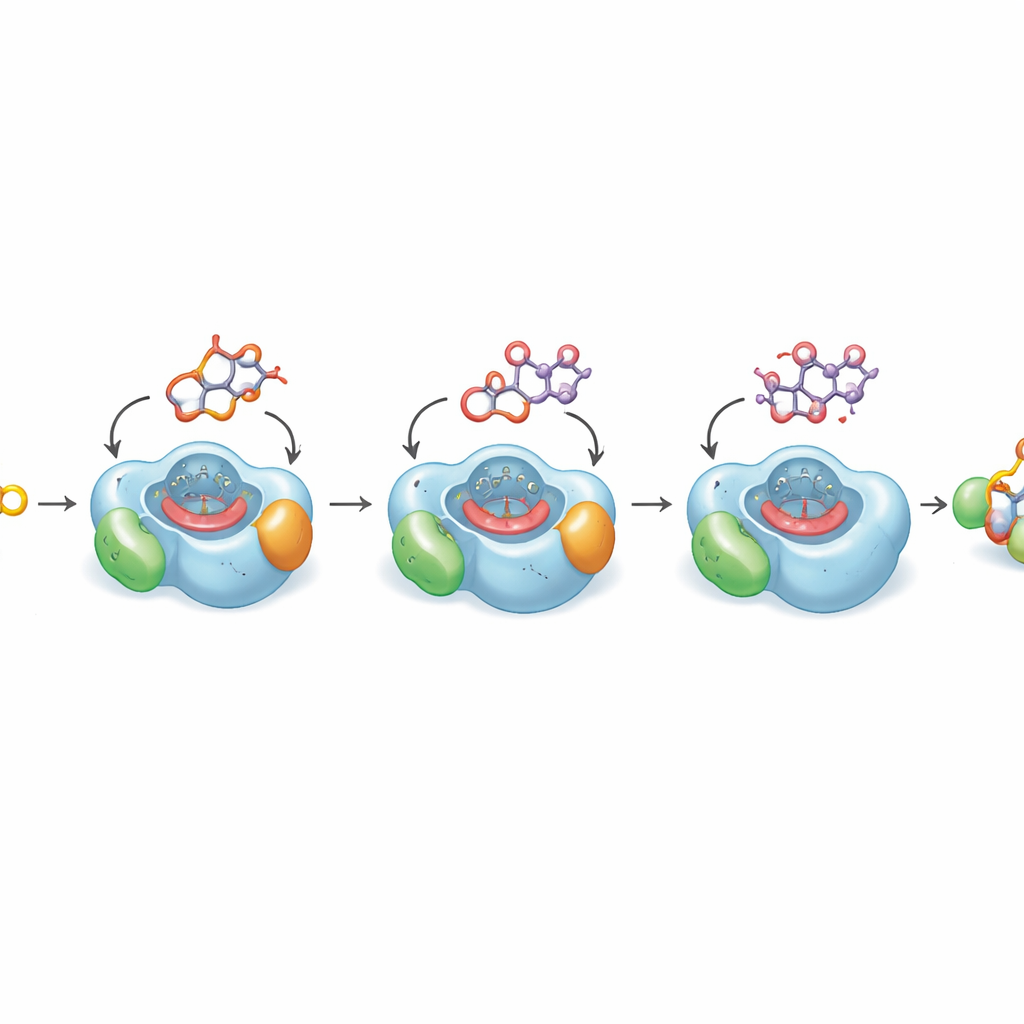
Son adımın neden bu kadar yavaş olduğunu görmek
Anahtar son oksidasyonun doğası gereği neden yavaş olduğunu anlamak için yazarlar DoxA'nın üç ardışık ara ürünle bağlanmış yüksek çözünürlüklü kristal yapısını çözdüler. Bu yapılar, düz ilaç çekirdeğinin ve bağlı şekerinin enzimin heme grubunun üzerinde sıkı bir cebe nasıl yerleştiğini gösteriyor; heme, oksidasyonu gerçekleştiren reaktif metal merkezidir. Daha erken adımlar için değiştirilecek karbon atomu heme'ye yakın, reaksiyon için ideal bir konumdadır. Ancak son substrat olan daunorubisinin hidroksileştirilmesi gereken kısmı, heme'den uzaklaşıp küçük yağlı bir boşluğa doğru bükülür; kuantum hesaplamaları bunun enerji açısından tercih edildiğini gösteriyor. Mikrosaniye ölçeğinde bilgisayar simülasyonları, molekülün son oksijen eklemesi için verimli bir konumu nadiren ziyaret ettiğini doğruluyor. Bu yapısal eğilim, doksorubisine dönüşümün doğası gereği verimsiz olmasını açıklıyor.
Daha iyi doksorubisin üreten bir suş inşa etmek
Bu bulgularla donanmış araştırmacılar rastgele mutageneze güvenmek yerine bakteriyi akılcı şekilde yeniden tasarladılar. Üretimi stabilize etmek için bir DNA onarım geni tanıttılar, ardından ekstra kopyalarını dikkatle seçilmiş promotörler altında dengelemek için doxA, optimal redoks partnerleri fdx4 ve fdr3 ile yardımcı bağlayıcı dnrV'yi yerleştirdiler. Kültür koşullarını da ince ayarladılar ve toksik ve yapışkan ara ürünleri emmek için özel reçineler kullandılar. Laboratuvar şişelerinde ve 20 litrelik bir biyoreaktörde en iyi mühendislikli suş, litre kültürde 336 miligram doksorubisin ve doksorubisin:daunorubisin oranı 81:19 olacak şekilde üretti—başlangıç suşuna göre yaklaşık %180 artış ve çok daha temiz bir ürün karışımı sağladı.
Gelecekteki kanser ilacı tedariki için bunun anlamı
Elektriksel destek sistemini ve anahtar bir enzimin 3B yapısını ayrıştırarak, bu çalışma tıbbi açıdan hayati olan bir mikroba neden en değerli antrasiklinimizi üretmede yetersiz kaldığını açıklıyor. DoxA'yı doğal redoks partnerleriyle eşleştirmek, bir ilaç bağlayıcı yardımcı protein eklemek ve gen ifadesini yeniden dengelemek isteksiz bir üreticiyi dayanıklı bir hale dönüştürdü. Daha ileri enzim ayarlamaları son kimyasal adımı daha da hızlandırabilse de çalışma zaten tamamen biyolojik doksorubisin üretimini endüstriyel gerçekliğe bir hayli yaklaştırıyor. Hastalar ve sağlık sistemleri için bu tür ilerlemeler, temel bir kemoterapi ilacına daha güvenli, ölçeklenebilir ve maliyet‑etkin erişim anlamına gelebilir.
Atıf: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Anahtar kelimeler: doksorubisin üretimi, antrasilin biyosentezi, enzim mühendisliği, mikrobiyal ilaç üretimi, sitokrom P450