Clear Sky Science · tr
Atipik protein kinaz C aktivasyonu diyabette bağırsaktan glikoz atılımını artırıyor
Bağırsak: Bir Şeker Vanasına Dönüştürmek
Diyabetliler kanlarında aşırı şekerle yaşarlar. Gastrik bypass gibi bariatrik ameliyatlar, kilo kaybı henüz belirgin olmadan bile kan şekerini şaşırtıcı biçimde hızla normale döndürebilir; bunun nasıl gerçekleştiği uzun süredir bir sırdı. Bu çalışma, bağırsakta bulunan bir “şeker vanasını” ortaya koyuyor — bağırsağın kan dolaşımından şeker çekip bir kısmını tekrar bağırsak boşluğuna atmasını sağlayan bir yol — ve ameliyatın yararlarını cerrahi olmadan taklit edebilecek yeni bir ilaç hedefi öneriyor.
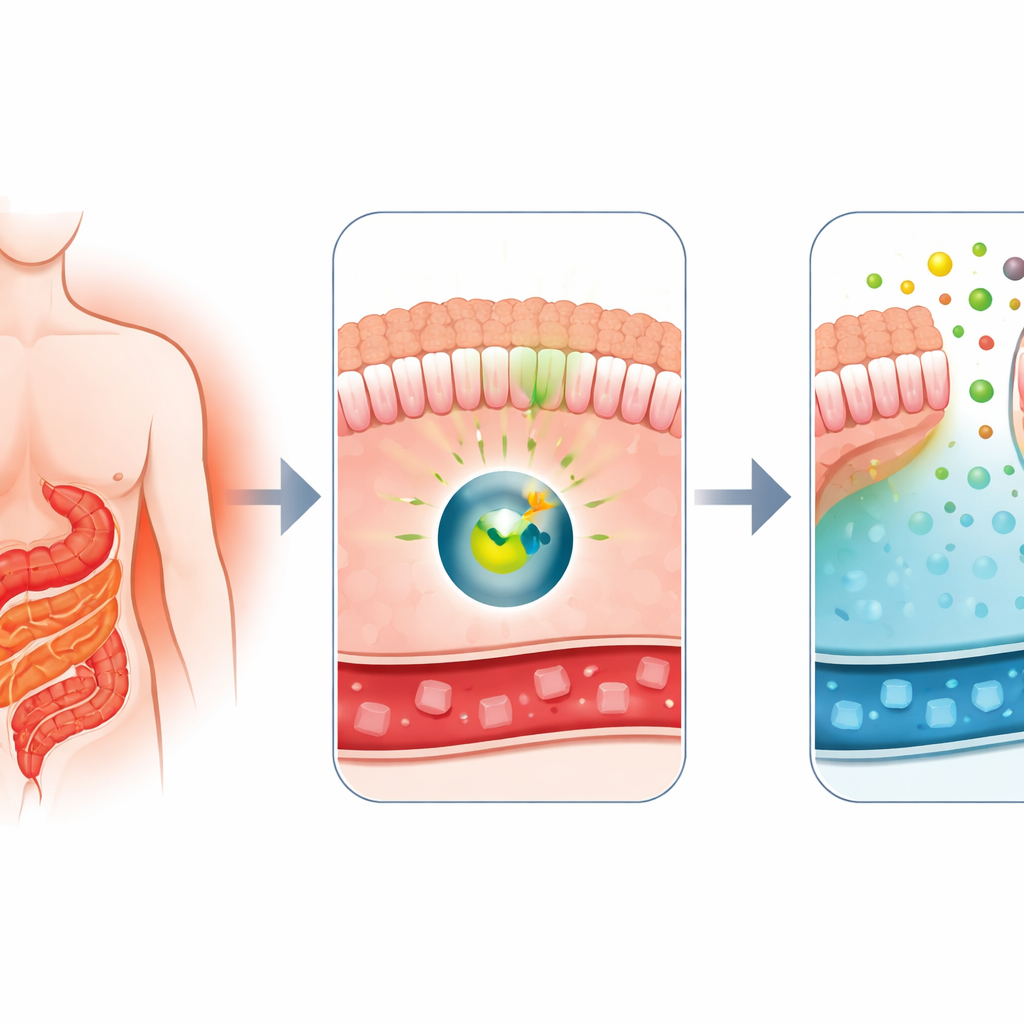
Ameliyat Kan Şekerini Neden Bu Kadar Hızlı Değiştirir
Hekimler uzun zamandır Roux-en-Y gastrik bypass’ın, yaygın bir kilo verme ameliyatı olmasının yanı sıra tip 2 diyabet için de en etkili tedavilerden biri olduğunu biliyorlar. Ameliyattan kısa süre sonra hastaların kan şekeri sıklıkla çarpıcı biçimde düzelir; bu, fazla kilo verilmeden önce bile görülür. Bu grubun önceki çalışmaları, bypass sonrası ince bağırsağın belirli bölümlerinin bir sünger gibi davranmaya başlayıp kan dolaşımından glikozu emdiğini ve bir kısmını bağırsak içine bıraktığını göstermişti. Bu tuhaf davranış, bağırsaktan glikoz atılımı olarak adlandırıldı ve GLUT1 adlı bir taşıyıcı proteine dayanıyor gibi görünüyordu. Büyük soru şuydu: bağırsakta bu şekeri temizleme modunu başlatan moleküler anahtar nedir?
Moleküler Anahtarı Bulmak İçin Büyük Veri Kullanmak
Bu anahtarı aramak için araştırmacılar, binlerce kimyasalın hücrelerde gen etkinliğini nasıl değiştirdiğini içeren Connectivity Map veri tabanına dayanan büyük ölçekli bir hesaplamalı ilaç keşif sistemi kullandılar. Bypass geçirmiş sıçan dokusu ve bağırsak büyüme sinyaliyle muamele edilmiş hücreler gibi bağırsaktan glikoz atılımının yüksek olduğu beş durumdan elde edilen gen ifade desenlerini bilinen ilaçların ürettiği desenlerle karşılaştırdılar. Tutarlı şekilde öne çıkan bir bileşik sınıfı vardı: hücre içi sinyal ileten enzim ailesi olan protein kinaz C (PKC) aktivatörleri. Daha derine inince ekip, PKC enzimlerinin “atipik” alt grubuna, özellikle de bağırsak hücrelerindeki etkinliği bypass-benzeri, glikoz atılımı durumuna en çok uyan PKCζ adlı üyesine odaklandı.
Bağırsak Hücrelerindeki Şeker Pompası İşbaşında
Tek hücre RNA dizilemesiyle bireysel bağırsak hücrelerine yaklaştıklarında, yazarlar bypass ameliyatının distal ince bağırsağın besin emen özel hücrelerinde hem PKCζ hem de GLUT1’i artırdığını buldular. Hücre kültürlerinde ve insan bağırsak organoidlerinde yapay olarak PKCζ’yi yükseltmek ya da bitkisel kökenli ve bu atipik PKC enzimlerini güvenli şekilde aktive eden prostratin ile muamele etmek, GLUT1’in hücre yüzeyine taşınmasını sağladı. Orada GLUT1 iki yönlü bir pompa gibi davrandı: hücrelerin kana bakan tarafından daha fazla glikoz çekti ve fazla glikozun bağırsak boşluğuna çıkmasına izin verdi. Önemli olarak, bu şeker yönlendirmesi hücrelerin kendi şeker yakımını (glikoliz) anlamlı şekilde hızlandırmadı; bu da temel etkinin ekstra enerji üretimi değil, glikozun bertaraf edilmesi olduğunu gösteriyordu.
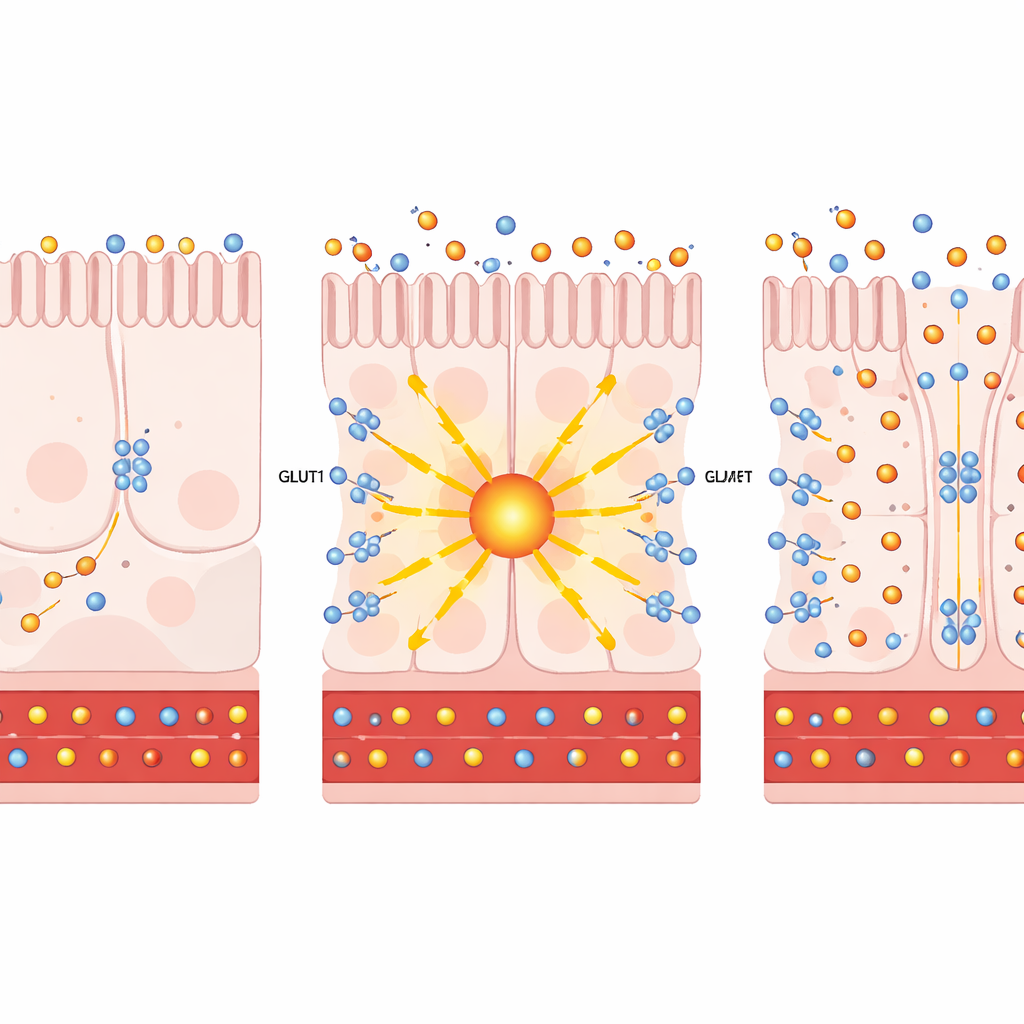
Hücrelerden Farelere: Bıçağa Gerek Olmadan Ameliyatı Taklit Etmek
Ekip ardından bu yolun canlı hayvanlarda aktive edilmesinin diyabeti iyileştirip iyileştirmeyeceğini test etti. Obez, insüline dirençli farelerde PKCζ’yi özel olarak bağırsaklara verince kilo alımı yavaşladı, açlık kan şekeri düştü ve glikoz toleransı iyileşti. Radyoaktif şeker izleyicileri, distal bağırsağın daha fazla şeker aldığı ve bunun bağırsak lümenine yıkandığını gösterdi. Prostratin ile tedavi edilen diyabetik fare modellerinde benzer bir tablo ortaya çıktı: daha az kilo aldılar, şeker yüklerini daha iyi idare ettiler ve daha fazla glikozu bağırsak yoluna yönlendirdiler; tüm bunlar insülin düzeylerinde, yiyecek alımında veya bağırsak bariyer bütünlüğünde değişiklik olmadan gerçekleşti. Doku dilimlerinde GLUT1 hem kana bakan hem de bağırsak boşluğuna bakan yüzlerde görünerek, şekeri dolaşımdan çekip bağırsak içine itmek için ideal bir konum aldı.
Geleceğin Diyabet Bakımı İçin Ne Anlama Gelebilir
Bir uzman olmayan için temel mesaj, bağırsağın fazla kan şekerini kontrollü biçimde dışarı atacak bir kaçış yolu haline getirilebileceğidir. Bağırsak hücreleri içinde belirli bir enzimi — atipik PKC — aktive ederek, araştırmacılar hücreleri daha fazla GLUT1 taşıyıcısını yüzeye taşımaya ve geri döndürülebilir bir boşaltma görevi görmeye yönlendirebildiler; böylece kanı şekerden çekip bir kısmını bağırsak içine boşalttılar. Farelerde bu bağırsak kaynaklı şeker bertarafı, insülini aşırı uyarmadan, iştahı değiştirmeden veya bağırsaklara zarar vermeden kan şekerini düzeltti ve kilo alımını sınırladı. Prostratin ve benzeri bileşikler henüz diyabet ilaçları olarak onaylanmamış olsa da, bu çalışma aPKC–GLUT1 yolunu gastrik bypass cerrahisinin metabolik faydalarının bir kısmını ameliyata gerek kalmadan yeniden oluşturabilecek gelecek ilaç hedefi olarak gösteriyor.
Atıf: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Anahtar kelimeler: bağırsaktan glikoz atılımı, tip 2 diyabet, GLUT1 taşıyıcı, atipik protein kinaz C, prostratin