Clear Sky Science · tr
Ferrik-oksil uyarılmış durumları, heme peroksidaz katalitik ara ürünlerindeki uzamış demir-oksijen bağlarını açıklayabilir mi?
Enzimlerde demir ve oksijen bağlarının önemi
Hücrelerimiz içinde, özel proteinler olan enzimler, güçlü kimyasal tepkimeleri güvenli biçimde yürütmek için oksijeni kullanır. Bunların arasında, heme peroksidazlar, çekirdeklerindeki bir demir–oksijen çifti sayesinde hidrojen peroksidi, reaktif ve potansiyel olarak zararlı bir molekülü parçalamakta rol alır. On yıllardır bilim insanları bu demir–oksijen bağının tam doğası konusunda anlaşmazlık yaşadı: bağ sıkı bir çift bağa mı benziyor yoksa daha gevşek bir tek bağa mı—ve bunun enzimlerin işleyişi için ne anlama geldiği nedir? Bu çalışma, ultrahızlı X-ışını yöntemleri ve gelişmiş hesaplamalar kullanarak bu gizemi ele alıyor ve yanıtın demir–oksijen biriminin kısa süreli uyarılmış durumlarında yattığını ortaya koyuyor.
Bir enzimi gerçek zamanlı izlemek
Araştırmacılar, tipik olarak iki ana yüksek enerjili form arasında dönen, bacterial boya giderici peroksidaz adı verilen bir heme enzime odaklandılar: Bunlar Compound I ve Compound II olarak bilinir. Bu ara formlar her ikisi de demir atomunun oksijene bağlandığı yapıları içerir ve enzimin hidrojen peroksidi işlemesi ile diğer molekülleri okside etmesinde merkezi rol oynar. Benzer enzimler üzerinde yapılan önceki deneyler, bazı bilim insanlarının sözde yüksek reaktiviteye sahip demir–oksijen biriminin ya X-ışınlarıyla değiştirilmiş olduğu ya da fazladan bir proton alarak karakterinin değiştiği yorumunu yaptığı şaşırtıcı derecede uzun demir–oksijen bağ uzunlukları vermişti. Bu tür artefaktları önlemek için ekip, X-ışını serbest-elektron lazerinde zaman çözünürlüklü seri femtosaniye X-ışını kristalografisi kullandı; odacıklarını hasardan daha hızlı olan onlarca femtosaniye içinde binlerce küçük protein kristalinden kırınım ve X-ışını emisyon sinyalleri yakaladılar.
Kristaller içindeki kimyayı izlemek
Düzenekte, enzimin hafifçe değiştirilmiş bir versiyonunun mikrokristalleri, hareketli bir bant üzerinde doğrudan hidrojen peroksitle karıştırıldı ve yarım saniyeden onlarda dakikaya kadar değişen gecikmelerle incelendi. Erken zaman noktaları Compound I oluşumunu desteklerken, daha sonraki zamanlar Compound II tarafından domine edildi. Yapısal veriler, her iki ara üründe de demir atomunun heme cebinde tek bir oksijen atomunun yanında yer aldığını ve proteinin koruyucu döngü bölgelerinin bu yüksek oksitleyici merkezi kapatmak için kaydığını gösterdi. Önemli olarak, hassas ölçümler demir–oksijen bağ uzunluğunun tüm zaman noktalarında yaklaşık 1.83 angström civarında kaldığını gösterdi—klasik bir çift bağlı ferril (Fe(IV)=O) türü için beklenenden daha uzun ve tek bağa daha yakın; buna rağmen X-ışını emisyonu ve optik absorbsiyonun spektral imzaları, Compound I ve II ile tutarlı yüksek oksidasyon durumlarını açıkça işaret ediyordu.
Basit açıklamaları eliyor
Deneyler ultrakısa darbelerle ve oda sıcaklığında gerçekleştirildiği için, bozulmuş bağ uzunluklarının olağan şüphelileri olan X-ışını kaynaklı indirgenme ve kriyojenik artefaktlar büyük ölçüde göz ardı edilebildi. Ekip ayrıca demire bağlanan oksijenin protonlanıp protonlanmadığını, çift bağı hidroksit benzeri tek bağa dönüştürüp dönüştürmediğini test etti. Ancak benzer heme merkezlerinin bilinen asit–baz özellikleri ve önceki kimyasal çalışmalar bu tip enzimlerde böyle bir protonlanmanın lehine güçlü argümanlar sunmuyor. Spektroskopik veriler ayrıca demirin hidrojen peroksit reaksiyonundan sonra yüksek oksidasyon ve düşük spin durumunda kaldığını gösterdi; bu da gerçekten ferril ara ürünlerine uygun sonuçtu ve beklenmedik uzun bağın basit bir kimyasal değişiklikten ziyade daha ince elektronik etkilere bağlı olması gerektiği fikrini güçlendirdi.
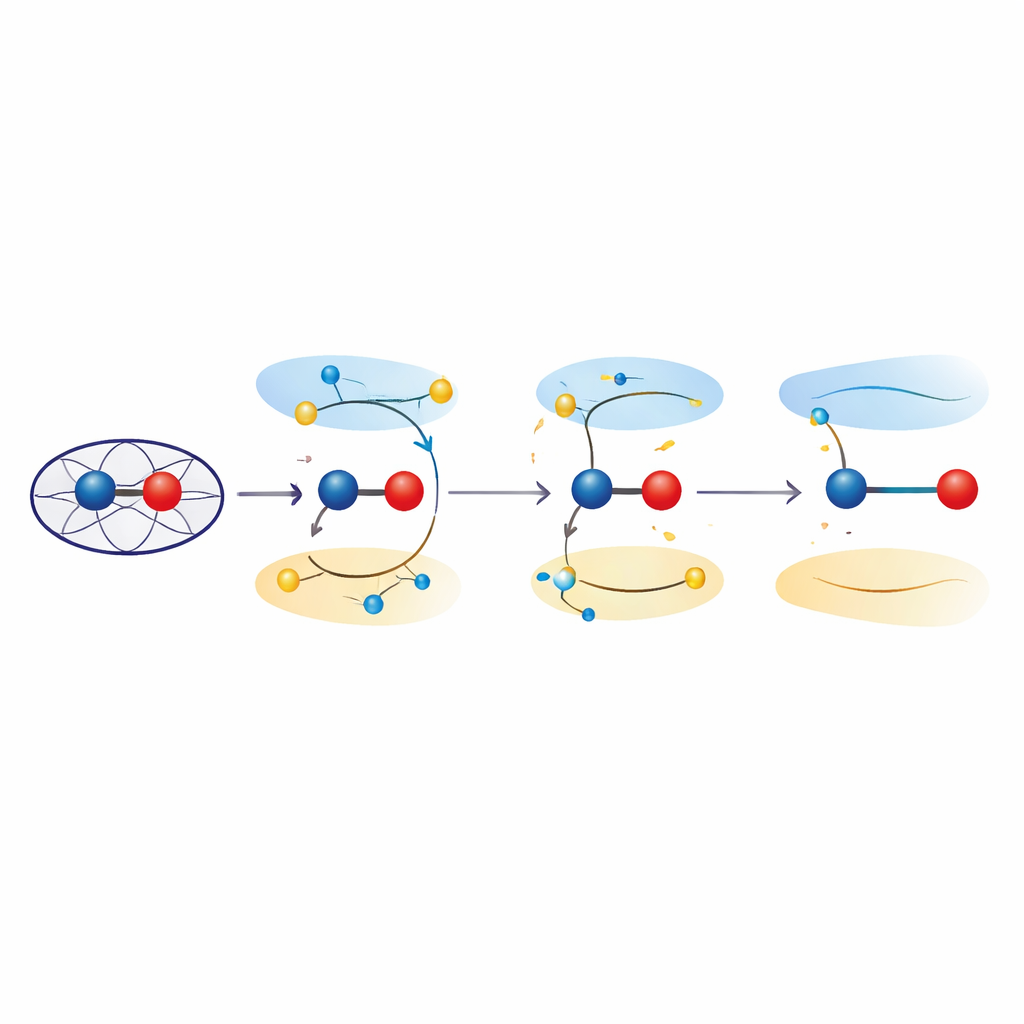
Bağları uzatan uyarılmış durumlar
Bu etkileri araştırmak için araştırmacılar hem basitleştirilmiş modellerde hem de tüm protein ortamında kuantum mekanik hesaplamalara başvurdular. Zaman-bağımlı yoğunluk fonksiyoneli teorisi ve birleşik kuantum mekaniği/moleküler mekaniği yaklaşımları kullanarak, demir–oksijen biriminde bağlayıcı orbitallerden antibaglayıcı orbitallere elektron terfi ettirmenin tercih edilen bağ uzunluğunu nasıl değiştirdiğini incelediler. Bu uyarılmış durumlar, yerel ferril temel durumuna enerjik olarak yakın olup sürekli olarak demir–oksijen mesafelerini 1.8–1.9 angström aralığında ürettiler—kristalografik gözlemlerle örtüştü. Elektron dağılımının analizi, bu durumlarda demir–oksijen çiftinin artık saf bir Fe(IV)=O çift bağı gibi davranmadığını, bunun yerine Fe(III) ile oksijen-merkezli bir radikale benzeyen özellikler taşıyan “ferrik–oksil” karakteri benimsediğini gösterdi. Deneysel yapıların kuantum iyileştirmesi, bu tür uyarılmış durum tanımlamalarının verileri en azından geleneksel temel durum modelleri kadar iyi açıkladığını doğruladı.
Enzimin gücünü anlamak için ne anlama geliyor
Basitçe ifade etmek gerekirse, çalışma bu heme peroksidazlarda gözlenen uzun demir–oksijen bağlarının hasar, indirgenme veya gizli protonlar gibi varsayımları gerektirmediğini öne sürüyor. Bunun yerine, ferril birimin kısa süreli olarak bağı zayıflatan ve ferrik–oksil karakteri kazandıran düşük enerjili uyarılmış durumlara erişmesi doğal olarak bu uzunlukları ortaya çıkarabilir. Konuya hakim olmayanlar için bu, birçok oksijen-aktif enzimde ‘‘işin yürütüldüğü’’ bölgenin, artık düşünüldüğünden daha dinamik ve elektronik açıdan esnek olabileceği; elektron yerleşimindeki ince kaymaların bağ gücünü ve reaktiviteyi, genel kimyayı değiştirmeden etkileyebileceği anlamına geliyor. Bu uyarılmış durumların tanınması, güçlü biyolojik oksidanların yapısal verilerinin yorumlanmasını yeniden şekillendirebilir ve yapay katalizörlerin tasarımında, bu hassas elektronik dengeyi taklit etmeyi veya kasıtlı olarak ayarlamayı yönlendirebilir.
Atıf: Williams, L.J., Kamps, J.J., Brânzanic, A.M.V. et al. Can ferric-oxyl excited states explain elongated iron-oxygen bonds in heme peroxidase catalytic intermediates?. Nat Commun 17, 2324 (2026). https://doi.org/10.1038/s41467-026-69192-8
Anahtar kelimeler: heme peroksidaz, ferril ara ürün, demir-oksijen bağı, uyarılmış elektronik durumlar, X-ışını serbest-elektron lazeri