Clear Sky Science · tr
Vibrio cholerae NADH-kinon oksidoreduktazındaki redoks kaynaklı Na+ pompalama mekanizması dinamik konformasyon değişikliklerine dayanır
Kolera’nın Güç Santrali Nasıl Bir İlaç Hedefi Haline Geldi
Kolera hastalığına neden olan bakteri Vibrio cholerae, hücre zarında küçük bir moleküler güç santrali çalıştırarak hayatta kalır ve çoğalır. Bu çalışma, ana makinelerinden biri olan Na⁺-NQR adlı enzimin, sodyum iyonlarını hücre dışına pompalamak için çalışırken nasıl şekil değiştirdiğini benzeri görülmemiş bir ayrıntıyla ortaya koyuyor. Bu moleküler mekanizmayı anlamak, besini kullanılabilir enerjiye dönüştürme sürecine dair temel merakı gidermekle kalmaz; aynı zamanda insan hücrelerini etkilemeden zararlı bakterileri kapatacak yeni antibiyotikler tasarlamak için de yollar gösterir.
Bakterilerde Sodyumla Çalışan Bir Motor
Birçok deniz ve hastalık yapıcı bakteri, solunum zincirlerinin ilk adımı olarak Na⁺-NQR’ye dayanır; bu zincir, besinlerden enerji çıkaran reaksiyonlar dizisidir. Na⁺-NQR iç zarında yer alır ve yakıt molekülü NADH’den elektron alır; bunları koenzim olarak görev yapan renkli “yardımcı” moleküller zinciri boyunca kinoneye iletir. Elektronlar akarken enzim, bu enerjiyi kullanarak sodyum iyonlarını (Na⁺) hücre içinden dışına doğru iter ve bir sodyum gradiyenti oluşturur. Bu gradiyent şarjlı bir pil gibidir: bakteriyel kamçı motorunu yüzme için güçlendirir, ATP (hücrenin enerji para birimi) üretimine yardımcı olur ve besin alımı ile ilaç atılımını sürer. Na⁺-NQR yalnızca bakterilerde bulunduğundan ve mitokondriyal muadillerinden çok farklı olduğundan, yüksek seçiciliğe sahip antibiyotikler için cazip bir hedeftir.
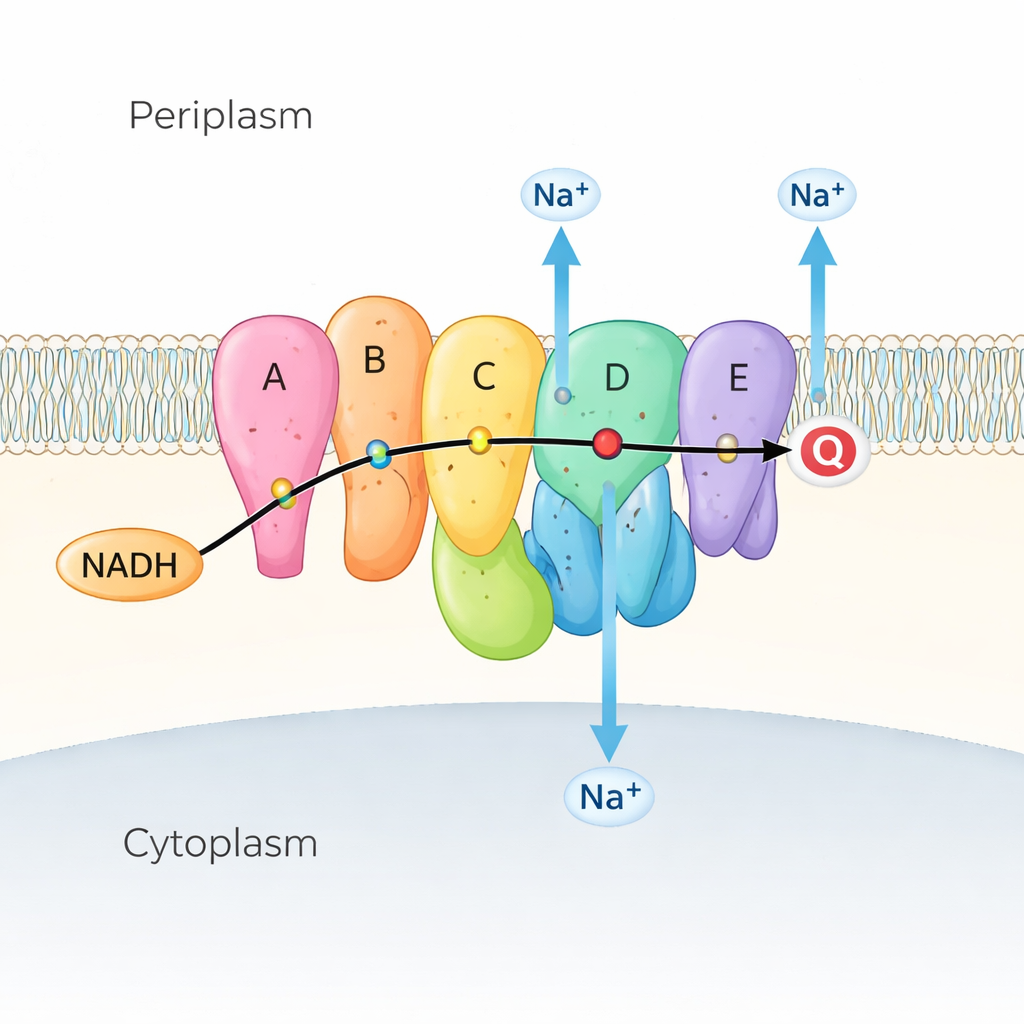
Aygıtın Hareketini İzlemek
Önceki X-ışını ve kryo-elektron mikroskobu görüntüleri Na⁺-NQR’nin alt birimleri ve koenzimlerinin nerede bulunduğunu gösterdi, ancak aynı zamanda bir bilmece de ortaya koydu: bazı kritik elektron atlamaları, protein şekil değiştirmedikçe elektronların verimli şekilde hareket etmesi için çok uzak görünüyordu. Yazarlar bunu, Na⁺-NQR’yi birçok hafif farklı koşulda yakalayarak ele aldılar. Belirli koenzimleri çıkaran mutantlar, reaksiyonu belirli aşamalarda durduran ilaçlar ve sodyum içeren ya da içermeyen çözeltiler kullandılar. Yüksek çözünürlüklü kryo-EM ve gelişmiş görüntü analizleriyle aynı enzimin birden çok konformasyonunu ayırıp yeniden yapılandırabildiler; böylece durağan anlık görüntüleri çalışan döngüsünün bir filmine dönüştürdüler.
Esnek Bir Kol ve Salınan Bir Kıskaç
Ana bulgulardan biri, iki elektron taşıyıcı koenzimi tutan sitoplazmik, esnek bir alt birim olan NqrF ile ilgilidir. Ekip, onun “ferredoksin-benzeri” domaini için “yukarı”, “orta” ve “aşağı” olarak adlandırılan üç konum belirledi. Nadir ama kritik olan “aşağı” durumda, bu küçük domain NqrD ve NqrE tarafından oluşturulan bir cebe doğru sallanarak demir-kükürt kümesini elektron aktarımı için yeterince yakın getirir. Bu arada periplazmik (dış) bir alt birim olan NqrC hareketli bir kıskaç gibi davranır. Bir konformasyonda (“kararlı”), NqrC diğer bir zar alt birimi NqrB’ye yaslanmış şekilde, elektronları son kinon akseptörüne doğru iletmeye konumlanmıştır. İkinci bir konformasyonda (“kaymış”), NqrC NqrD/E’ye doğru hareket ederek flavin koenzimini onların demir-kükürt merkezinden bir elektron alabilecek kadar yaklaştırır. Bu hareketler, NqrF ve NqrC’nin koenzim zincirindeki büyük boşlukları köprüleyen dinamik kuryerler olarak davrandığını gösterir.
Şekil Değişiklikleri Sodyumu Nasıl Pompalıyor
Sodyum pompasının kalbi, zar boyunca geçen helikslerden oluşan merkezi demet oluşturmak için eşleşen NqrD ve NqrE alt birimlerinde yatar. Yapılar ve atom düzeyinde moleküler dinamik simülasyonları kullanarak, yazarlar NqrD/E’deki demir-kükürt kümesi indirgenince (bir elektron kazanınca) negatif yüklü bir bölge oluştuğunu; bunun sitoplazma tarafından bir Na⁺ iyonunu ve birkaç su molekülünü çekerek geçici bir bağlanma cebi oluşturduğunu gösteriyor. Bu cebin üstünde ve altında bulunan hidrofobik amino asitler, iyonun erişimini kontrol eden iç ve dış kapılar gibi davranır. NqrD/E ‘‘içe açık’’ hâlden ‘‘dışa açık’’ şekle geçtiğinde Na⁺ periplazmik tarafa doğru hareket eder ve demir-kükürt kümesi yeniden oksitlenince serbest bırakılır. Simülasyonlar, Na⁺’un kısmen hidratlı kaldığını ancak hiçbir zaman sürekli su dolu bir tünel görmediğini; bunun da enzimin istenmeyen proton sızıntılarına karşı sıkı bir şekilde mühürlendiğini öne sürdüğünü gösterir.
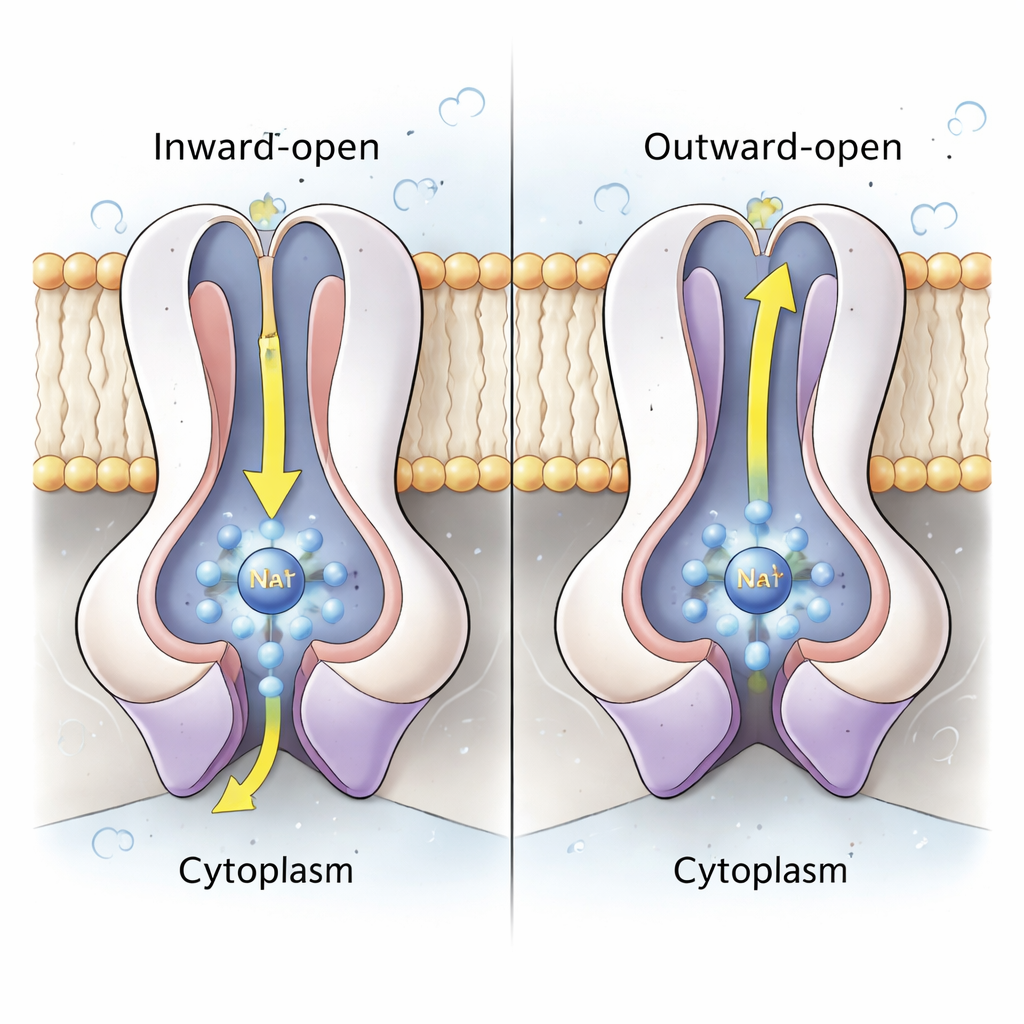
Yönü Kilitleyen Koordine Döngü
Tüm yapısal durumlarını ve simülasyonları birleştirerek araştırmacılar altı adımlı bir döngü öneriyor. İlk olarak NADH bağlanır ve elektronları NqrF’e verir; NqrF sonra bir elektronu NqrD/E’ye aktarır, bu da sitoplazmadan Na⁺ alımını tetikler ve merkezi cebin dolmasını sağlar. NqrD/E’nin dışa-açık formuna geçmesi hem Na⁺’u periplazmaya boşaltır hem de NqrC’nin elektronu almak için konuma gelmesini teşvik eder. Sonraki adımlar elektronları son flavin ve riboflavin koenzimlerine ve nihayetinde iki elektron alması gereken kinoneye aktarır. Önemli olarak, Na⁺’u hareket ettiren aynı şekil değişiklikleri NqrF ve NqrC’yi sırasıyla gevşetip sertleştirerek ileri elektron akışını yalnızca Na⁺ dışarı pompalanırken muhtemel kılar ve geriye kaymayı engeller. Bu bağlanma, enzimin mevcut bir gradiyente karşı Na⁺ pompalamasına yardımcı olarak bakteriyel “pilin” şarjlı kalmasını sağlar.
Bu Çalışmanın Tıp ve Biyoloji İçin Önemi
Uzman olmayan bir okuyucu için bu çalışma, yaşamın proteinlerden oluşan son derece koreografileştirilmiş makineler inşa ettiğini; küçük yük değişimlerinin büyük, yararlı hareketleri tetiklediğini gösterir. Enfeksiyon hastalıkları araştırması açısından ise Na⁺ aktarımının Na⁺-NQR’de esas olarak NqrD/E çekirdeği üzerinden gerçekleştiğini, daha önce şüphelenilen NqrB alt birimi yoluyla olmadığını netleştirir. Bu bulgu, Vibrio cholerae ve diğer patojenleri güçlendiren motoru en iyi şekilde bozmak için gelecekte ilaçların nerelere bağlanması gerektiğini daraltır ve insan enzimlerini korur. Daha geniş anlamda çalışma, redoks reaksiyonlarının iyon pompalamaya nasıl bağlanabileceğine dair yapısal bir plan sunar—doğa bu tasarım ilkesini birçok farklı biyoenerjetik makinede tekrar kullanır.
Atıf: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Anahtar kelimeler: sodyum pompası, bakteriyel solunum, Na+-NQR, kryo-EM, antibiyotik hedefleri