Clear Sky Science · tr
Tip III‑E CRISPR nükleaz‑proteazına dayanan RNA’ya duyarlı bir piroptozis sentetik sistemi
Öldürücü Hücre Patlamalarını Hedefe Yönelik Araçlara Çevirmek
Vücudumuz bazen enfekte veya hasarlı hücreleri enflamatuvar bir tür öz‑yıkım olan patlama yoluyla ortadan kaldırarak kendini savunur. Bu patlama yalnızca tehlikeli hücreleri uzaklaştırmakla kalmaz, aynı zamanda bağışıklık sistemini de çağırır. Yeni çalışma, bir hücrenin içindeki RNA mesajlarını okuyup o hücrenin yok edilip edilmeyeceğine karar verebilen DAMAGE adlı sentetik bir gen devresini tanıtıyor. Mikrobiyal bir savunma sistemini bizim hücre‑ölümü mekanizmamıza bağlayarak araştırmacılar, sağlıklı komşulara zarar vermeden virüsle enfekte olmuş, kanserli veya yaşlanmış hücreleri seçici biçimde yok etmenin bir yolunu gösteriyor. 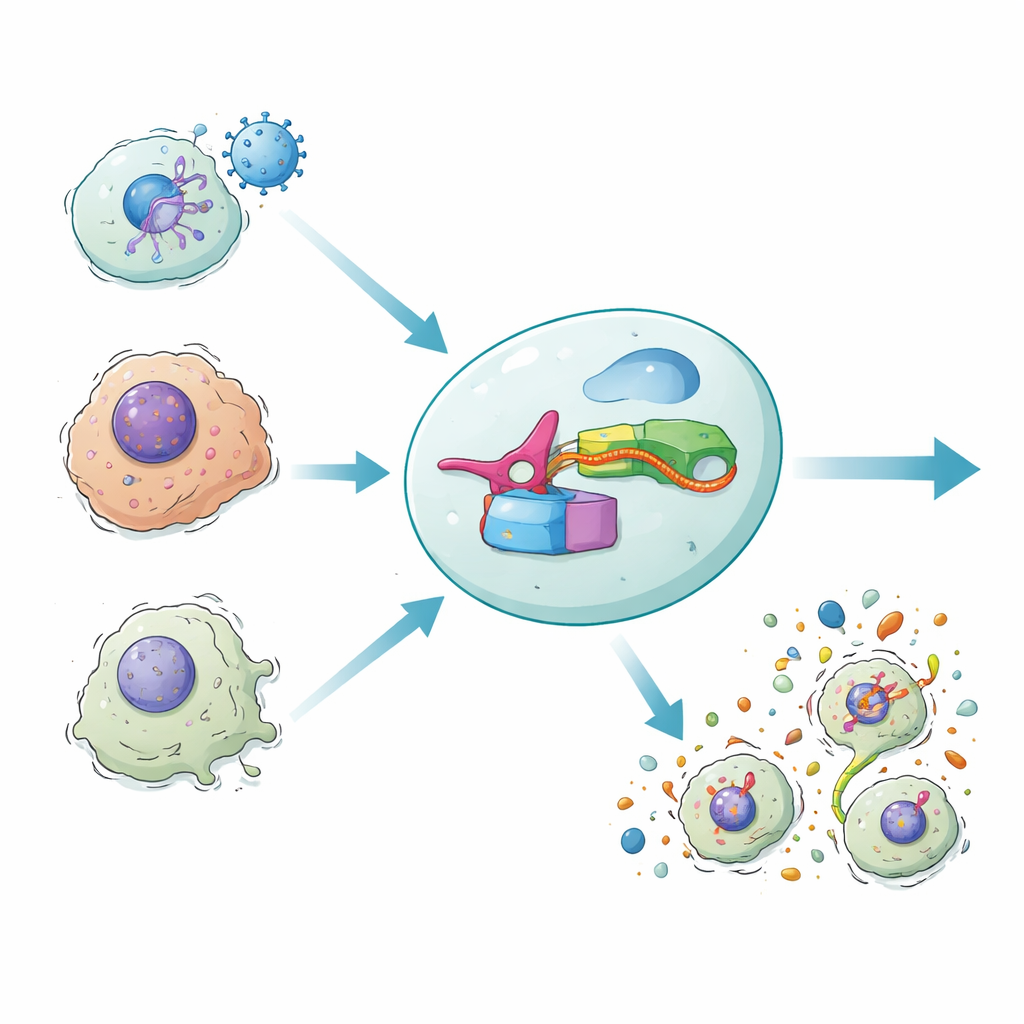
Hücreler Normalde Nasıl Kendini Patlatır
Enflamatuvar hücre ölümünde, gazderminler olarak bilinen bir protein ailesi hücrelerin içinde yüklü birer düzenek gibi durur. Her gazderminin hücre zarında delik açabilen “katil” ön yarısı ve katili kontrol altında tutan bir “emniyet kapağı” arka yarısı vardır. Bağışıklık sensörleri tehlikeyi algıladığında enzimler gazderminleri ikiye keser ve ön yarıyı dış zarda gözenekler oluşturmak üzere serbest bırakır. Hücre şişer, parçalanır ve bağışıklık hücrelerini toplayan alarm sinyalleri salar. Bu güçlü tepki enfeksiyonlara ve tümörlere karşı savaşmaya yardımcı olur, ancak doğal kontrol ağı karışıktır ve tedavi için yeniden düzenlemesi zordur.
RNA Okumak İçin Bakteriyel Savunmaları Ödünç Almak
Bakteriler CRISPR teknolojisiyle bilinen kompakt savunma modülleri geliştirmiştir. Bu sistemlerden biri olan tip III‑E, kısa bir kılavuz RNA yardımıyla belirli RNA dizilerine bağlanabilen Cas7‑11 adlı bir protein kullanır. Cas7‑11 uyumlu bir hedef RNA bulduğunda, eşlik eden bir enzim olan Csx29’u açar; Csx29 da ortak bir protein olan Csx30’u keser. Yazarlar Csx30’un herhangi iki protein parçası arasında özelleştirilebilir bir “menteşe” görevi görebileceğini fark ettiler. Bu menteşeyi insan gazderminlerinin katil ve emniyet kapağı yarıları arasına birleştirerek, CRISPR‑benzeri sensör seçtikleri RNA’yı bir hücre içinde algıladığında yalnızca ayrılan yapay yürütücüler oluşturdular.
Hastalıklı Hücreler İçin Programlanabilir Bir Ölüm Anahtarı
DAMAGE (Death Manipulation Gene) adını taşıyan bu tasarım beş parçadan oluşur: Cas7‑11 sensörü, Csx29 kesici, gazdermin–Csx30 füzyonu, bir kılavuz RNA ve hücre içindeki hedef RNA. Doğru RNA mesajı ortaya çıktığında Cas7‑11 ona bağlanır, Csx29’u etkinleştirir ve Csx29 füzyon protekteki Csx30 menteşesini keser. Gazderminin katil yarısı serbest kalır, zarında gözenekler açar ve hücre enflamatuvar bir patlama ile ölür. Kılavuz RNA’yı değiştirerek ekip DAMAGE’ı farklı hücresel hedeflere yönlendirdi. Respiratuvar sinsityal virüsünden, servikal kanser hücrelerindeki yüksek riskli insan papilloma virüsünden ve normal RNA’dan yalnızca tek bir harfle farklı birkaç kanser tetikleyici KRAS mutasyonundan gelen RNA’ları tanıyabildiğini gösterdiler. Her durumda, şüpheli RNA taşıyan hücreler seçici olarak yok edilirken, yakınlardaki kontrol hücreleri sağlam kaldı. 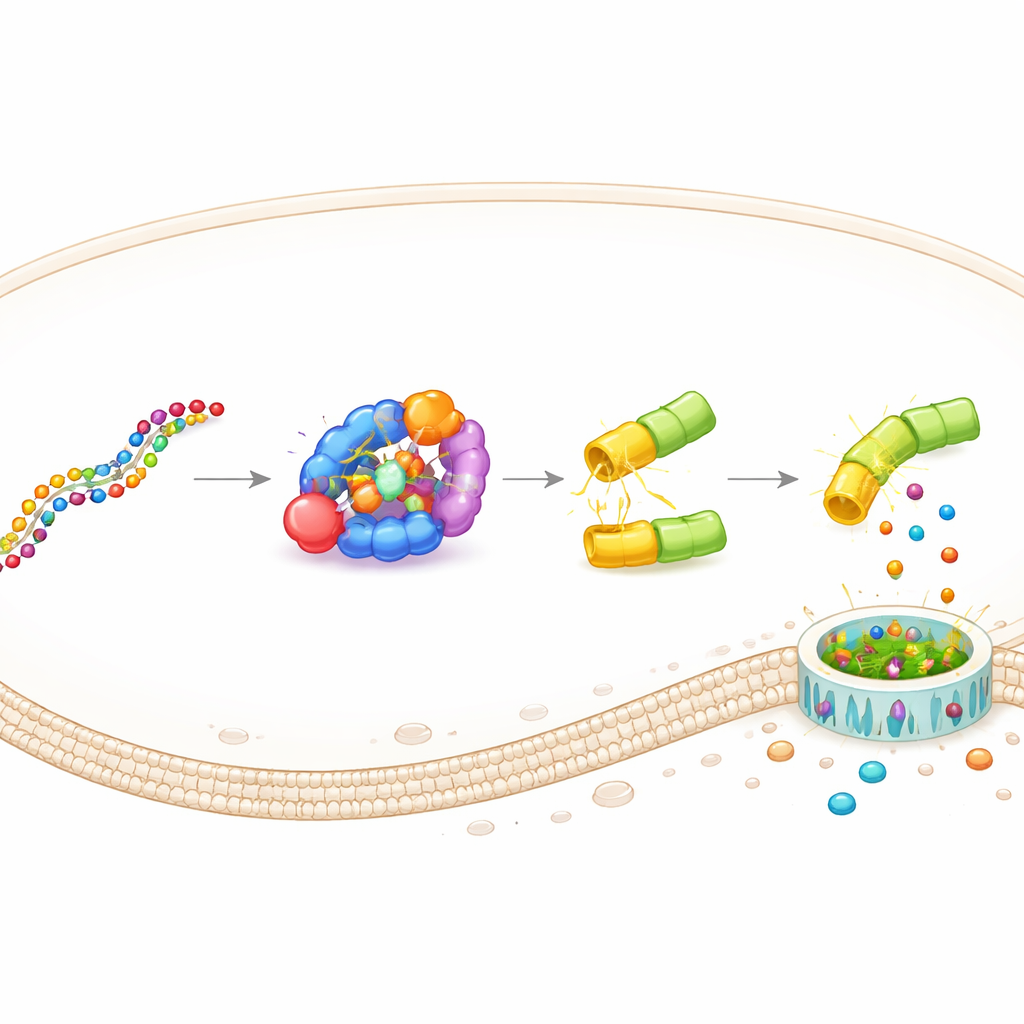
Yaşlanan Hücrelere Doğru Hedefleme
Araştırmacılar ayrıca DAMAGE’ın bölünmeyi bırakan, dokularda biriken ve kırılganlık ile kronik hastalıklara katkıda bulunan yaşlı veya stresli hücreler olan senescent hücreleri avlayıp avlayamayacağını sordular. Bu tür hücreler genellikle iki kapı bekçisi proteini olan p16 ve p21’in üretimini artırır. p16 ve p21 için RNA’lara karşı kılavuzlar programlayarak ekip DAMAGE‑Aging adında bir versiyon oluşturdu. Bu devre, bu mesajların yüksek düzeyde olduğu hücreleri öldürürken p16’nın genetik olarak çıkarıldığı hücreleri koruyarak sistemin sabit DNA değişiklikleri yerine gerçek zamanlı RNA bolluğunu okuduğunu doğruladı. p16 veya p21 seviyelerini artıran ilaç tedavileri hücreleri bu hedefe yönelik öz‑yıkıma karşı daha hassas hale getirdi.
Gelecekteki Terapiler İçin Sistemi Paketlemek
Pratik kullanıma yaklaşmak için yazarlar DAMAGE’ın çok sayıda DNA parçasını DAMAGE‑Plus adında daha derli toplu bir yapıya sıkıştırdılar ve bunun hâlâ güvenilir şekilde çalıştığını gösterdiler. Ardından bu yapıyı sentetik mRNA’ya çevirip COVID‑19 aşılarında kullanılanlara benzer lipit nanopartiküller içinde paketleyip kültürdeki hücrelere teslim ettiler. mRNA versiyonu devreyi başarıyla birleştirdi ve viral veya kanserle ilişkili RNA taşıyan hücrelerde hedefe yönelik enflamatuvar ölümü tetikledi. Genel sistem hâlâ hacimli ve yalnızca hücre hatlarında test edilmiş olsa da, bu sonuçlar programlanabilir, RNA‑yönlendirmeli hücre öldürmenin bir gün enjeksiyonla verilen mRNA formülasyonları aracılığıyla uygulanabileceğini düşündürüyor.
Hücresel Mesajları Okumanın ve Tepki Vermenin Yeni Bir Yolu
Basitçe söylemek gerekirse DAMAGE, her hücrenin içsel RNA “kimliğini” kontrol eden ve yalnızca tehlikeli görünenleri—enfekte, mutasyon taşıyan veya senescent—patlayıcı bir öz‑yıkıma zorlayarak dışarı atan moleküler bir kapıcıdır. Çalışma, bakteriyel RNA sensörlerinin insan hücre‑ölümü mekanizmasına yüksek hassasiyetle bağlanabileceğini ve genetik mesajlardaki tek harf farklılıklarını bile ayırt edebileceğini gösteriyor. Bu tür bir sistemin hayvanlarda veya insanlarda güvenle kullanılabilmesi için daha çok mühendislik gerektiği halde, hücrelerin içindeki canlı RNA sohbetini okuyup doğrudan yaşam veya ölüm kararlarına çevirme konusunda güçlü yeni bir strateji ortaya koyuyor.
Atıf: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Anahtar kelimeler: piroptozis, CRISPR, RNA hedefli tedavi, kanser immünoterapisi, hücresel yaşlanma