Clear Sky Science · tr
hnRNPM, oosit gelişimi sırasında alternatif eklemeyi düzenlemek için BCAS2 ile işbirliği yapıyor
Yumurta hücresi kalitesinin önemi
Her insan yaşamı tek bir yumurta hücresiyle başlar, ancak bilim insanları bu alışılmadık büyük hücrelerin döllenme anına nasıl hazırlandığını hâlâ çözüyor. Sperm daha gelmeden çok uzun süre önce, büyüyen oositler olgunlaşmalarını ve embriyonun ilk günlerini yönlendirecek binlerce RNA mesajı depolar. Bu çalışma, az tanınan bir proteinin bir ortakla birlikte, fare yumurtalarında bu mesajları nasıl dikkatle düzelttiğini ve bu düzenleme sistemi başarısız olduğunda neler olduğunu ortaya koyuyor.
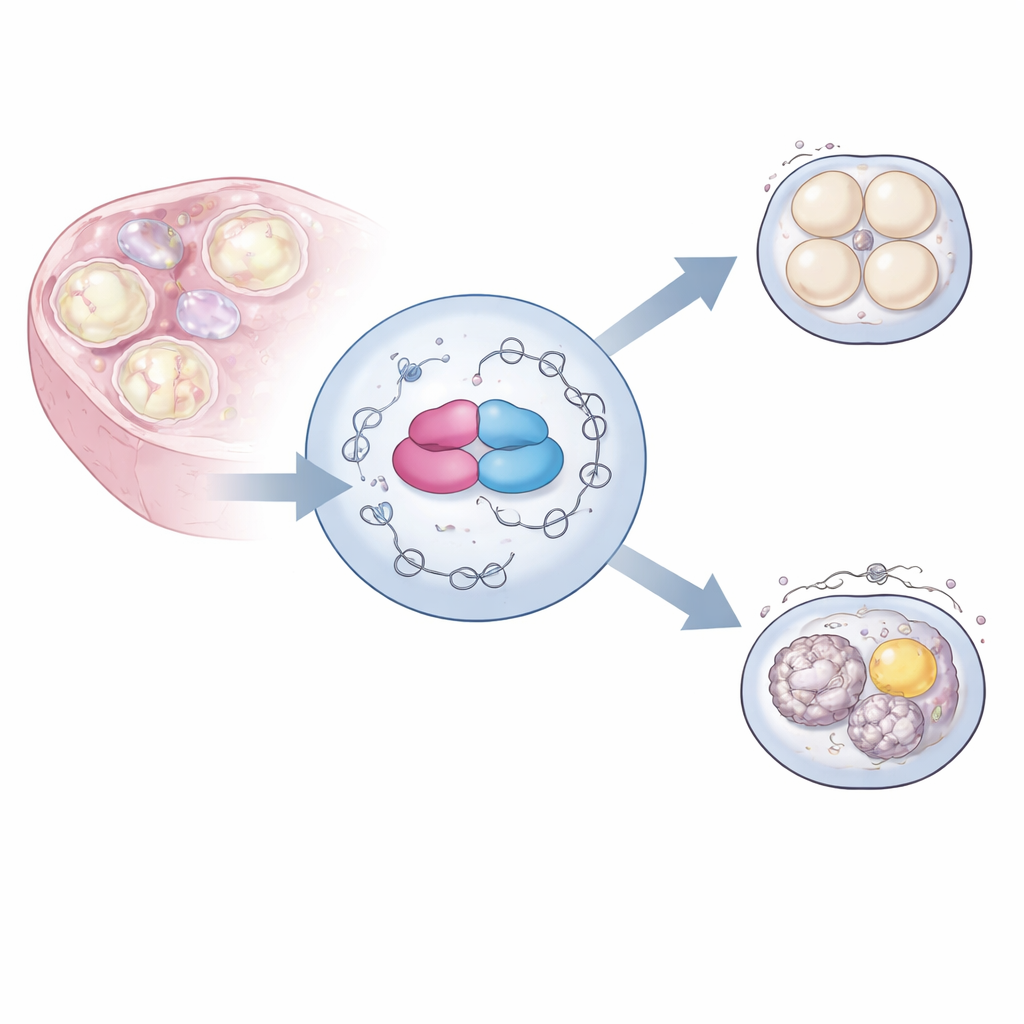
Genetik mesajların bekçileri
Yumurta hücreleri, DNA’ları büyük ölçüde sessiz kalırken haftalarca yumurtalıkta büyür. Bu süre zarfında, daha önce genomdan kopyalanmış geniş bir maternal RNA kütüphanesi biriktirirler. Bu mesajlar, alternatif ekleme olarak adlandırılan bir süreçte farklı biçimlerde kesilip birleştirilerek, doğru aşamalarda doğru protein varyantlarının üretilmesi sağlanmalıdır. Yazarlar, RNA’ya bağlanan geniş bir ailenin üyesi olan hnRNPM adlı proteine ve diğeri BCAS2 olan ortağına odaklandı; her ikisi de kadın üreme sisteminde bol bulunur. Önceki çalışmalar bu proteinlerin oositlerde birçok RNA’ya bağlandığını ima etmişti, ancak verimliliği şekillendirmedeki kesin rolleri belirsizliğini koruyordu.
Bu düzenleyici yoksa neler ters gider
hnRNPM’in işlevini araştırmak için ekip, genetik mühendislik kullanarak Hnrnpm genini özel olarak fare oosit öncüllerinden çıkardı. Bu dişilerin yumurtalıkları normal görünüyordu ve denetim gruplarıyla karşılaştırılabilir sayıda yumurta üretiyordu. Ancak bu yumurtalar laboratuvarda döllendiğinde, neredeyse hiç ilk bölünmelerin ötesine geçemedi ve dişileri tamamen kısır bıraktı. Olgunlaşmamış yumurtaların daha yakından incelenmesi, normalde berrak olan sitoplazmada koyu yumakların olduğunu ortaya çıkardı. Elektron mikroskobu, sitoplazmik örgü adı verilen ince iç iskeletin büyük ölçüde eksik olduğunu ve mitokondri ile yağ damlacıkları gibi önemli organellerin eşit dağılmak yerine anormal şekilde kümelendiğini gösterdi. Bu değişiklikler, yolunun iç organizasyonunda derin bir sorun olduğunu işaret ediyordu.
Bozulmuş hücre bölünmesi mekanizması
Aynı mutant yumurtalar mayozu tamamlamakta da zorlandı; kromozom sayısını yarıya indiren özel hücre bölünmesi. Araştırmacılar yumurtaları kültürde olgunlaştırdıklarında mayoza başlayabildiler ancak genellikle tamamlamadan durakladılar. Mikroskop altında kromozomları ayıran yapıların—iğlerin—bükülmüş, çok kutuplu veya zayıf sabitlenmiş olduğu görüldü. İğ kutuplarını organize etmeye yardımcı olan pericentrin adlı protein geç ve yanlış yerlerde ortaya çıkıyordu. Bu kusurların tümü, yumurtaların kromozomları güvenilir şekilde hizalayıp ayıramamasına yol açtı; bu durum döllenme sonrası tam gelişim başarısızlığının muhtemel bir nedeniydi.
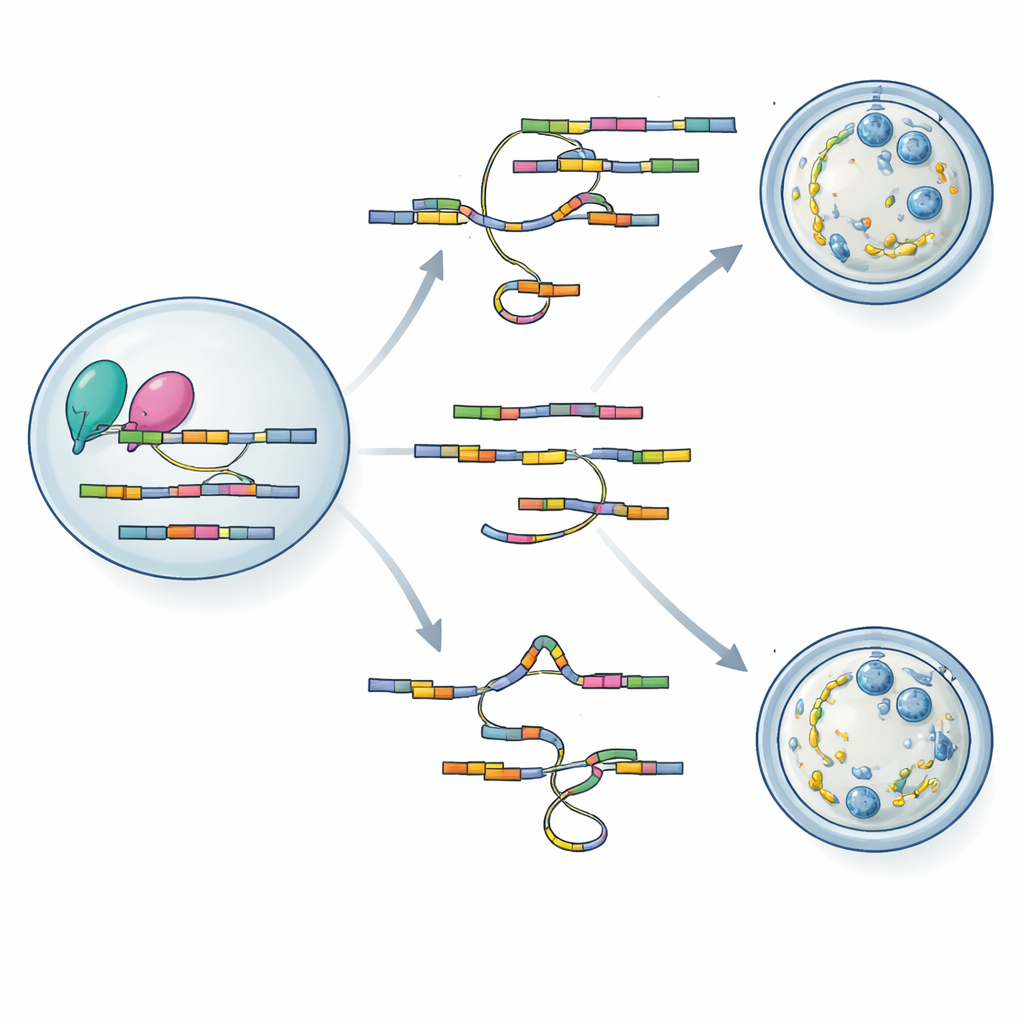
RNA talimatlarını okumak ve yeniden yazmak
hnRNPM kaybının bu kadar geniş kusurlara nasıl yol açtığını anlamak için ekip, küçük oosit örnekleri için uyarlanmış iki güçlü dizileme aracına yöneldi. Tekli oositlerden tam uzunluklu RNA moleküllerini okuyan SCAN-seq kullanıldığında, mutant yumurtalarda birçok daha önce bilinmeyen RNA varyantı da dahil olmak üzere binin üzerinde ekleme değişikliği keşfettiler. Sitoplazmik örgünün inşası, iğ davranışının kontrolü ve mayotik hücre döngüsünün düzenlenmesinde görevli genler özellikle etkilendi. İkinci yöntem olan LACE-seq, hnRNPM’in RNA’ların üzerinde tam olarak nerelere bağlandığını haritalandırdı ve ekzon içindeki GU-zengin dizilimlere bir eğilim ortaya koydu. İki veri kümesini üst üste koyarak, yazarlar hnRNPM’in proteinin eksik olduğu durumlarda eklemesi değişen birçok mesajın üzerinde doğrudan durduğunu gösterdi; bu da bağlanma aktivitesini ekleme doğruluğuna bağladı.
Oosit kontrolü için bir ekip çalışması modeli
Protein etkileşim çalışmaları, hnRNPM’in BCAS2 ve ekleme mekanizmasının çekirdek bileşenleriyle fiziksel olarak ilişkili olduğunu gösterdi. Bu iki ortak birçok ortak RNA hedefine bağlanır ve ya proteinden biri bozulduğunda genellikle aynı şekilde değiştirir. İlginç bir şekilde hnRNPM kaybı BCAS2 protein düzeylerini azalttı ve paylaşılan RNA hedefleri üzerindeki BCAS2’nin tutunmasını zayıflattı; bu, hnRNPM’in yalnızca mesajları düzenlemekle kalmayıp aynı zamanda ortağını bu mesajlar üzerinde stabilize etmeye de yardımcı olduğunu düşündürür. Yazarlar, hnRNPM ve BCAS2’nin oosit büyümesi sırasında kritik maternal RNA’ları biçimlendiren işbirlikçi bir kompleks oluşturduğu; böylece sitoplazmik örgünün doğru bir şekilde toplanmasını ve mayotik bölünmenin güvenilir olmasını sağladığı modelini öne sürüyorlar.
Bu bulguların doğurganlık için anlamı
Düz anlatımla, bu çalışma moleküler bir düzenleme ekibi—hnRNPM ve BCAS2’nin—döllenme sonrası yaşam için oositleri sahne arkasında hazırladığını gösteriyor. Bu ekip yoksa, yumurtanın iç iskeleti çöker, kromozom ayırma makinesi yanlış çalışır ve yumurta normal sayılarda üretilse bile embriyo gelişimini destekleyemez. hnRNPM farelerde ve insanlarda yüksek benzerlik gösterdiğinden, bu bulgular açıklanamayan bazı kadın kısırlığı biçimlerine temel teşkil eden korunmuş bir kalite kontrol sistemine işaret ediyor ve tanı veya tedavi için yeni giriş noktaları sunuyor.
Atıf: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Anahtar kelimeler: oosit gelişimi, alternatif ekleme, kadın kısırlığı, RNA-bağlayıcı proteinler, sitooplazmik örgü