Clear Sky Science · tr
Metabolik rekabet ve virülans susturulması yoluyla Enterohemorajik Escherichia coli'yi baskılayan tasarlanmış bakteri tedavisi
Canlı İlaç Olarak Dost Bakteriler
Bazı Escherichia coli suşlarının yol açtığı gıda zehirlenmeleri sadece mide rahatsızlığıyla kalmayabilir. Enterohemorajik E. coli (EHEC) adı verilen bazı türler, özellikle çocuklarda böbrek yetmezliğine yol açabilecek güçlü toksinler salgılar ve standart antibiyotikler durumu daha da kötüleştirebilir. Bu çalışma farklı bir tedavi yolunu araştırıyor: akıllı mikrokapsüller içinde paketlenmiş, insan anne sütünde bulunan bir şeker ile mühendislik uygulanmış bir probiyotiği kullanarak tehlikeli bakterileri besin rekabetiyle geride bırakmak ve zararlı davranışlarını susturmak; tüm bağırsak ekosistemini bozmayacak şekilde.
Neden Bazı E. coli Türleri Bu Kadar Tehlikeli?
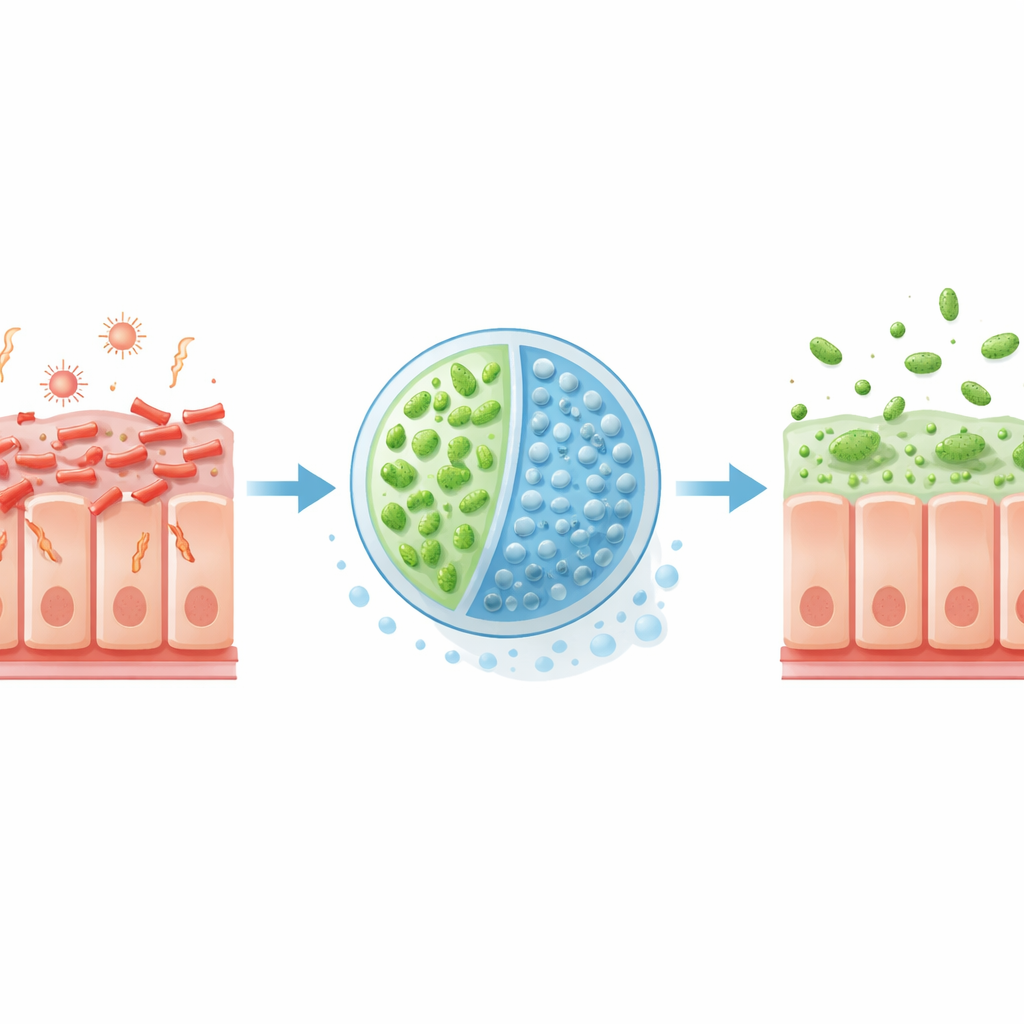
EHEC, genellikle az pişmiş et veya kontamine sebze-meyveden kaynaklanan bir gıda kaynaklı patojendir. Bağırsak içine girdikten sonra bağırsak hücrelerine sıkıca tutunur ve hücre yüzeyini yeniden şekillendiren proteinler enjekte ederek bakterilerin tutunmasını ve yayılmasını kolaylaştıran çıkıntılar oluşturur. Aynı zamanda EHEC, Shiga toksinleri üreterek bunların kana karışmasına ve kan damarlarına zarar vermesine neden olur; bu durum bazen hayatı tehdit eden hemolitik üremik sendroma yol açabilir. Birçok antibiyotik bu bakteriler üzerinde strese yol açıp daha fazla toksin salımını tetiklediği için doktorların destekleyici bakım dışında güvenli seçenekleri sınırlıdır; bu da hedefe yönelik yeni yaklaşımları çok arzu edilir kılar.
Bir Probiyotiği EHEC'yi Açlığa ve Silahsızlandırmaya Programlamak
Araştırmacılar uzun süredir kullanılan probiyotik suş Escherichia coli Nissle 1917'ye yöneldi ve onu EcN3 adlı terapötik bir mikrop haline getirmek için yeniden düzenledi. EcN3'e, EHEC'nin kalın bağırsakta tercih ettiği besin kaynağı olan glukuronik asidi daha verimli parçalamasını sağlayan ek genler eklendi. Ayrıca EcN3'e, anne sütü şekeri 2′-fukozillaktozu laktoz ve fukoza bölen bir enzim verildi. Laktaz yerine içsel bir "anahtar" gibi davranan laktöz, EcN3'te geliştirilmiş besin kullanım sistemini açarak glukuronik asidi emmesini ve EHEC'yi bu yakıttan mahrum bırakmasını sağlıyor. Öte yandan fukoz, EHEC'ye anahtar virülans genlerini azaltması gerektiğini bildiren bir sinyal görevi görerek onun sıkı tutunma ve hasar verme yeteneğini düşürüyor.
Terapinin Doğru Yerde Salınmasını Sağlayan Akıllı Kapsüller
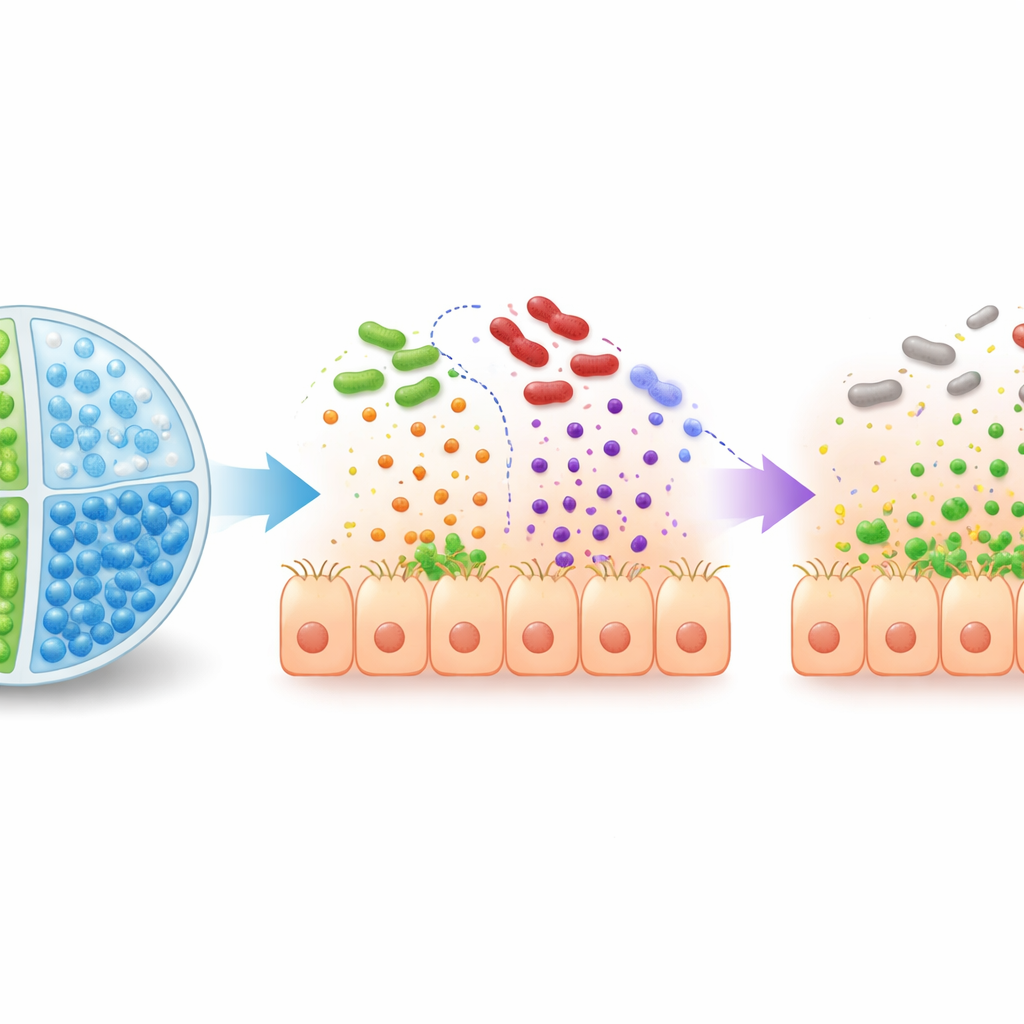
Mühendislik uygulanmış bakterileri ve şekeri doğrudan beslemek yeterli değil: mide asidi probiyotiği öldürebilir ve diğer mikroplar şekeri kolona ulaşmadan önce tüketebilir. Bunu çözmek için ekip, iki ayrı iç bölmesi olan alginat jelden yapılmış çok bölmeli mikroküreler—minik boncuklar— geliştirdi. Bir bölme EcN3'ü, diğeri 2′-fukozillaktozu taşıyarak bunları bağırsaklarda hedeflenen yere ulaşana kadar ayrı tuttu. Bu mikrokapsüller simüle edilmiş mide sıvısında parçalanmaya direnç gösterir, ancak kolon benzeri koşullarda çözünerek hem mühendislik uygulanmış bakteriyi hem de şekeri tam ihtiyaç duyulan yerde serbest bırakır. Farelerde kapsüllenmiş sistem, aynı bileşenlerin kapsülsüz verilmesine kıyasla EcN3 hayatta kalmasını ve mühendislik genlerinin daha güçlü aktivasyonunu sağladı.
Hayvan Modellerinde Koruyuculuğun Test Edilmesi
Ekip stratejisini EHEC ile enfekte edilmiş infant tavşanlar ve insan hastalığının birçok yönünü taklit eden yakından ilişkili bir patojen olan Citrobacter rodentium ile enfekte edilmiş farelerde test etti. Enfeksiyon sonrasında EcN3 artı 2′-fukozillaktoz ile tedavi edilen hayvanlarda bağırsakta daha az patojen, bakterilerin tutunma genlerinin daha düşük ekspresyonu ve bağırsak dokusunda daha az hasar görüldü—bunların hepsi Shiga toksini üretiminde artış olmadan ortaya çıktı. Önleyici amaçla, serbest (kapsülsüz) kombinasyon zayıf çalıştı çünkü şeker mevcut mikrobiyota tarafından hızla tüketildi. Buna karşılık, EcN3 ve 2′-fukozillaktoz çift bölmeli mikrokürelerde birlikte verildiğinde hem tavşanlarda hem de farelerde patojen kolonizasyonu belirgin şekilde azaldı, hastalık daha hafif geçti ve hayatta kalma oranları iyileşti.
İyi Mikropların ve Bağırsak Bariyerinin İyileşmesine Yardımcı Olmak
Bağırsak bakterilerini DNA dizilemesi ile profilleyen bilim insanları, enfeksiyonun normal mikrobiyal dengeyi bozduğunu, zararlı Citrobacter'ı artırıp faydalı grupları zayıflattığını buldu. Mühendislik uygulanmış mikrokapsüllerle tedavi sadece patojen seviyelerini azaltmakla kalmadı, aynı zamanda topluluğu daha sağlıklı bir duruma geri döndürdü; özellikle bağırsak sağlığını desteklediği bilinen Lactobacillus türlerinde artış gözlendi. Bağırsak bariyer fonksiyonuna ilişkin ölçümler de benzer bir tablo verdi: kapsüllenmiş terapisi alan hayvanlarda mukusla ilişkili ve sıkı bağlantı genlerinin seviyeleri daha yüksekti, koruyucu mukus tabakaları daha kalındı ve bağırsaktan kana florasan işaretleyicinin sızıntısı daha azdı; bu da daha sıkı, daha az iltihaplı bağırsak duvarlarını gösteriyordu.
Antibiyotik İçermeyen Geleceğin Enfeksiyon Bakımına Bir Bakış
Genel olarak bu çalışma, tedavisi zor bir gıda kaynaklı enfeksiyona karşı iki yönlü, hedefe yönelik bir strateji gösteriyor. Besin için rekabet eden ve zararsız bir şeker sinyalini algılayan mühendislikli bir probiyotik ile her iki bileşeni de kolona taşıyan mikrokapsülleri birleştirerek tedavi EHEC'yi zayıflatıyor, sayısını azaltıyor ve bağırsakları geleneksel antibiyotiklere bağımlı kalmadan koruyor. Daha fazla güvenlik ve klinik çalışma gerekse de bu yaklaşım, canlı ilaçlar ve akıllı malzemelerin bir gün şiddetli bağırsak enfeksiyonlarını hassas, mikrobiyom-dostu yollarla yönetmek ve geleneksel ilaçlara bağımlılığı azaltmak için kullanılabileceğini gösteriyor.
Atıf: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
Anahtar kelimeler: tasarlanmış probiyotikler, bağırsak enfeksiyon tedavisi, EHEC, mikrobiyom, ilaç salımlı mikroküreler