Clear Sky Science · tr
Triterpenoid antifungal ilaçların mantar β−1,3-glukan sentazlarını engelleme mekanizması
Mantar enfeksiyonlarını durdurmanın önemi
Mantar enfeksiyonları her yıl sessizce bir milyondan fazla kişinin ölümüne yol açıyor ve tarım ürünleri ile ekosistemleri küresel ölçekte tehdit ediyor. Hekimler zaten sınırlı sayıda antifungal ilaca mahkûm ve bazı tehlikeli mantarlar bunlardan kaçınacak şekilde evrimleşiyor. Bu çalışma, yeni bir antifungal ilaç sınıfının mantarların koruyucu hücre duvarını oluşturmak için ihtiyaç duyduğu anahtar enzime nasıl tutunup onu işlevsiz hale getirdiğini moleküler ayrıntıda ortaya koyuyor. Bu sürecin anlaşılması, dirençli mantarları alt edebilecek daha iyi tedavilerin tasarımı için bir yol haritası sunuyor.
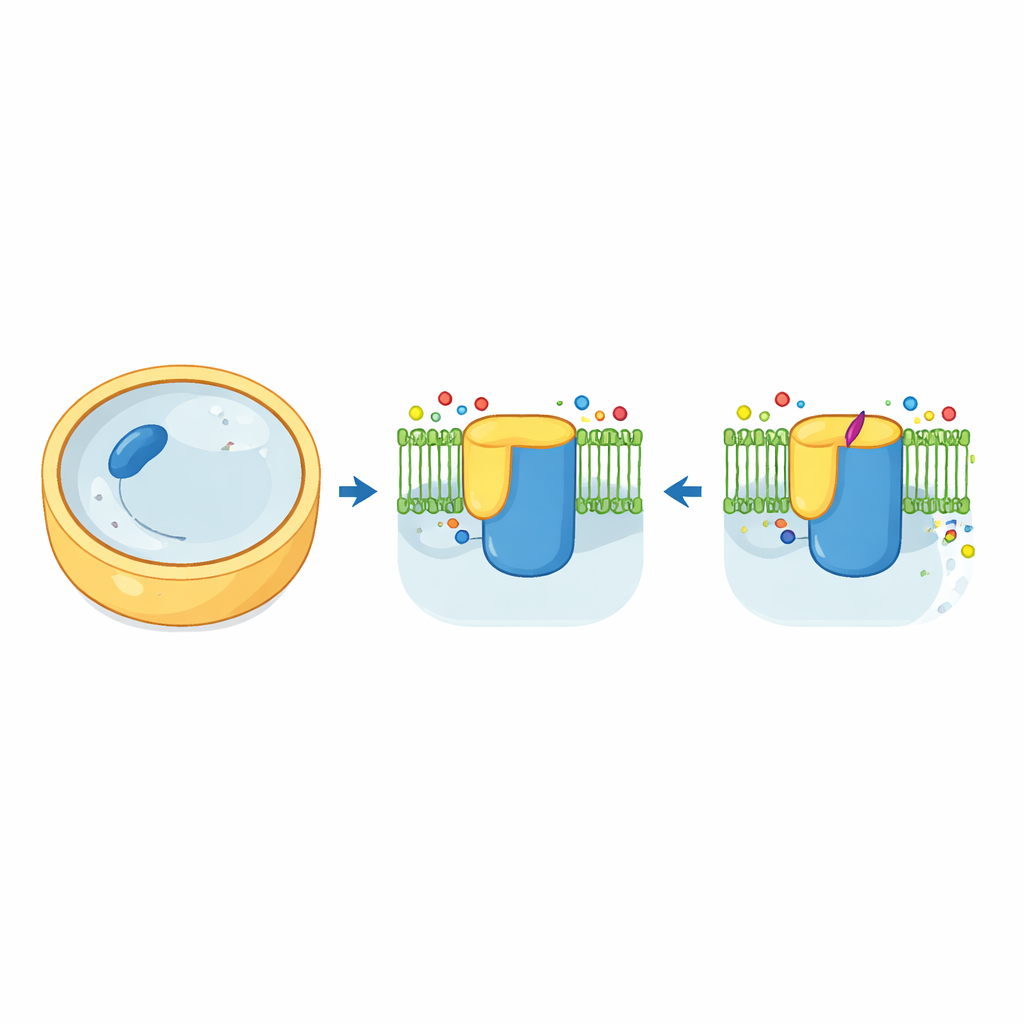
Mantar hücre duvarının tuğla üreticisi
Mantar hücreleri büyük ölçüde beta-1,3-glukan adı verilen şeker bazlı bir polimerden oluşan dayanıklı bir duvarla çevrilidir. Bu polimeri üreten ve hücre dışına aktarılmasını sağlayan enzim, beta-1,3-glukan sentaz, adeta bir tuğla üreticisi ve konveyör bantın birleşimi gibidir. Mayada bu makine, hücre zarına gömülü ve küçük bir yardımcı protein olan Rho1 ile kontrol edilen Fks1 ve Fks2 adındaki iki çok benzer versiyondan oluşur. Yazarlar kriyo-elektron mikroskopi kullanarak hem Fks1 hem de Fks2’nin doğal formlarına yüksek çözünürlüklü üç boyutlu görüntüler yakaladılar. Yapılar, büyük bir sitozolik “çalışma tezgâhı”nın zar boyunca uzanan bir dizi heliks ormanına bağlı olduğunu ve büyüyen glukan zincirinin hücre dışına çıktığı tünel olarak hizmet etmesi muhtemel merkezi bir boşluk içerdiğini ortaya koyuyor.
Doğal bir ürün ilacın enzimi nasıl yakaladığı
Oral ilaç ibrexafungerp de dahil klinik açıdan önemli triterpenoidlerin kökeni enfumafungin adlı doğal bir bileşiğe dayanır. Bugüne dek bu ilaçların glukan sentazın neresine bağlandığı tam olarak bilinmiyordu. Araştırmacılar, hem Fks1 hem de Fks2’nin enfumafungin ile bağlı yapısını çözdü. Şaşırtıcı biçimde ilaç, şeker birimlerinin birleştirildiği aktif bölgeye girmiyor. Bunun yerine, tek bir zar heliksi olan TM5’in dış bölümünde, katalitik merkezden yaklaşık üç nanometre uzakta ve muhtemel glukan çıkış kanalına yakın bir yerde zar içinde yuvalanıyor. Bu yamadaki anahtar amino asitler ilacın hidrofobik çekirdeğini kavrarken asidik kuyruğuyla temas kuruyor; ilacın şeker yan zinciri ise proteine zar zor değiyor—bu da kimyagerlerin o kısmı değiştirebilip etkinliği kaybetmemelerini açıklıyor.
Hareket halindeki makineyi donduran ilaçlar
İlk bakışta, enzimin enfumafungin ile ve olmadan aldığı genel şekil neredeyse değişmemiş görünüyor. Kritik fark, çevredeki lipidlerin nasıl organize olduğunda ve bazı helikslerin ne kadar esnek olduğunda yatıyor. İlaç bağlandığında, yakındaki bir aromatik yan zincir enfumafungini sabitlemek için döner ve bir diğer kalıntı ile birlikte ilacın yanında düzenli bir lipidi stabilize eder. Eksterol benzeri lipitler, glukan ihracat yolu için tanımlayıcı rol oynayan yatay heliksler setinin etrafında düzenlenir. Bu lipitler kama ve destek gibi davranarak heliksleri ve kanal girişini belirli bir “bazal” düzene kilitler. Genetik testler, ilacın veya bu sterollerin temas noktalarını değiştirmeyi zayıf ilaç bağlanmasına veya enzim işlevinin yitirilmesine yol açtığını gösteriyor ve bu bölgelerdeki mutasyonlar insan ve bitki patojenlerinde bilinen direnç mutasyonlarıyla uyuşuyor.
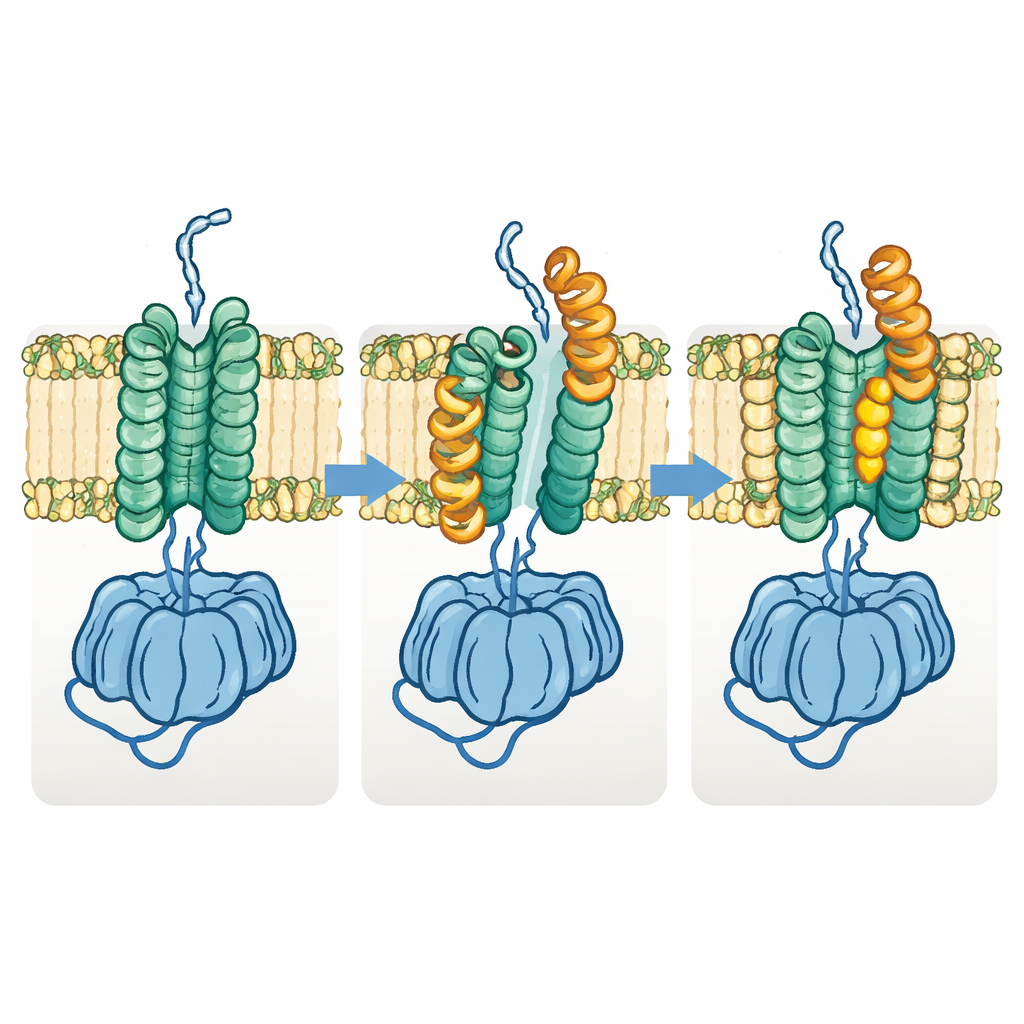
Polimer taşıma için gerekli bir şekil değiştirme
Araştırma ekibi ayrıca Fks1’in belirgin bir “açık” formunu keşfetti. Bu durumda membran bölgesinin yarısı yana kayıyor ve anahtar yatay heliksler dışa doğru sallanarak iki membran demeti arasındaki alanı açıyor ve görünür glukan tünelini genişletiyor. Çok sayıda yapının karşılaştırılması, enzimin normal çalışması sırasında bazal ve açık durumlar arasında döngüye girdiğini düşündürüyor: bazal durum polimer oluşumunu hazırlar ve başlatırken, açık durum büyüyen zincirin zar boyunca dışa doğru yanlamasına hareket etmesine izin veriyor. Yazarların enzimi kalıcı olarak her iki durumda kilitlemeyi amaçlayan disülfit bağları mühendisliklerle oluşturduklarında, her iki varyant da büyük ölçüde aktivitesini kaybetti; bu da bu şekil değiştirmenin işlev için gerekli olduğu fikrini destekliyor.
Geleceğin antifungal ilaçları için çıkarımlar
Enfumafungin ve ilişkili ilaçların katalitik cebi engelleyerek değil, yerel zar ortamını yeniden şekillendirerek ve glukan sentazı bazal durumda dondurarak etki ettiğini göstermesiyle bu çalışma alışılmadık bir ilaç etki mekanizmasını ortaya koyuyor. Ayrıca Fks1 ve Fks2’nin neredeyse aynı yapıları ve ilaç yanıtlarına sahip olduğunu göstererek dirençle mücadelede her ikisinin de dikkate alınması gerektiğini açıklıyor. Daha geniş anlamda bu çalışma, küçük moleküllerin sığ yüzeylere bağlanarak ve lipitleri işe katarak “ilaçlanamaz” olarak görülen membran proteinlerini nasıl kontrol edebileceğini vurgulayarak, mantarlar evrimleşse bile etkili kalabilecek yeni nesil antifungalların tasarımı için kavramsal bir şablon sunuyor.
Atıf: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Anahtar kelimeler: antifungal ilaçlar, mantar hücre duvarı, glukan sentaz, ilaç direnci, kriyo-elektron mikroskopisi