Clear Sky Science · tr
Fare hedefleyen fare retinasına yönelik genom düzenleme protein taşıyıcı ajanları geliştirmek için kombinatoryel sentetik strateji
Kalıtsal körlüğün tedavisinde yeni umut
Kalıtsal körlüğün birçok biçimi, gözün arkasındaki ışık algılayıcı hücrelerdeki tek bir hatalı genle başlar. CRISPR gibi modern gen düzenleme araçları, prensipte bu hataları düzeltebilir, ancak düzenleme makinelerini güvenli biçimde doğru hücrelere ulaştırmak büyük bir engel olmuştur. Bu çalışma, özel tasarlanmış yağ benzeri partiküller kullanarak güçlü gen düzenleyicileri doğrudan fare retinasına taşımanın yeni bir yolunu tanımlıyor ve tek seferlik tedavilerle genetik göz hastalığı olanlarda görmenin geri kazanılma olasılığını gündeme getiriyor.
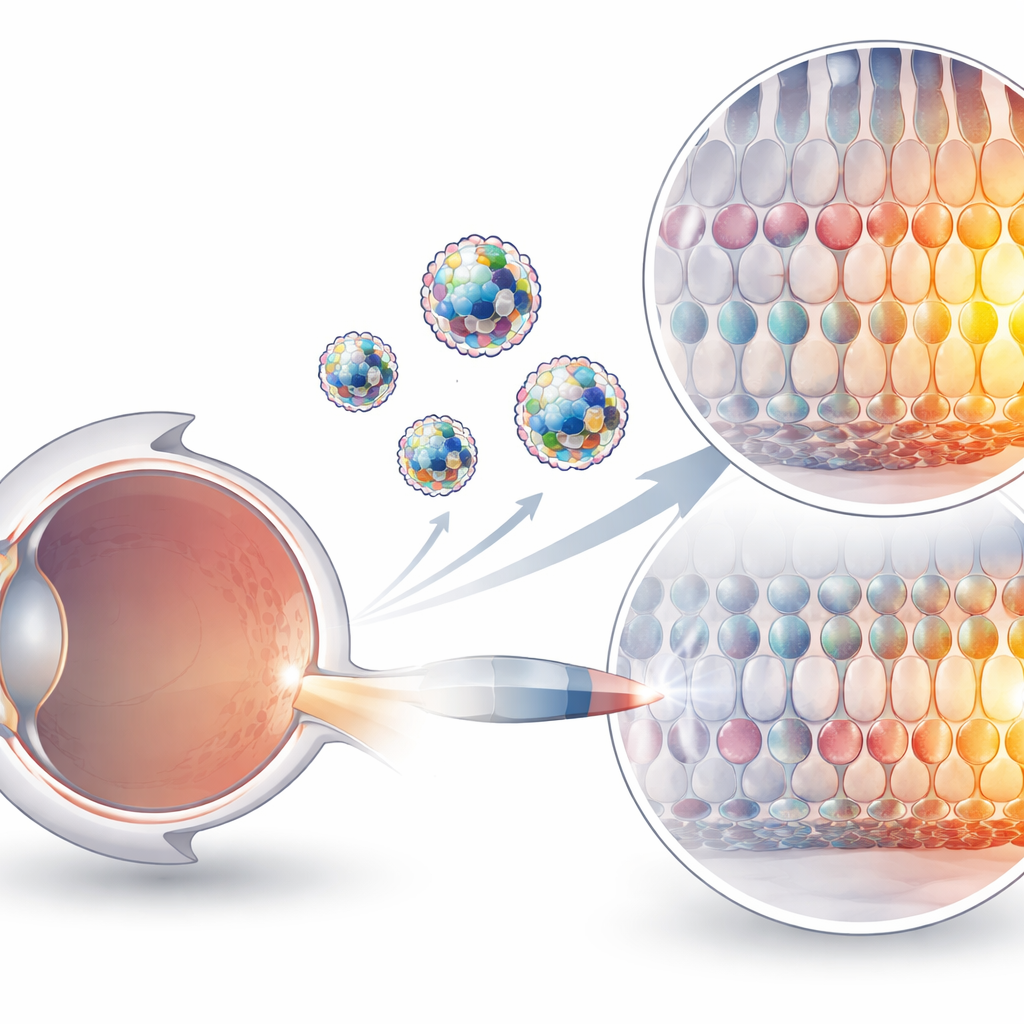
Gen düzenleyicilerin teslim edilmesini zorlaştıran nedenler
CRISPR tabanlı araçlar artık her iki DNA zincirini kesmeden bireysel DNA harflerini değiştirebiliyor; bu, onları genetik bozuklukların tedavisi için cazip kılıyor. Ancak bu araçlar hacimli protein–RNA makineleri olup vücutta elektriksel olarak yüklü ve hassastır. Mevcut taşıma yöntemleri büyük ölçüde modifiye edilmiş virüslere veya düzenleyicinin kendisi yerine düzenleyicinin genetik planlarını taşıyan partiküllere dayanıyor. Viral araçlar bağışıklık tepkileri tetikleyebilir ve boyut sınırlamalarına tabidir; haberci RNA ile teslimat karaciğerde çok iyi çalışırken göz dahil birçok dokuda hâlâ verimsiz kalır. Önceden monte edilmiş protein–RNA komplekslerini doğrudan enjekte etmek kavramsal olarak daha temiz ve daha güvenli olsa da, bunların hücre zarlarını aşmalarına ve hedeflerine ulaşmalarına yardımcı olacak uygun bir taşıyıcı eksikti.
Proteinler için boya esinli bir taşıyıcı
Araştırmacılar beklenmedik bir başlangıç noktasına yöneldiler: biyoloji laboratuvarlarında yaygın olarak kullanılan ve belirli göz ameliyatları için onaylı olan Coomassie Brilliant Blue adlı koyu mavi boya. Bu boya birçok farklı proteine sıkıca yapışıyor. Ekip, Coomassie “başlarını” yağ benzeri “kuyruklara” kimyasal olarak bağlayarak lipidoid adı verilen yeni bir molekül ailesi yarattı. Suda bu lipidoidler, yağlı kısımları içe gömülü ve Coomassie grupları dışa açık olacak şekilde kümelenme eğilimindedir; dışta yer alan bu gruplar proteinleri yakalayabilir. Kuyrukların uzunluğu, dallanması ve yükünü değiştirerek, bilim insanları bir tarafta gen düzenleyici proteinlere bağlanıp diğer tarafta hücre zarlarıyla etkileşime girecek onlarca aday bileşik tasarladı.
Göz hücrelerine protein tesliminin test edilmesi
Hangi tasarımların gerçekten işe yaradığını görmek için grup önce Cre rekombinaz adlı basit bir test proteini kullandı; bu protein, mühendislik yapılmış hücre ve farelerde genetik bir anahtarı yeşilden kırmızıya ya da kırmızıdan yeşile çeviriyor. Bazı Coomassie lipidoidleri Cre’i kültür hücrelerine verimli biçimde taşıdı ve hücrelerin büyük bir kısmını yeşilden kırmızıya çevirdi. Raportör farelerin retina altına enjekte edildiğinde, seçilmiş bileşikler hem görmeyi destekleyen pigment tabakasında hem de ışığı algılayan fotoreseptörlerde çarpıcı renk değişiklikleri tetikledi; bu da proteinlerin birçok körlüğe neden olan hücrelere ulaştığını gösterdi. Bu erken deneyler ayrıca lipidoid yapısındaki ince değişikliklerin hangi hücre tiplerinin hedeflendiğini kaydırabileceğini ortaya koydu; bu, gelecekteki versiyonların belirli retinal katmanlar için ayarlanabileceğini ima ediyor.
Gen düzenlemeyi artırma ve görüşün kurtarılması
Sırada, ekip sistemlerini adenine baz editörü ile doldurdu; bu, rd12 farelerinde görme kaybına neden olan tek harfli spesifik mutasyonu düzeltebilen rafine bir CRISPR varyantı. Editörün protein–RNA kompleksi tek başına hücrelere zayıf nüfuz ediyordu. CBB11 olarak adlandırılan bir lipidoid teslimatı iyileştirdi ama çözeltide kümelenme eğilimindeydi. Bunu stabilize etmek için araştırmacılar CBB11’i küçük, iyi tanımlanmış lipozomların içine gömdüler—bunlar mRNA aşılarında kullanılan klinik bileşenleri de içeren birkaç tip lipidden oluşan boş kürelerdi. Bu formülasyonlarda lipozom yüzeyindeki CBB11 editörün protein kısmını yakalarken, diğer lipidler RNA kılavuzu bağlamaya yardımcı oldu ve tüm kompleksi partikül yüzeyinde tutan işbirlikçi bir kabuk oluşturdu.
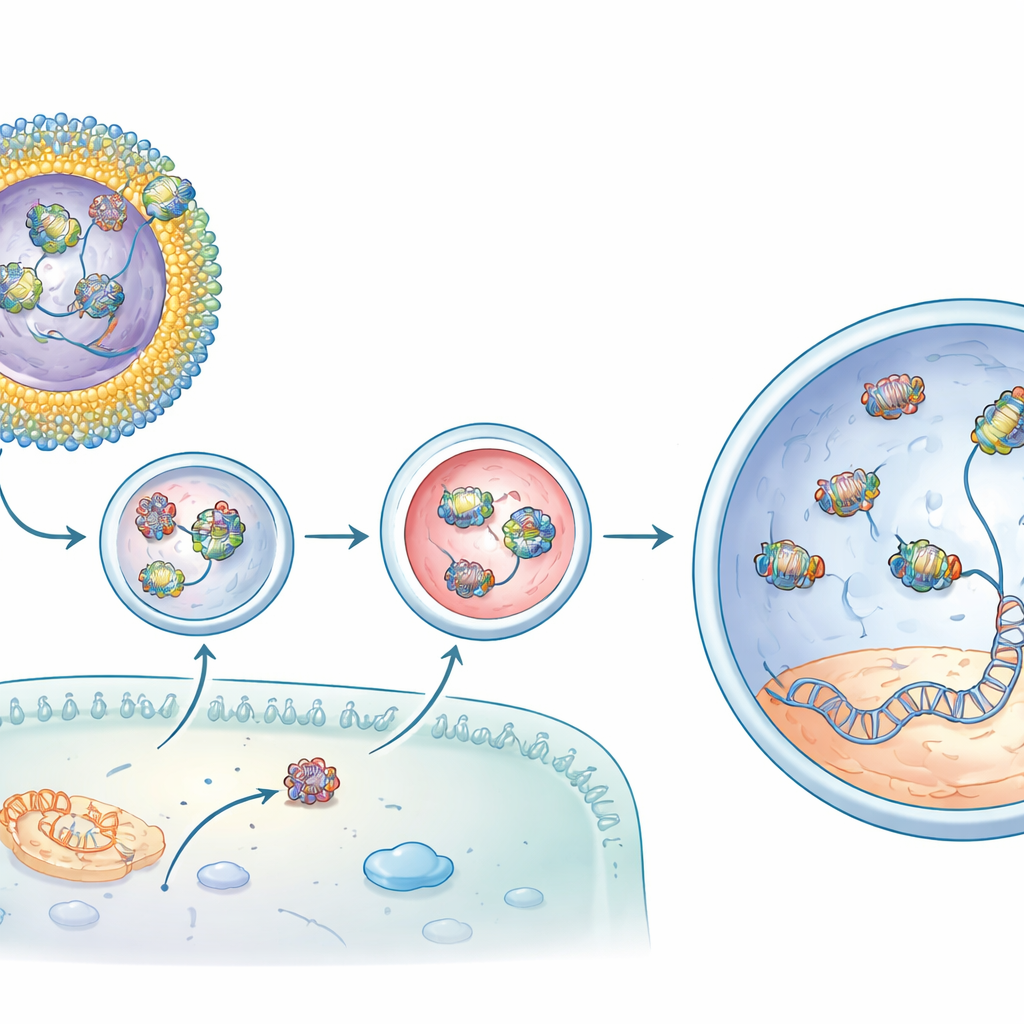
Moleküler onarımdan ışık yanıtlarının geri kazanılmasına
CBB11 içeren ve baz editörü taşıyan bu lipozomlar rd12 farelerin retina altına enjekte edildiğinde sonuçlar çarpıcıydı. Editörün tek başına enjekte edilmesiyle karşılaştırıldığında, optimize edilmiş formülasyon hedef gen içindeki istenen DNA düzeltmesini ondan çok daha fazla — bir mertebeden fazla — artırdı ve düzeltilmiş haberci RNA seviyelerinde daha yüksek artışlar üretti. Kimyasal analizler, hastalıkta eksik olan ışığa duyarlı retinal pigmentin geri kazanıldığını gösterdi. En etkileyici olarak, hayvanların gözlerinden alınan elektriksel kayıtlar, rod hücrelerinin loş ışığa yanıt verme yeteneklerinin büyük kısmını yeniden kazandığını ortaya koydu—en iyi vakalarda normal bir farenin sinyalinin yaklaşık üç çeyreğine kadar. Genomun diğer bölgelerindeki hedef dışı değişiklikler arka plan düzeyindeydi; bu da düzenlemenin hem güçlü hem de hassas olduğunu düşündürüyor.
Gelecek göz terapileri için bunun anlamı
Uzman olmayan birine göre ana mesaj, yazarların yaşayan göze doğrudan çalışan yeniden kullanılabilir bir gen düzenleyici proteinler “servis aracı” inşa etmiş olmalarıdır. Güvenli, aşı benzeri yağ parçacıklarını protein tutan bir boya ile süsleyerek, yüzeyinde farklı düzenleyicileri yakalayabilen, bunları retinal hücrelere teslim eden, hastalık yapan mutasyonları düzelten ve tek bir tedaviyle farelerde görmeyi ölçülebilir şekilde geri getiren bir sistem yarattılar. Güvenliği tam olarak değerlendirmek, hedeflemeyi iyileştirmek ve yöntemi insan kullanımına uyarlamak için daha fazla çalışma gerekse de bu platform, kalıtsal retinal hastalıklar ve dikkatli, lokalize DNA onarımının körlük ile görme arasındaki farkı yaratabileceği diğer genetik durumlar için gelecekteki tek seferlik hassas ilaçlara işaret ediyor.
Atıf: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Anahtar kelimeler: retinal gen terapisi, CRISPR baz düzenleme, lipozomlar, protein teslimi, kalıtsal körlük