Clear Sky Science · tr
FLASH-MM: doğrusal karışık etkili modeller kullanarak hızlı ve ölçeklenebilir tek hücreli diferansiyel ifade analizi
Neden küçük hücreler büyük hesaplama desteğine ihtiyaç duyar
Modern biyoloji artık yüz binlerce bireysel hücrede binlerce genin etkinliğini eş zamanlı olarak okuyabiliyor. Bu tek hücreli bakış, vücudumuzun enfeksiyonlarla nasıl savaştığını, kadınlarla erkekler arasındaki farklılıkları veya hastalık gelişimini daha net görmeyi vaat ediyor. Ancak bu devasa, dağınık veri kümelerini güvenilir keşiflere dönüştürmek acı verici derecede yavaş olabilir ve dikkatsizce yapılırsa yanıltıcı sonuçlar doğurabilir. Bu makale, istatistikleri doğru tutarken hesaplamayı günümüzün en büyük çalışmalarına yetecek kadar hızlandıran yeni bir tek hücre veri işleme yöntemi olan FLASH-MM’i tanıtıyor.
Gürültülü, kalabalık hücre verilerinin zorluğu
Tek hücreli RNA dizileme her bir hücrede hangi genlerin “açık” veya “kapalı” olduğunu ölçer; bu ölçümler birçok kişi ve koşul arasında yapılır. Aynı kişiye ait hücreler genleri ve yaşam öykülerini paylaştıkları için birbirine benzer görünme eğilimindedir, oysa kişiler arasında geniş farklılıklar bulunur. Bu, veride katmanlı bir yapı oluşturur: her kişide çok sayıda hücre ve her koşulda (örneğin hasta vs. sağlıklı) çok sayıda kişi. Bu ilişkiler göz ardı edilirse, standart yöntemler her hücreyi bağımsız veri noktasıymış gibi sayarak binlerce geni yanlışlıkla değişmiş olarak etiketleyebilir. Aynı zamanda, tek hücre veri setleri boyut olarak patladı; şimdi yüzlerce katılımcı ve milyonlara varan hücreleri içerebiliyor ve geleneksel istatistiksel araçları zaman ve bellek açısından sınırlarının ötesine zorluyor.
İnsanları ve hücreleri modellemek için daha akıllı bir yol
Bu karmaşıklıklarla başa çıkmak için, istatistikçiler genellikle koşullar arasındaki tutarlı farkları (örneğin tüberküloz durumu veya cinsiyet) rastgele bireyler arası farklılıklardan açıkça ayıran doğrusal karışık etkili modellere başvurur. Pratikte bu modeller, aynı kişiden gelen hücrelerin benzerliklerini ve kişiler arasındaki değişimi hesaba katabildikleri için tek hücre çalışmaları için idealdir. Ancak yaygın olarak kullanılan yazılımlar büyük tek hücre deneylerinde ciddi şekilde yavaşlıyor veya bellek yetersizliğine uğruyor. Bu nedenle araştırmacılar sıklıkla her bir kişideki aynı hücre tipinin sayımlarını ortalamak gibi kestirme çözümlere yöneliyor; oysa bu, tek hücre verilerinin gücünü sağlayan ince hücreler arası bilgilerin çoğunu yok ediyor.
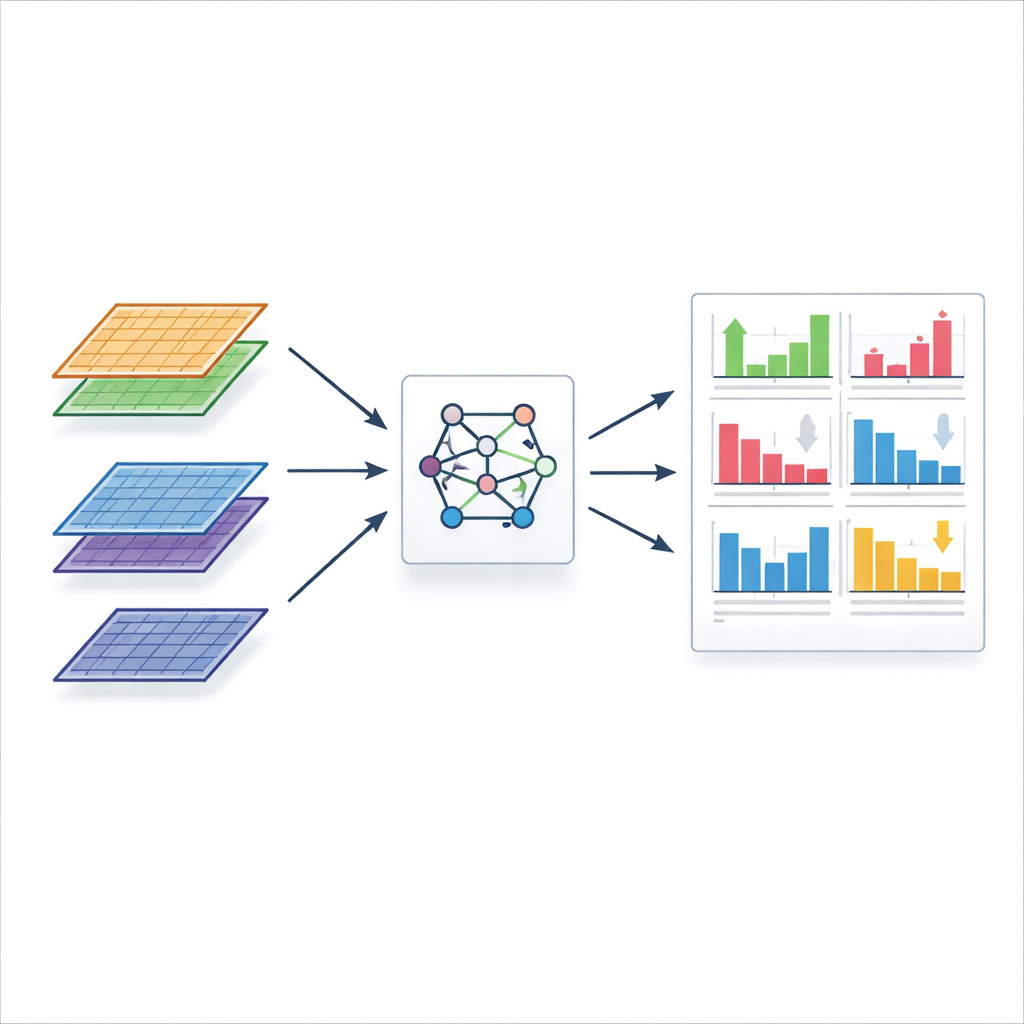
FLASH-MM ağır işi nasıl hızlandırıyor
FLASH-MM, karışık etkili modellerin güçlü yönlerini korurken hesaplamaların yapılış şeklini yeniden tasarlar. Devasa hücre×gen tablolarını defalarca taramak yerine FLASH-MM önce her veri kümesini kütüphane büyüklüğü, hücre tipi, tedavi veya donör gibi bilinen özelliklerle hücrelerin ilişkisini yakalayan kompakt özet sayılara dönüştürür. Çekirdek algoritma daha sonra sadece bu küçük matrislerle çalışır; böylece hesaplama yükü her hücre ile ölçeklenmek yerine model bileşenlerinin çok daha küçük sayısıyla ölçeklenir. Yazarlar ayrıca model varyansının temsil şeklini ince ayar yaparak standart istatistiksel testlerin geçerliliğini korurlar; bu sayede basit t ve z istatistikleri hem ilgilenilen ana etkileri hem de kişi-ara farklılıkların ek değerini değerlendirebilir. Gerçekçi yapay verilerle yapılan simülasyon çalışmalarında FLASH-MM’nin sonuçları altın standart yazılımlarla birkaç ondalık basamağa kadar örtüşürken, yaklaşık 50–140 kat daha hızlı çalıştığı ve çok daha az bellek kullandığı gösterildi.
Yöntemi gerçek dokularda uygulamak
Gerçek dünya etkisini göstermek için ekip FLASH-MM’i iki zorlu tek hücre veri setine uyguladı. 19 donörden elde edilen 27.000’den fazla sağlıklı insan böbrek hücresinden oluşan bir haritada FLASH-MM, her hücre tipinde erkek ve kadın donörler arasındaki gen etkinliği farklarını ararken her kişiyi rastgele bir faktör olarak ele aldı ve aşırı güvenli sonuçları engelledi. En güçlü cinsiyete bağlı desenleri, erkek hücrelerinin asit yönetimi ve kan basıncıyla ilişkili yolaklara, kadın hücrelerinin ise sinyal iletimi ve reseptör geri dönüşümü süreçlerine zenginleşme gösterdiği belirli bir böbrek tübül hücre tipinde buldu. FLASH-MM bu analizi yaklaşık bir dakika içinde tamamladı; oysa standart bir araçla neredeyse iki saat sürmüştü. Yöntem ayrıca tüberküloz kohortundan 259 kişiden yaklaşık yarım milyon bellek T hücresini analiz ederek farklı aktive T hücre durumlarında hastalık durumuyla ilişkili gen ve yolak setlerini tanımladı. Burada FLASH-MM bir buçuk saatin altında tamamlanırken, geleneksel yaklaşımda iki günden fazla sürmüştü.
Gelecekteki hücre başına hücre çalışmaları için anlamı
Halk diliyle söylemek gerekirse, artık tek hücreli veri selinden köşe kapatmadan daha iyi yararlanabileceğimiz anlamına geliyor. FLASH-MM hangi hücrelerin hangi kişiden ve hangi koşuldan geldiğini izliyor; böylece tespit edilen gen değişiklikleri örnekleme veya partiden kaynaklanan tuhaflıklardan ziyade gerçek biyolojiyi yansıtma olasılığı daha yüksek oluyor. Aynı zamanda, yalın hesaplamaları yüz binlerce hücrenin standart bilgisayarlarda analiz edilebilir olmasını sağlıyor ve ince hastalık sinyalleri, cinsiyet farklılıkları ve nadir hücre durumlarının daha iddialı çalışmalarının önünü açıyor. Yöntem genel amaçlıdır ve hem R hem Python’da mevcut olduğundan uzamsal gen haritalama ve çok katmanlı moleküler ölçümler gibi yeni teknolojilere genişletilebilir; bu da araştırmacıların geniş hücre düzeyindeki veri kümelerini sağlam, klinik açıdan anlamlı içgörülere dönüştürmesine yardımcı olur.
Atıf: Xu, C., Pouyabahar, D., Voisin, V. et al. FLASH-MM: fast and scalable single-cell differential expression analysis using linear mixed-effects models. Nat Commun 17, 2384 (2026). https://doi.org/10.1038/s41467-026-69063-2
Anahtar kelimeler: tek hücre RNA dizilemesi, diferansiyel ifade, doğrusal karışık etkili modeller, istatistiksel genomik, hesaplamalı biyoloji