Clear Sky Science · tr
Paclitaxel, Nab-paclitaxel’e kıyasla daha zayıf tedavi etkinliğinin altında yatan TREM2+ makrofaj genişlemesini tetikliyor
Bu çalışma neden önemli
Meme kanseri tanısı konan birçok kadın, taksan denilen kemoterapi ilaçları alıyor; en yaygın olanı paklitaksel veya albümin parçacıklarına bağlanmış daha yeni bir form olan nab‑paklitaksel. Hekimler uzun süredir yeni ilacın sıklıkla daha iyi sonuç verdiğini şüphe ediyorlardı, fakat nedenleri belirsizdi. Bu çalışma hasta verilerini ve hayvan deneylerini inceleyerek, standart paklitakselin bağışıklık hücrelerini yeniden şekillendirerek istemeden kanserin akciğere yayılmasına yardımcı olabileceğini gösteriyor ve bu zararlı yan etkiyi engellemenin bir yolunu işaret ediyor.
Görünüşte benzer iki ilaç, iki farklı sonuç
Araştırmacılar önce binlerce meme kanserli kadında paklitaksel ile nab‑paklitakselin gerçek dünya performansını karşılaştırdı. 6.486 hastayı içeren 17 klinik çalışmanın sonuçlarını birleştirerek, nab‑paklitakselin tümör küçülme oranlarını ve ameliyat öncesi memede ve çevre lenf düğümlerinde kanserin tam kaybolma oranlarını daha yüksek yaptığını buldular. Bu avantaj, özellikle önceki tedaviler başarısız olduktan sonra uygulanan hastalarda belirgindi. Oysa her iki ilaç benzer dozlarda verildi ve bölünen kanser hücrelerine benzer şekilde saldıracak biçimde tasarlanmıştı; bu da aralarındaki farkın doğrudan tümör öldürmenin ötesinde bir mekanizmaya işaret ettiğini düşündürüyor.
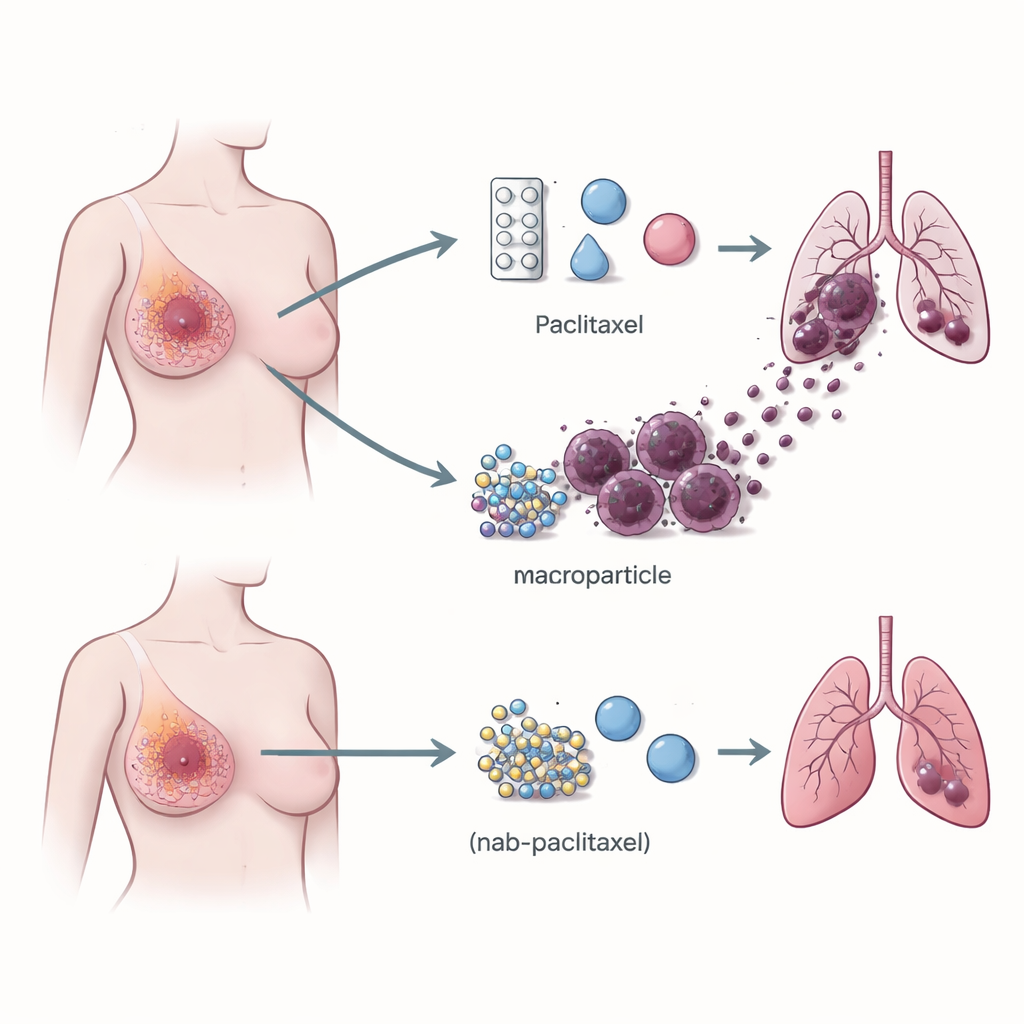
Kansere yayılmada yardımcı olan bağışıklık hücreleri
Dikkat, tümörün bağışıklık ortamına—kanserle savaşabilen veya şaşırtıcı derecede sıkça ona yardımcı olabilen beyaz kan hücrelerinin karışımına—kaydı. Binlerce tek hücrenin gen etkinliğini okuyan tek hücreli RNA dizileme kullanarak ekip, paklitaksel ile nab‑paklitakselle tedavi edilen hastalardan alınan tümörleri karşılaştırdı. Paklitakselle tedavi edilen tümörlerin yüzeylerinde TREM2 adı verilen bir reseptörü taşıyan çok daha fazla makrofaj içerdiğini buldular. Bu TREM2‑pozitif makrofajlar tümör kenarlarında zenginleşmişti ve daha sonra akciğer metastazı gelişen hastalarda, kanseri yerinde kalanlara göre çok daha fazla bulundu. Bu desen daha geniş hasta gruplarında ve fare modellerinde de doğrulanarak bu makrofaj tip ile kanser yayılma riski arasında güçlü bir bağ kuruldu.
Tedavi tümörleri küçültürken yayılmayı beslediğinde
Meme tümörü olan farelerde paklitaksel beklenen etkiyi yaptı: primer tümörleri yavaşlattı veya küçülttü. Ancak aynı zamanda akciğerdeki kanser yatakları sayısını artırdı ve tümörlerde ile kanda TREM2‑pozitif makrofajları yükseltti. Buna karşılık nab‑paklitaksel, ana tümörü küçültmede aynı derecede etkili olmasına rağmen akciğer metastazını tetiklemedi veya bu makrofajları genişletmedi. Farelerde TREM2 geni silindiğinde veya TREM2 antisent oligonükleotidlerle (belirli genleri susturan kısa DNA parçaları) azaltıldığında, paklitaksel primer tümörleri hâlâ küçülttü ancak akciğere yayılmayı büyük ölçüde besleme yeteneğini kaybetti. Bu, TREM2 taşıyan makrofajların sadece seyirci olmadığını; paklitaksel kaynaklı metastazda gerekli ortaklar olduğunu gösteriyor.
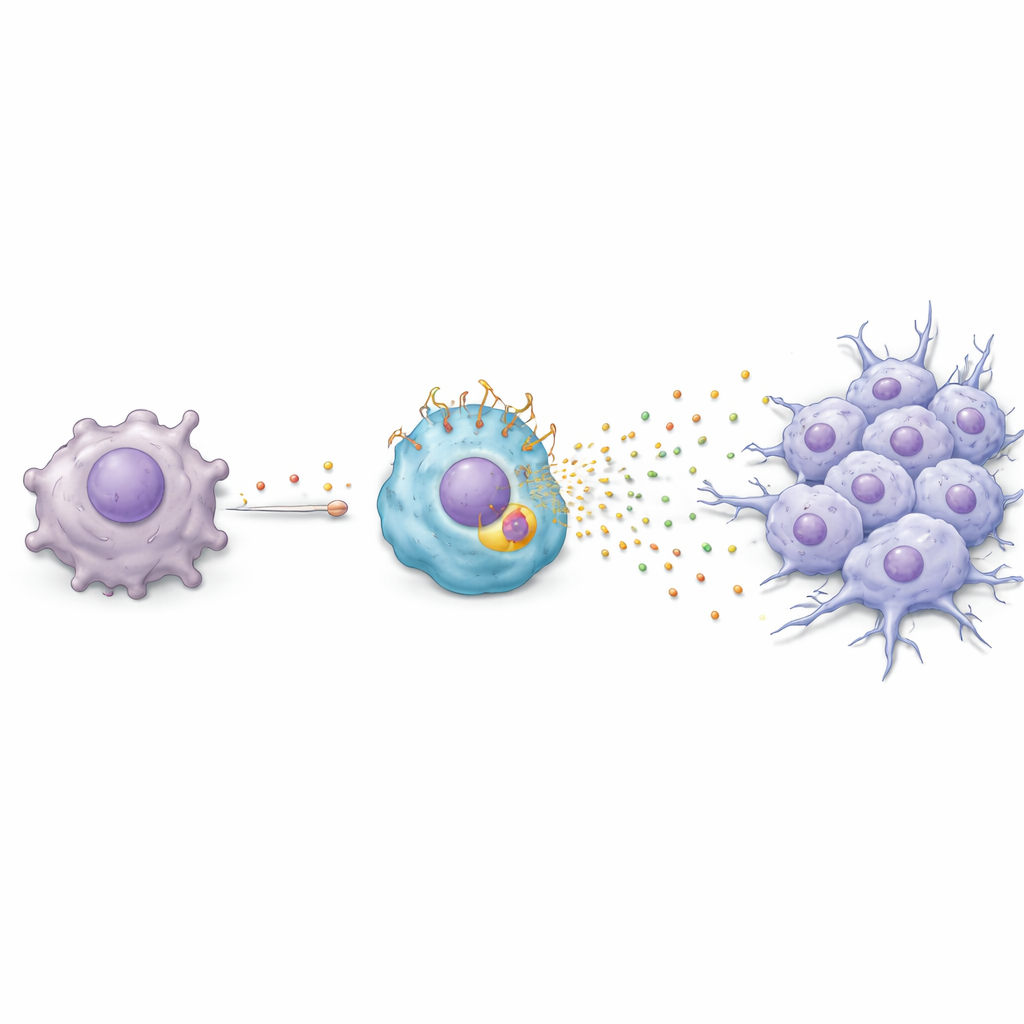
Tümörden bağışıklık hücresine kimyasal bir zincirleme reaksiyon
Ekip bir sonraki soruda paklitakselin makrofajları bu zararlı, TREM2 bakımından zengin duruma nasıl dönüştürdüğünü sorguladı. Bir zincirleme reaksiyon keşfettiler: paklitaksel kanser hücrelerine ATF3 adlı bir stres yanıt genini açtırma sinyali veriyor, bu da FGF2 adlı bir büyüme faktörünün üretimini artırıyor. Kanser hücreleri ardından FGF2’yi çevrelerine salıyor ve bu, yakınlardaki makrofajlarda etkili oluyor. O makrofajlarda FGF2, TREM2 düzeylerini artıran başka bir düzenleyici olan EGR1’i aktive ediyor. TREM2 yüksek seviyeye ulaştığında makrofajlar Serpin E1, HGF, CCL3 ve CXCL2 dahil bir protein kokteyli salgılamaya başlıyor; bunlar kanser hücrelerini daha hareketli, invaziv bir çeşide—epitelyal‑mezenkimal geçişe—itiyor. Laboratuvar ortamında ve farelerde bu kimyasal çapraz konuşma, tümör hücrelerini göç etmeye ve istila etmeye daha yatkın hale getirdi; bu, metastaza giden yol üzerindeki kilit adımlar.
Çift taraflı kılıcı daha güvenli bir araca çevirme
Halk açısından ana mesaj şudur: paklitaksel çift taraflı bir kılıç gibi davranabilir: tümörlere saldırırken aynı zamanda belirli bağışıklık hücrelerine kanserin uzak organlara kaçmasına yardım etme talimatı da veriyor. Nab‑paklitaksel bu özel bağışıklık hatasını tetiklemekten kaçınıyor gibi görünüyor. Cesaret verici haber, TREM2’yi veya FGF2–EGR1–TREM2 sinyal zincirinin parçalarını engellemenin, hayvan modellerinde paklitakselin tümör küçültme faydalarını metastazı teşvik etme risklerinden ayırabilmesi. Benzer stratejiler insanlarda güvenli ve etkili bulunursa, hekimler tanıdık ve yaygın olarak ulaşılabilen bu kemoterapi ilacını kullanmaya devam ederken kanser yayılma eğilimini azaltabilir; bu da hastalar için daha iyi uzun vadeli sonuçlara yol açar.
Atıf: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Anahtar kelimeler: meme kanseri, paklitaksel, tümör mikroçevresi, makrofajlar, metastaz