Clear Sky Science · tr
Canlı organizmada çift yönlü RNA-Seq, ekstraselüler bir patojenin epitel bariyerini bozmasında önemli efektörleri ortaya çıkarıyor
Bazı Mikroplar Hücresel Çitlerimizin Yanından Nasıl Sızıyor
Organlarımız, kanı, mikrop ve toksinleri olması gerektiği yerde tutan sıkıca paketlenmiş hücrelerle kaplıdır; bunlar duvar gibi davranır. Yine de bazı mikroplar bu hücreler arasından kayıp vücutta yayılmayı başarır. Bu çalışma, dünya çapında ciddi bir hastalık olan leptospirozu yapan bakterinin karaciğer ve böbrek gibi organlara nasıl sessizce ulaştığını ve ardından hücre içindeki kalsiyumu kullanan zekice bir hileyle bu koruyucu bariyerleri nasıl araladığına ilişkin ayrıntıları çarpıcı biçimde açıklıyor.
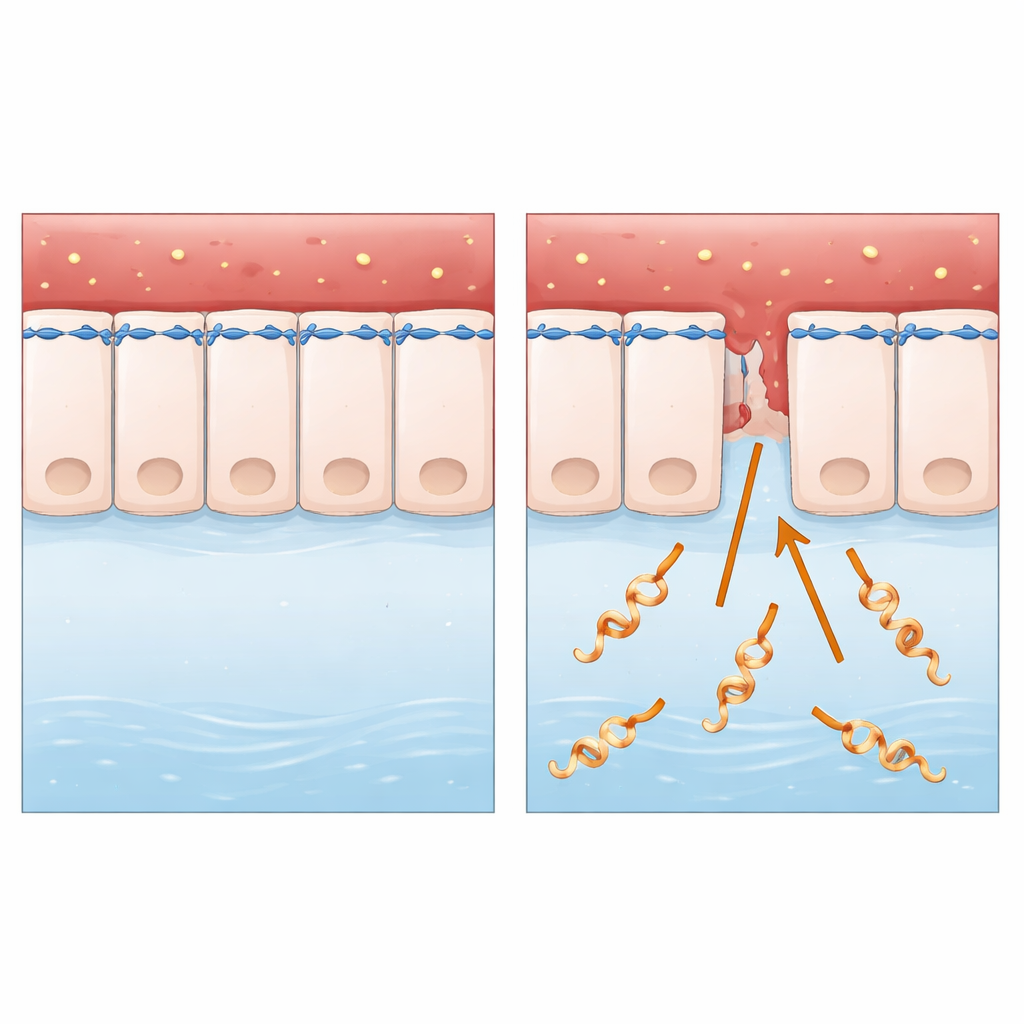
Hayvan ve İnsan Dokularının Sinsi Bir İstilacısı
Araştırma, esas olarak kirli su veya toprak yoluyla hayvanlardan insanlara geçen spiral biçimli Leptospira interrogans bakterisine odaklanıyor. Küçük deri yaraları veya mukoza zarı yoluyla girdikten sonra kan dolaşımıyla yayılır ve karaciğer ile böbrek yetmezliği ve iç kanama dahil olmak üzere şiddetli hastalığa yol açabilir. Pek çok iyi çalışılmış mikrobun aksine, Leptospira hücrelerin dışında yaşar ve bilim insanlarının genellikle aradığı klasik “moleküler silahlardan” bazılarına sahip değildir. Bu da onu temel bir soruyu sormak için ideal bir sınama vakası yaptı: görece basit, serbest yaşayan bir bakteri sağlam hücre katmanlarını bu kadar verimli şekilde nasıl geçebiliyor?
Konakçı ve Mikrop Genlerinin Aynı Anda Konuşmasını İzlemek
Enfeksiyon sürecini canlı bir hayvanda yakalamak için ekip, akut leptospirozun modeli olarak hamsterlarda çift yönlü RNA dizileme kullandı. Bu yöntem hem konakçının hem patojenin hangi genlerinin aynı anda açıldığını veya kapandığını okur. Bilim insanları hamsterları enfekte etti ve bir ile üç gün sonra karaciğer ve böbrek dokusu topladılar. Erken dönemde, yüksek bakteri sayısına rağmen hayvanların hücrelerinde gen aktivitesinde neredeyse hiçbir değişiklik yoktu; bu, Leptospiranın başlangıçta bağışıklık sisteminin radarının altından kaydığına işaret ediyordu. Ancak üçüncü gün itibarıyla her iki organ da güçlü bir yanıt gösterdi, özellikle karaciğer: iltihap, hücre–hücre bağlantıları ve hücrelerin iç iskeletiyle ilgili genler keskin şekilde değişmişti; bu da doku bariyerlerinin aktif olarak yeniden şekillendiğini gösteriyordu.
Dışarıdan İçeri Hücresel Fermuarı Bozmak
Hücre katmanları, komşu hücreleri birbirine bağlayan ve bunları aktin ve miyozinden oluşan bir halka üzerine sabitleyen sıkı ve adherens bağlantılarla mühürlenir; aynı protein çifti kasların kasılmasına da yardım eder. Leptospira ile enfekte edilmiş insan epitel hücrelerinin mikroskopik incelemesi, hücrelerin şeklinde değişiklikler olduğunu, hücreler arasında boşluklar açıldığını ve anahtar bağlantı proteinlerinin zayıfladığını ya da yanlış yerde olduğunu gösterdi. Önemli olarak, hücreler ölmedi; bu, bariyerin yok edilmediği, söküldüğü anlamına geliyordu. Araştırmacılar ayrıca hücrelerin protein katlama fabrikalarında stres işaretleri gördü, ancak bu stresi engellemek bağlantıları geri getirmedi; bu da onları başka bir suçluya yönlendirdi.
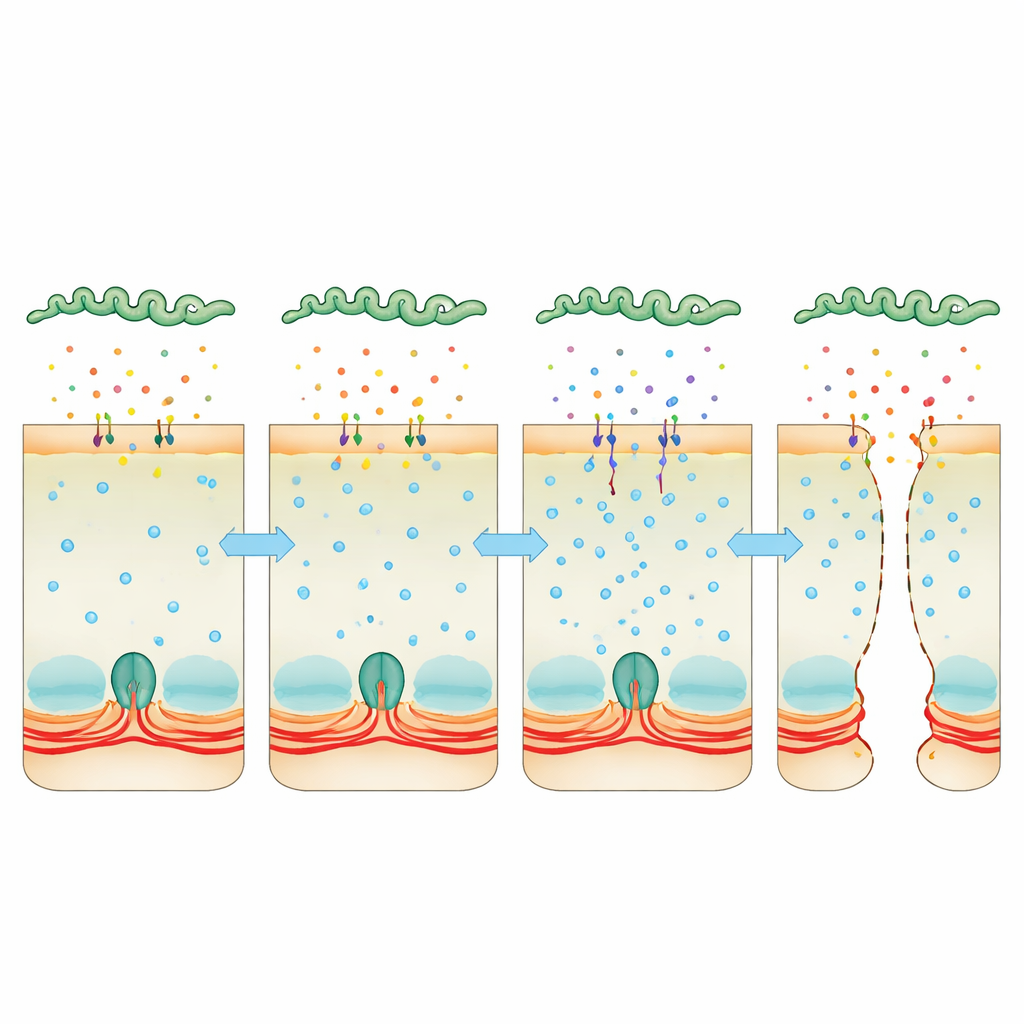
Gizli Bir Kaldıraç Olarak Kalsiyumun Ele Geçirilmesi
Dikkat, hücre içinde aktin–miyozin halkasını sıkılaştırıp gevşetebilen evrensel bir sinyal olan kalsiyuma çevrildi. Enfekte hücrelerde daha fazla kalsiyum birikti ve bu, kontraktil halkayı bağlantılara çektiren bir enzim olan miyozin hafif zincir kinazın daha yüksek aktivitesiyle ilişkilendirildi. Ekip, kalsiyumu temizleyen bir bileşik veya kalsmodulin ya da bu kinazı inhibe eden ilaçlar kullandığında hücre katmanları daha bütün kaldı ve bakterilerin arasından sıyrılması daha zor hale geldi. Aynı zamanda bakteriyel RNA’nın derin dizilenmesi, konak içinde Leptospiranın toksinlere benzeyen iki “Virülans‑Değiştirici” proteinin üretimini güçlü biçimde artırdığını ortaya koydu. Bu proteinler çevreye salgılanıyor, konak hücrelerine yapışıyor ve hücre içinde bulunuyordu. Bakteriler bu proteinlerden birine veya her ikisine sahip olmadığında, hücre katmanlarını geçme veya öldürücü hastalık oluşturma kapasiteleri çok azaldı ve onların salgılanmış sıvısı artık kalsiyum seviyelerini yükseltmiyor ya da bağlantıları bu kadar etkili biçimde sökmüyordu.
Hastalık ve Gelecekteki Savunmalar İçin Anlamı
Bir araya getirildiğinde bulgular açık bir hikâye çiziyor. Vücuda neredeyse fark edilmeden sızdıktan sonra Leptospira, toksin benzeri Virülans‑Değiştirici proteinleri salgılamaya başlar. Bu proteinler epitel hücrelere bağlanır ve hücre içindeki kalsiyum dengesini bozar; bu da komşu hücreleri bir arada tutan hücresel “fermuarı” çeken bir kontraktil yolunu aktive eder. Sıkı ve adherens bağlantılar gevşediğinde mikroskobik boşluklar oluşur, bakterilerin hücreler arasından geçmesine, organları kolonize etmesine ve şiddetli hastalığı tetiklemesine izin verir. Kalsiyum odaklı bu mekanizmayı ve arkasındaki bakteriyel proteinleri belirleyerek çalışma, bu proteinleri veya onların sinyal yolunu engellemek gibi yeni stratejilere giden bir yol açıyor; bu da epitelsel çitlerimizi güçlendirmeye ve leptospirozu ile benzer taktiklerden yararlanan diğer enfeksiyonların yayılmasını sınırlamaya yardımcı olabilir.
Atıf: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Anahtar kelimeler: leptospirozis, epitel bariyer, kalsiyum sinyalleşmesi, bakteriyel toksinler, konakçı–patojen etkileşimleri