Clear Sky Science · tr
Supercharging destekli nDIA-MS, ilaç kaynaklı tüm proteom çözünürlük değişimlerinin küresel profillenmesini sağlıyor
Basit sayımların ötesinde neden protein davranışı önemlidir
İlaçlar, bir hücrenin ne kadar protein ürettiğini değiştirebilmenin yanı sıra o proteinin hücre içinde nereye gittiğini ve serbest mi yoksa hücresel yapılara mı yapıştığını da değiştirebilir. Proteinlerin hücre içinde “nerede” ve “nasıl” var olduğundaki bu kaymalar kanser ve nörodejenerasyon gibi hastalıklarla yakından bağlantılıdır, ancak ölçekli olarak ölçülmesi zordur. Bu çalışma, binlerce insan proteininin aynı anda taranarak çözünürlüklerinin — serbest mi yoksa daha bağlı bir durumda mı olduklarının — iki yaygın deneysel ilaca maruz kaldıklarında nasıl değiştiğini hızlı ve güçlü biçimde görmeyi sağlayan bir yöntem sunuyor.
Proteinlere bakmak için daha hızlı, daha keskin bir yol
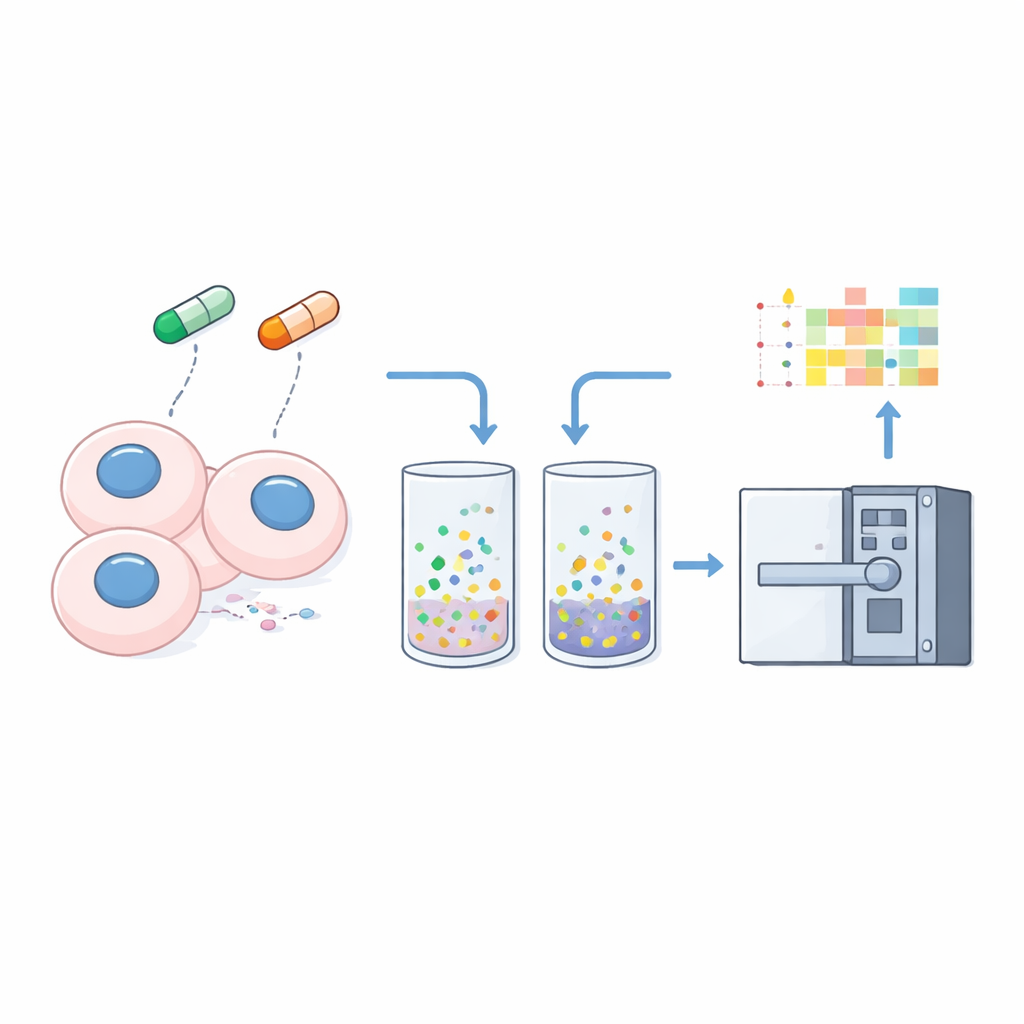
Yazarlar, modern biyolojinin temel teknolojilerinden birinin üzerine inşa ediyor: kütle spektrometrisi; protein parçacıklarını tartıp sayan bir teknik. Standart yöntemler her bir proteinin miktarını söylemede zaten başarılıdır, fakat protein durumundaki değişimleri — örneğin DNA’ya bağlanma veya yoğun topluluklara katılma gibi — ortaya koymakta zorlanırlar. Burada araştırmacılar, dar aralıklı veri-bağımsız edinim (nDIA-MS) adlı bir kütle spektrometrisi çeşidini iyileştiriyor. Peptidleri cihazdan taşıyan sıvıya küçük kimyasal yardımcılar, yani supercharging reaktifleri ekleyerek, bu parçacıkların elektrik yüklerini artırıyorlar ve sinyali büyük ölçüde güçlendiriyorlar.
İki yaygın supercharging katkı maddesini, dimetil sülfoksit (DMSO) ve m-nitrobenzil alkol (mNBA) test ettikten sonra, %3 DMSO’nun genel sinyal artışını ve tespit edilen protein sayısını en çok artırdığını; mNBA’nın ise bireysel peptid parçacıklarının sayısını ve yükünü artırmada daha iyi olduğunu buluyorlar. Optimum düzenlemeyle ekip, standart bir hücre sindiriminin sadece bir mikrogramından 15 dakikalık bir çalışmada yaklaşık 9.600 insan proteini tanımlayabiliyor — rutin deneyler için dikkat çekici bir hız ve derinlik bileşimi. Bu performans, nDIA-MS’yi yalnızca protein saymak için değil, aynı zamanda fiziksel durumlarının strese nasıl yanıt verdiğini araştırmak için de uygun hale getiriyor.
Çözünürlüğü hücresel değişimin bir okumasına dönüştürmek
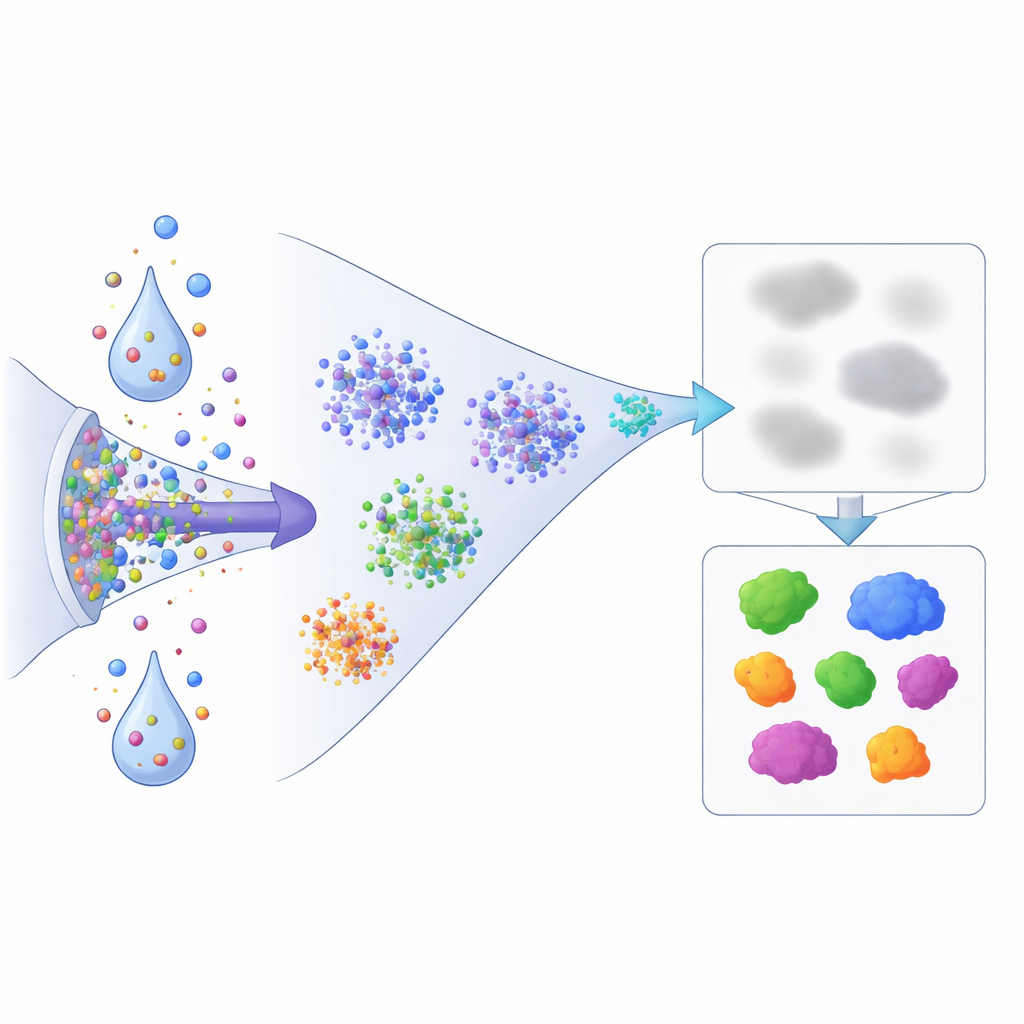
Çözünürlüğü ölçülebilir bir sinyale dönüştürmek için araştırmacılar hücreleri nazikçe hafif bir deterjanla ön işlemden geçiriyor; bu, serbestçe çözünür proteinleri çözerken DNA, membranlar veya diğer yapılara sıkı bağlanmış materyali geride bırakıyor. Optimiz edilmiş nDIA-MS yöntemiyle hem bütün hücre lizatı hem de bu “çözünmez” pelet üç kanser hücre hattından analiz ediliyor. Her proteinin pelet içindeki bolluğunu bütün hücre örneğine göre karşılaştırarak basit bir “çözünmezlik oranı” hesaplıyorlar — daha yüksek değerler hücresel yapılara daha güçlü bir bağlılığı, daha düşük değerler daha çözünür, serbest bir durumu gösterir.
Ekip daha sonra hücreleri yalnızca bir saat süreyle iki ilaca maruz bırakıyor: MG132, istenmeyen proteinlerin hücre tarafından parçalanmasını engelleyen bir proteazom blokeri; ve ML‑792, önemli bir protein işaretleme sistemini engelleyen SUMO aktivasyon inhibitörü. Bu kısa maruziyet kasıtlıdır; gen ekspresyonu değişiklikleri tam olarak ortaya çıkmadan önce protein davranışındaki hızlı, erken kaymaları yakalamayı amaçlar. Bu kısa pencerede bile, 8.694 protein için çözünürlük ve bolluk değişikliklerini nicelleştirebiliyorlar ve fraksiyonlamanın tübülinden histonlar gibi klasik çözünür proteinleri kromatin’e bağlı proteinlerden temiz biçimde ayırdığını doğruluyorlar.
Hücresel protein peyzajını yeniden şekillendiren ilaçlar
MG132 ve ML‑792 geniş çaplı fakat farklı biçimlerde protein çözünürlüğünü yeniden düzenliyor. MG132, üç hücre hattı boyunca binin üzerinde proteini daha çözünmez hale getirirken, altı yüzün üzerinde proteini daha çözünür yapıyor. Etkilenen birçok protein protein kalite kontrolü, DNA hasar yanıtı, gen düzenlemesi ve otofaji — hücrenin kendi kendini temizleme sistemi — kesişiminde yer alıyor. Örneğin, proteazom aktivatör kompleksinin bileşenleri ve hatalı proteinleri etiketlemeye yardımcı adaptörler daha az çözünür hale gelerek, yıkım engellendiğinde önemli kalite kontrol faktörlerinin kendilerinin kromatin veya hücresel membranlar gibi yapılara takılıp kaldığını düşündürüyor. Otofaji proteinleri ve stres düzenleyicisi HSF1 dahil hasar yanıtı oyuncuları da nükleer stres cisimciklerinin oluşumuyla tutarlı şekilde daha çözünmez, kondensat-benzeri durumlara kayıyor.
Buna karşılık ML‑792 güçlü bir şekilde transkripsiyonla ve SUMO sistemiyle ilgili proteinleri hedef alıyor. SUMO aktivasyonu engellendiğinde yüzlerce protein ya daha çözünmez ya da daha çözünür hale geliyor ve çekirdek SUMO proteinleri beklendiği üzere çözünür havuza geçiyor. Çalışma çarpıcı davranışları vurguluyor: RNA polimeraz III alt birimleri daha çözünmez hale gelerek değişmiş nükleer giriş veya kromatin bağlanmasını işaret edebilir; SP100 ve DAXX gibi nükleer cisimciklerle ilişkili ana baskılayıcılar daha çözünür hale gelerek SUMO işaretlerinin bu bileşenleri bu bölmelerde tutulmalarına yardımcı olduğunu gösteriyor. Her iki ilaç tek başına veya ardışık olarak uygulandığında, NAB2, SMAD2 ve RB1 dahil bazı proteinler koordine edilmiş ya da karşıt çözünürlük kaymaları gösteriyor; bu da ubikitin ve SUMO işaretleme sistemleri arasında protein lokalizasyonunu kontrol eden ince bir etkileşimi açığa çıkarıyor.
Gelecekte ilaç keşfi için bunun anlamı
Uzman olmayanlar için temel mesaj şudur: hücreler strese maruz kaldığında veya ilaçla tedavi edildiğinde proteinler yalnızca miktar olarak artıp azalmaz; aynı zamanda hareket eder, yoğunlaşır ve hücresel yapılara ne kadar sıkı bağlı olduklarını değiştirirler. Bu çalışma bu kaymaların gerçekleşmesini izlemek için yüksek hızlı, proteom çapında bir yol sunuyor. Ayarlanmış bir kütle spektrometrisi iş akışını basit bir çözünür-vs-çözünmez karşılaştırmayla birleştirerek yazarlar, yaygın deneysel ilaçların standart bolluk ölçümlerinin kaçıracağı şekillerde iç protein peyzajını hızla yeniden düzenlediğini gösteriyor. Bu yaklaşım, aday ilaçların hücre boyunca protein durumlarını nasıl yeniden şekillendirdiğini haritalamaya; beklenmedik hedefleri, stres yollarını ve hem terapötik etki hem de yan etkileri anlamada kritik olabilecek başarısızlık noktalarını ortaya çıkarmaya kapı açıyor.
Atıf: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Anahtar kelimeler: proteom çözünürlüğü, kütle spektrometrisi, proteazom inhibitörü MG132, SUMOylasyon inhibitörü ML-792, protein durum geçişleri