Clear Sky Science · tr
Çekirdek-kabuk lipit nanoparçacıklarının tasarlanmış iç mimarisi, etkili mRNA endozomal salınımını teşvik ediyor
Bu yeni teslimat yöntemi neden önemli
COVID-19 aşılarından deneysel kanser tedavilerine kadar en heyecan verici yeni ilaçların birçoğu haberci RNA, yani mRNA’dan üretiliyor. Ancak inatçı bir sorun var: bu hassas zincirler hücrelerimize girdiklerinde çoğu, endozom adı verilen küçük iç veziküllerde sıkışıp yok oluyor. Bu çalışma, mRNA taşıyan küçük yağ kabarcıkları olan lipit nanoparçacıklarını zekice bir şekilde yeniden tasarlıyor. İç yapısını katı bir altın çekirdek etrafında yeniden düzenleyerek, araştırmacılar mRNA’nın hücrenin çalışma alanına—yani gerçekten işe yarayan proteinleri üretebileceği yere—kaçma oranını dramatik biçimde artırıyor.
Minik kurye parçacıklarına daha iyi bir vücut planı vermek
Mevcut mRNA aşıları ve tedavileri çoğunlukla mRNA’yı saran, yağ karışımından oluşan yumuşak, düzensiz parçacıklara dayanıyor. Teoride, bu parçacıklardaki özel “iyonize olabilen” lipitler endozomların asidik iç ortamında pozitif yüke dönüşüp endozomal membranı yırtarak mRNA’yı serbest bırakmalı. Pratikte ise mRNA’nın negatif yükü bu etkinin büyük bir kısmını dengeliyor; böylece teslim edilen mRNA’nın yalnızca yaklaşık %2’si hücrenin protein yapım makinelerine ulaşabiliyor. Yazarlar basit ama güçlü bir soru sordular: Ya sadece yağların kimyasını değiştirmek yerine parçacığın iç mimarisini yeniden tasarlayıp mRNA ile lipitlerin birbirlerine göre nerede konumlandığını kontrol etselerdi?
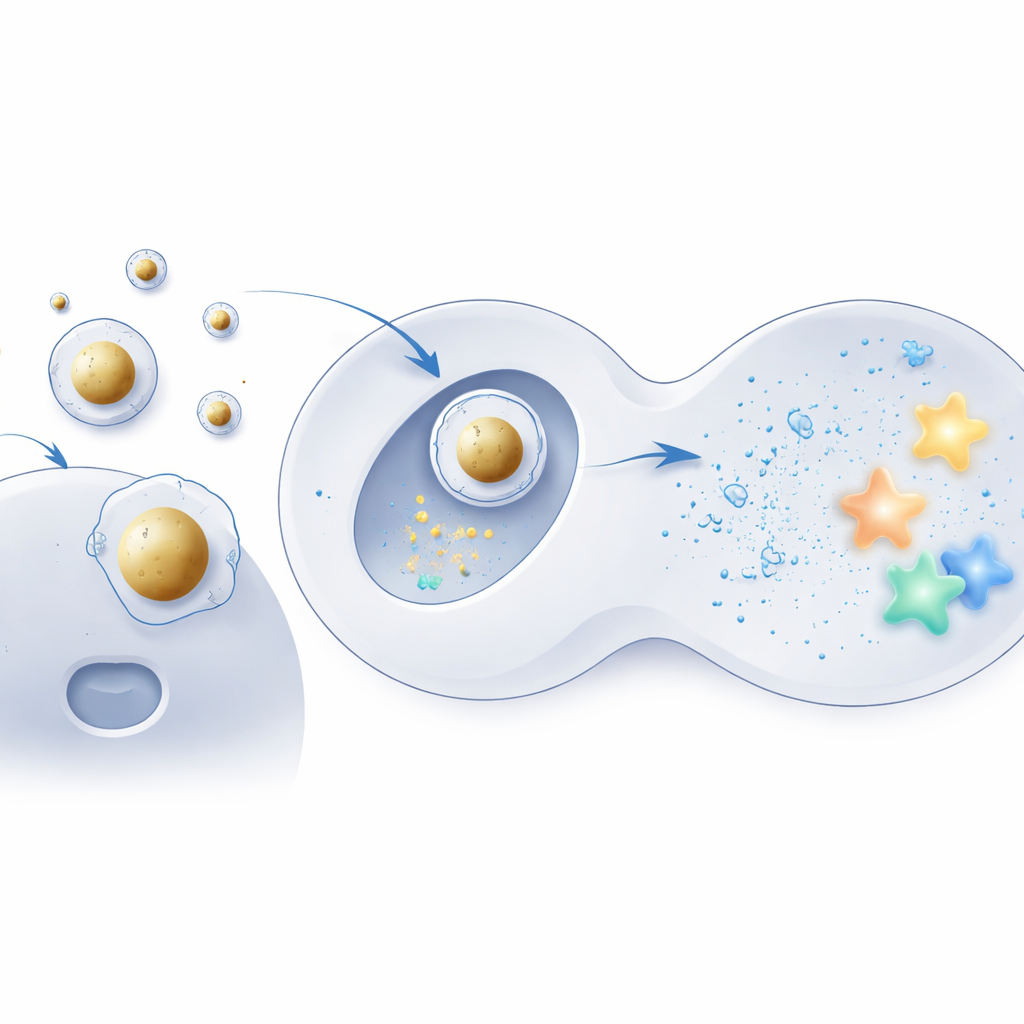
Altın merkezli bir teslimat kabuğu inşa etmek
Bu fikri test etmek için ekip, sert çekirdekler olarak küçük altın küreler kullandı ve bunları konvansiyonel formülasyonlarda kullanılan aynı iyonize olabilen lipitlerle kapladı. Negatif yüklü mRNA ilk olarak bu çekirdeklere kondense edildi ve ancak ondan sonra montaj, yardımcı yağlar ve stabilizatör moleküllerin tanıdık bir karışımıyla sarılarak düzenli bir çekirdek–kabuk yapısı oluşturuldu. Elektron mikroskobu ve bilgisayar simülasyonları bu “Au‑LNP”lerin oldukça uniform, termodinamik olarak kararlı ve sulu, vücut benzeri koşullarda şekillerini iyi koruduklarını gösterdi. Önemli olarak, bunların toplam yağ bileşimi standart parçacıklarla aynı kaldı; böylece temel değişiklik malzemeler değil, iç yapı olarak izole edildi.
Yeniden düzenlenmiş bir iç mekan kaçışı nasıl artırıyor
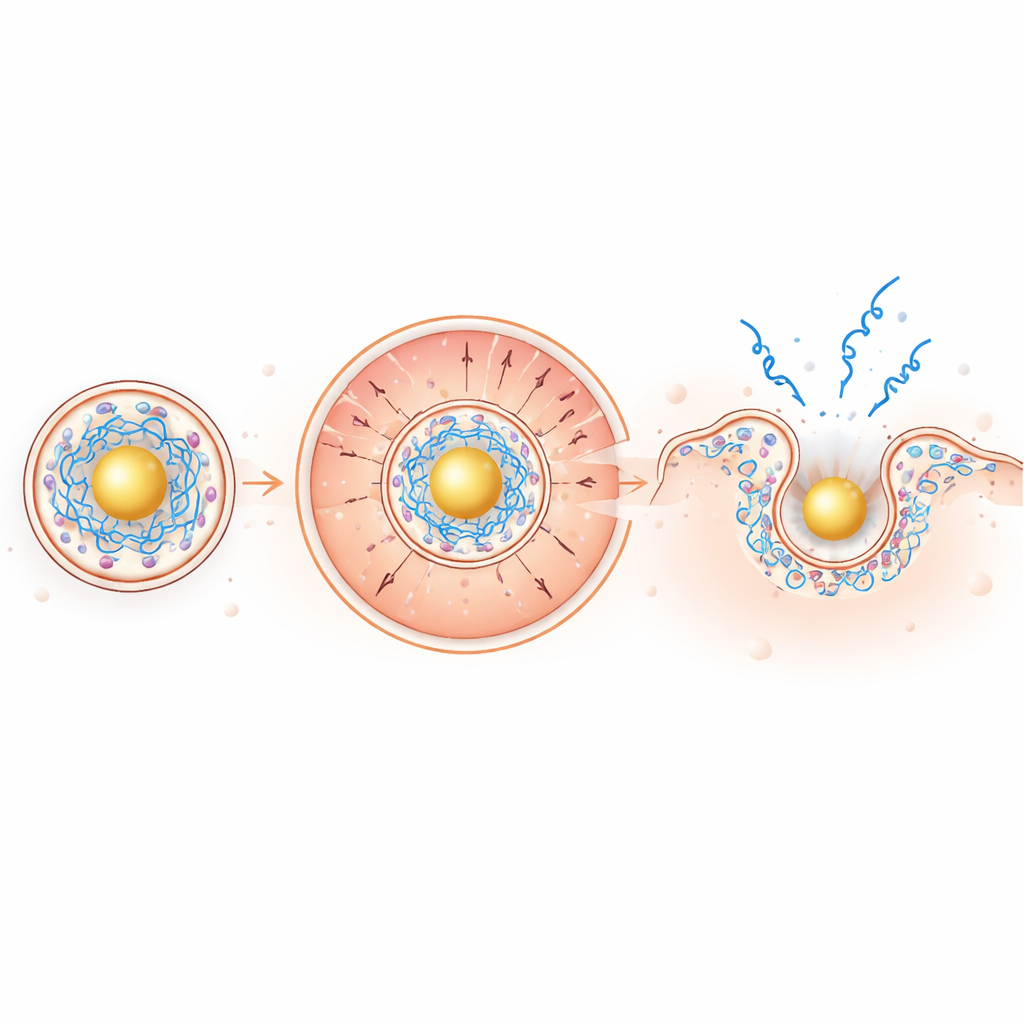
Hafif asidik endozomal ortam içinde, altın bazlı çekirdek güçlü şekilde pozitif hale gelip negatif yüklü mRNA’yı içe doğru çekerken iyonize olabilen pozitif lipitleri çevreleyen zaraya doğru dışa itiyor. Bu yük kaynaklı ayrışma, zararıveren lipitleri tam olarak ihtiyaç duyulan yere yoğunlaştırıyor. Model membran testlerinde ve kırmızı kan hücrelerinde, yeni parçacıklar düşük pH’ta membranları delmede daha etkili olurken nötr pH’ta sessiz kalıyorlardı; bu, arzu edilen bir güvenlik özelliği. Canlı hücrelerde floresan mRNA görüntülemeleri, endozomal kaçışta yaklaşık iki kat artış ve mRNA’nın sitoplazmada yayılmasında geleneksel parçacıklara kıyasla şaşırtıcı bir ~100 kat artış gösterdi.
Hücre kültürlerinden farelere: daha güçlü sinyaller ve daha iyi koruma
Bu fiziksel avantajlar gerçek biyolojik kazanımlara dönüştü. Birkaç hücre tipinde, altın çekirdekli parçacıklar, özellikle düşük dozlarda, standart formülasyonlara göre raporör protein üretimini çok daha yüksek düzeylere çıkardı. Farelerde, kas veya damar içine enjeksiyonlardan sonra mRNA yönlendirmeli protein üretimini beş ila yedi kata kadar artırdılar; parçacıkların vücutta biriktiği yerleri değiştirmeden. SARS‑CoV‑2 spike mRNA aşısı tesliminde, yeniden tasarlanmış parçacıklar ilk enjeksiyondan sonra antikor düzeylerini yaklaşık iki katına çıkardı ve bir güçlendirici sonrası daha da artırdı; aynı zamanda daha güçlü virüs nötralize edici antikorlar üretti. Zorlu bir triple-negatif meme kanseri modelinde, yeni parçacıklarla taşınan mRNA kanser aşıları tümörleri daha etkili küçülttü, tümör aktivite sinyallerini azalttı ve belirgin şekilde sağkalımı uzattı.
Güvenlik ve gelecekteki ilaçlara giden yol
Çekirdeklerinde altın kullanılmasına rağmen parçacıklar farelerde iyi tolere edildi gibi göründü. Vücut ağırlıkları, iltihap belirteçleri ve doku incelemeleri ciddi bir toksisite göstermedi ve organlardaki altın seviyeleri iki gün içinde tekrar başlangıç düzeyine yaklaştı. Yazarlar altının esasen bir kavram kanıtı iskeleti olarak hizmet ettiğini vurguluyor: aynı iç tasarım ilkesi diğer güvenli veya biyobozunur malzemelere uygulanabilir. Uzman olmayanlar için merkezi mesaj, mRNA’yı küçük taşıyıcısına nasıl paketlediğimizin, onunla ne koyduğumuz kadar önemli olabileceğidir. Lipit nanoparçacıklarına daha disiplinli bir iç düzen vererek, bu çalışma mRNA teslimatındaki uzun süredir devam eden bir darboğazı aşmanın yeni bir yolunu sunuyor—bulaşıcı hastalıklar, kanser ve ötesi için daha etkili aşılar ve terapiler açığa çıkıyor.
Atıf: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Anahtar kelimeler: mRNA teslimatı, lipit nanoparçacıklar, endozomal kaçış, nanotıp, RNA aşıları