Clear Sky Science · tr
Hedefe yönelik ve epigenetik temelli birleşik tedavi, pankreatik duktal adenokarsinomda GATA6-bağımlı MHCI ekspresyonunu stabilize ederek antitumör bağışıklığı güçlendiriyor
Bu araştırma pankreas kanseri için neden önemli
Pankreatik duktal adenokarsinom, bağışıklıktan saklanması ve birçok ilaca direnç göstermesi nedeniyle en ölümcül kanserlerden biridir. Bu çalışma, pankreas kanseri hücrelerini immün saldırıya daha açık hâle getiren GATA6 adlı bir gen tarafından yönlendirilen özgül bir tümör hücre durumunu ortaya koyuyor. Yazarlar ayrıca iki ilaç sınıfını birleştirmenin bu savunmasız durumu koruyabileceğini ve deneysel modellerde öldürücü T hücrelerinin tümörlere saldırma yeteneğini artırabileceğini gösteriyor.
Bağışıklık sistemini davet eden bir tümör hücre durumu
Tüm pankreas kanseri hücreleri aynı davranmaz. Bazıları daha düzenli, epitel benzeri bir kimliği korurken diğerleri daha hareketli ve agresif, mezenkimal-benzeri bir duruma kayar. Transkripsiyon faktörü GATA6 epitel kimliğinin korunmasına yardımcı olur ve hastalarda daha iyi sonuçlarla ilişkilidir. Büyük hasta kohortlarında, yüksek GATA6 seviyelerine sahip tümörlerde az veya hiç GATA6 içermeyen tümörlere kıyasla daha fazla immün hücre, özellikle CD8 “öldürücü” T hücresi bulunuyordu. İnsan tümör örnekleri üzerinde yapılan gelişmiş uzamsal görüntüleme, GATA6-pozitif kanser hücrelerinin CD8 T hücrelerinin yanında daha sık yer aldığını ve hücre içeriğini T hücrelerine gösteren bir işaretçi gibi davranan MHCI molekülünün daha yüksek düzeylerini sergilediğini ortaya koydu. Bu gözlemler GATA6'nın bağışıklık sistemi tarafından doğal olarak daha görünür bir tümör hücre popülasyonunu işaret ettiğini düşündürdü. 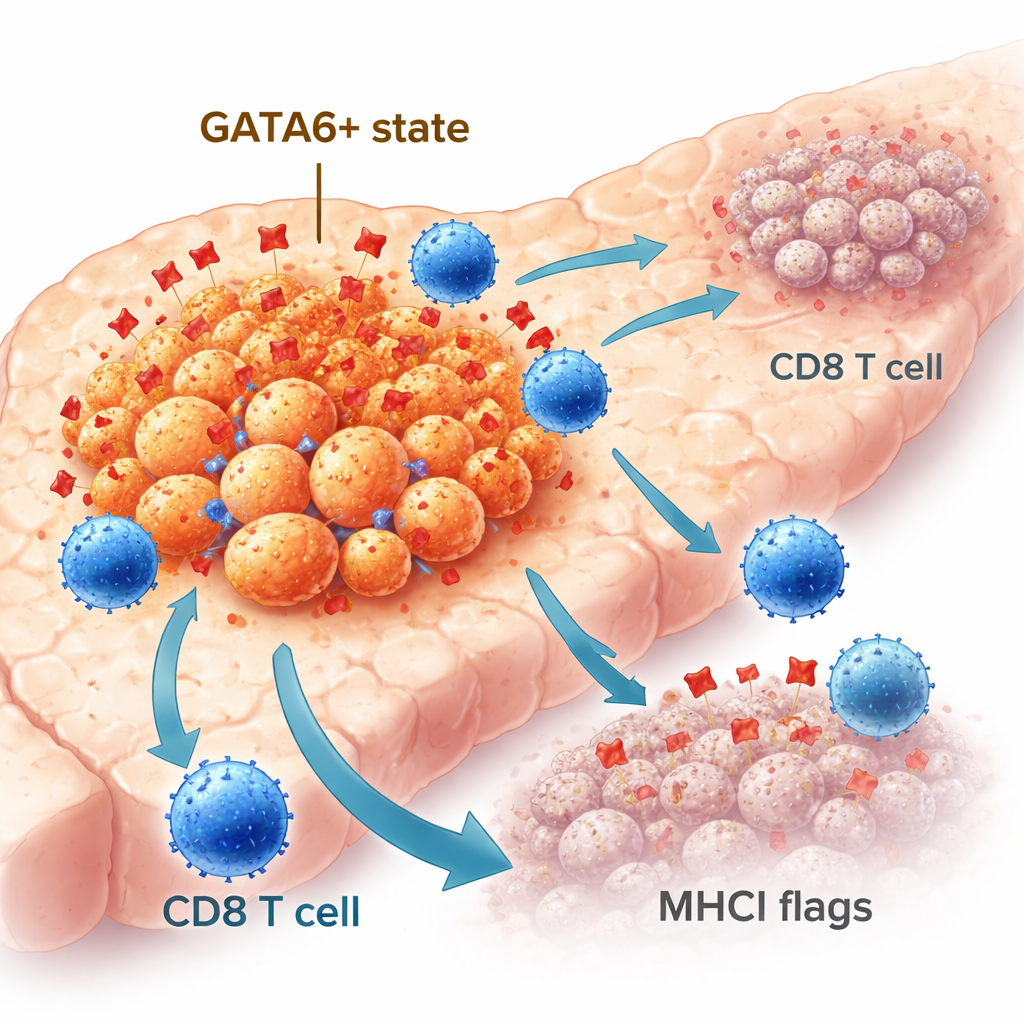
Tümör görünürlüğünü artıran hedefe yönelik terapi—ama bir bedeli var
Ekip, hedefe yönelik ilaçların bu görünürlüğü daha da artırıp artırmayacağını araştırdı. Pankreas kanserinde sıkça aktif olan bir büyüme sinyal yolunu engelleyen bir ilaç sınıfı olan MEK inhibitörlerine odaklandılar. Fare pankreas kanseri hücre hatlarında, farelerde büyütülen tümörlerde ve hasta kökenli ksenogreftlerde MEK inhibisyonu, GATA6-yüksek tümör hücrelerinin yüzeyinde MHCI düzeylerini artırarak bunları T hücreleri için potansiyel olarak daha iyi hedefler hâline getirdi. Farelerde GATA6-yüksek tümörler MEK inhibitörleriyle tedavi edildiğinde tümör büyümesi yavaşladı, MHCI arttı ve sitotoksik moleküller taşıyan daha fazla CD8 T hücresi tümörlere girdi. GATA6'nın gen knockout'u veya proteinin hızlı bir şekilde degradasyona uğratılması yoluyla doğrudan bloke edilmesi, MEK inhibitörünün neden olduğu bu MHCI artışını ve ortaya çıkan tümör kontrolünü ortadan kaldırdı; bu da GATA6'nın bu faydalı etki için vazgeçilmez olduğunu gösterdi.
Tümörlerin nasıl uyum sağladığı: öldürülmesi daha zor bir duruma kayış
Ancak hikâyede bir ters köşe vardı. Uzun süreli MEK inhibitörü tedavisi, birçok tümör hücresinin GATA6-pozitif epitel durumundan tedavi direnciyle ilişkili daha mezenkimal, GATA6-düşük bir duruma kaymasına yol açtı. Hem fare modellerinde hem de hasta kökenli ksenogreftlerde MEK inhibitörü ile tedavi edilen tümörler sonunda daha az GATA6-pozitif hücre, daha fazla epitelden-mezenkimale geçiş işareti ve genel olarak daha az kalıcı fayda gösterdi. Bireysel GATA6-pozitif hücreler hâlâ ilaca yanıt olarak MHCI'yi yukarı düzenlese de, bu popülasyonun küçülmesi tümör antijen sunumundaki genel iyileşmeyi sınırladı; bu da MEK inhibitörlerinin pankreas kanseri klinik deneylerinde tek başına neden hayal kırıklığı yarattığını açıklamaya yardımcı oldu.
Tümörleri savunmasız durumda tutan epigenetik ilaçlar
Bu uyum kaçışına karşı koymak için araştırmacılar, hücre kimliğini ve immün görünürlüğü etkilediği bilinen bir epigenetik ilaç sınıfı olan histon deasetilaz inhibitörlerine (HDAC inhibitörleri) yöneldi. Hücre kültürlerinde ve fare modellerinde, MEK inhibitörleri ile sınıf I HDAC inhibitörleri (örneğin domatinostat) kombinasyonu, MEK inhibitörleri tarafından baskılanmış olan GATA6 ekspresyonunu geri getirdi, epitelden-mezenkimale geçiş işaretlerini tersine çevirdi ve tümör hücrelerinde MHCI düzeylerini daha da artırdı. Önemli olarak, bu kombinasyon terapisi ortotopik fare tümörlerinde ve insan pankreas kanserini yakından taklit eden genetik olarak tasarlanmış fare modelinde CD8 T hücrelerinin infiltrasyonunu ve aktivasyonunu güçlendirdi ve daha fazla tümör hücresi ölümü sağladı. CD8 T hücrelerinin azaltılması faydanın büyük bir kısmını ortadan kaldırdı; bu da kombinasyonun esasen öldürücü T hücreleri güçlendirerek etki ettiğini doğruladı.
Zorlu bir kanser için daha akıllı kombinasyon terapilerine doğru
Bu bulguları bir araya getiren çalışma, hedefe yönelik MEK inhibisyonu ile epigenetik HDAC inhibisyonunun birlikte kullanılarak MHCI bakımından zengin ve dolayısıyla bağışıklık sistemi tarafından yüksek derecede tanınabilir bir GATA6 kaynaklı tümör hücre durumunu stabilize etme stratejisini öneriyor. Hem GATA6-pozitif hücre sayısını artırarak hem de bu hücrelerin MHCI “bayraklarını” güçlendirerek kombinasyon, agresif fare pankreas kanseri modellerinde daha derin CD8 T hücresi infiltrasyonu, daha güçlü sitotoksik aktivite ve daha uzun sağkalım sağlıyor. HDAC inhibitörlerinin önemli yan etkileri olabileceği ve bu çalışmanın preklinik olduğu halde, bu araştırma yol hedefleyen ilaçlar ile dikkatle seçilmiş epigenetik modifiye edicilerin eşleştirilerek pankreas tümörlerini vücudun kendi bağışıklık savunmalarına karşı daha savunmasız hâle getirme yönünde gelecek tedavi yaklaşımlarına işaret ediyor. 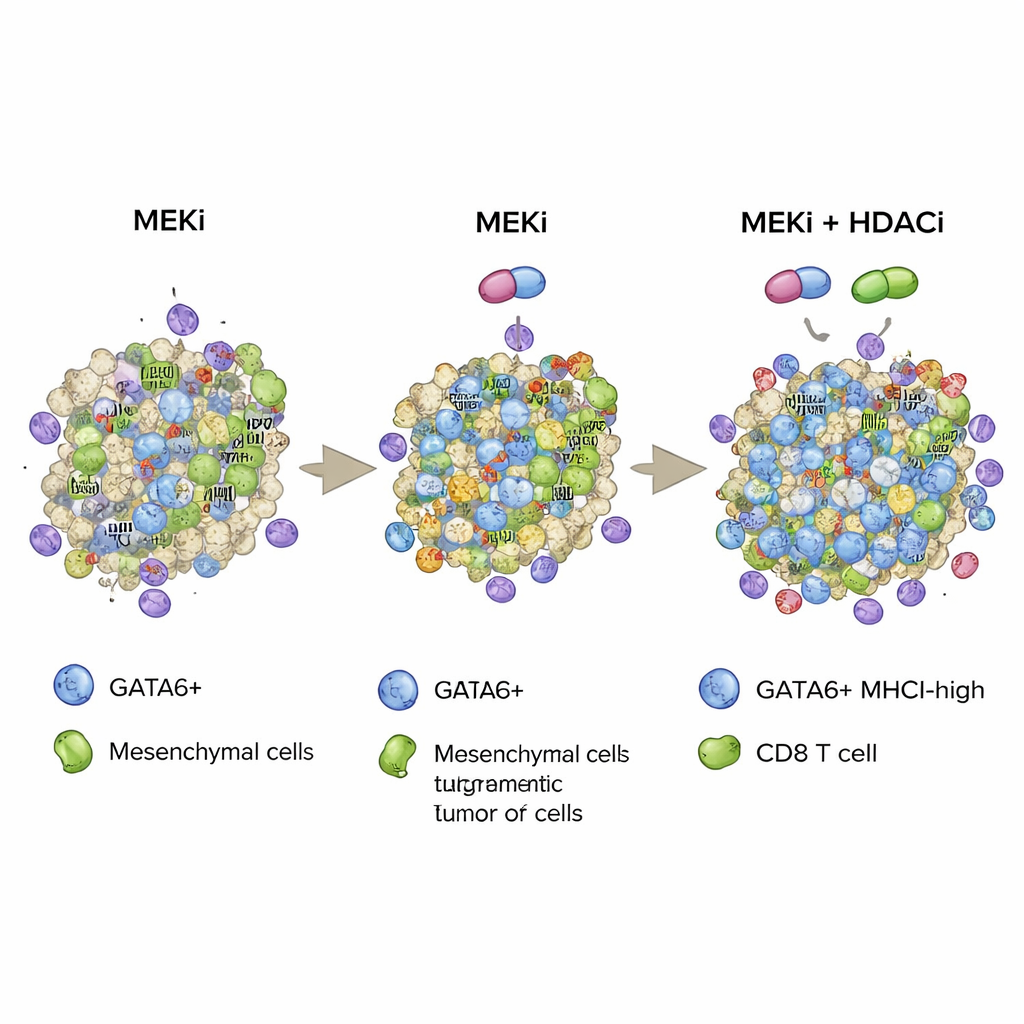
Atıf: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Anahtar kelimeler: pankreas kanseri, tümör bağışıklığı, GATA6, MEK inhibitörü, HDAC inhibitörü