Clear Sky Science · tr
Hiyerarşik biyofarmasötikler oluşturmak için yerinde ve dinamik değişim stratejileriyle çok bileşenli sinerjistik immobilizasyon
Daha Akıllı İlaçlar Geliştirmenin Neden Önemli Olduğu
Bugünün en etkili ilaçlarından çoğu, proteinler ve enzimler gibi büyük, hassas biyolojik moleküllerdir. Kanserle savaşabilir, zararlı bakterileri öldürebilir ve iyileşmeyi hızlandırabilirler; ancak kolayca zarar görürler ve vücudun doğru yerine taşınmaları zordur. Bu makale, bu tür narin bileşenlerin birkaçını koruyucu, süngerimsi bir materyal içine birlikte “paketlemenin” yeni bir yolunu anlatıyor; böylece ardışık şekilde daha güçlü etki gösterip yan etkileri azaltabiliyorlar.
Bir Kristali Moleküler Bir Apartman Binasına Dönüştürmek
Araştırmacılar metal iyonları ve küçük organik yapı taşlarından yapılan özel bir gözenekli materyalle başlıyorlar. Bu malzeme, odalar ve koridorlarla dolu küçük, esnek bir apartman binası gibi davranıyor. Çalışma, zeolitik pirimidin çerçevesi adı verilen bu iskeletin proteinlerin etrafında büyütülebileceğini ve böylece proteinlerin kristalin içinde korunmuş olarak kaldığını gösteriyor. Bu "yerinde" kapanma proteinleri ezmiyor veya etkisizleştirmiyor; hassas görüntüleme, proteinlerin binanın her katında yaşayan kiracılar gibi iç mekan boyunca dengeli şekilde dağıldığını doğruluyor.
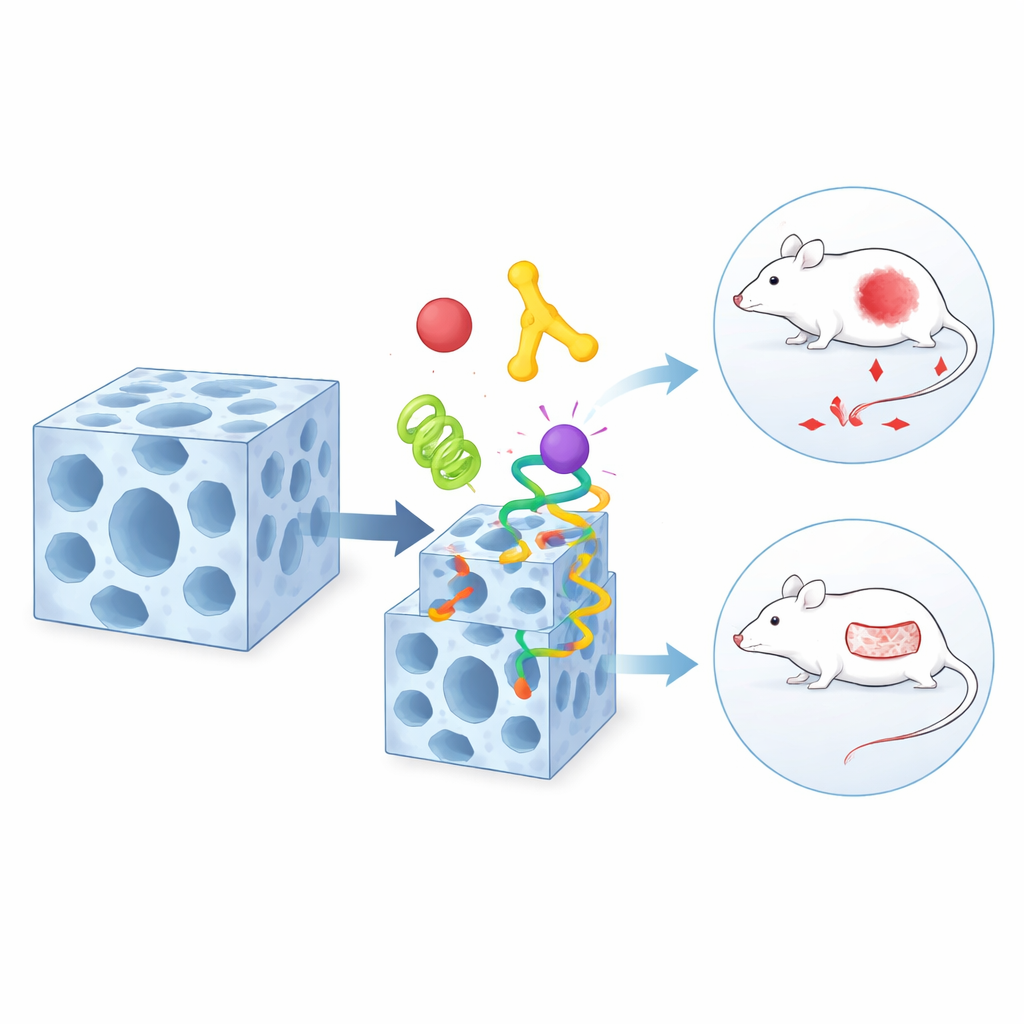
Yüzey Süslemesi İçin Şekil Değiştiren Bir Ev Sahibi
Aynı materyalin şaşırtıcı bir ikinci özelliği daha var: belirli çözücülere veya suya maruz kaldığında iç yapısını geri dönüşümlü olarak değiştirebiliyor. Bu nazik şekil değişimi sırasında iskeletteki bazı kimyasal bağlar gevşiyor ve sonra yeniden oluşuyor. Ekip, protein yüzeylerindeki belirli kimyasal grupların—bazı amino asitlerde bulunanlar gibi—bu zayıflık anından faydalanabildiğini keşfetti. Geçici olarak çerçevenin orijinal yapı taşlarıyla yarışıp yüzeye yakın yeni oluşan "kusurlara" sızıyorlar. Sonuç olarak, proteinlerden oluşan bir katman esasen kristalin dışına sabitlenirken içtekiler yerinde kalıyor. Bu dinamik değişim süreci, bilim insanlarının hangi bileşenlerin derinlerde, hangilerinin dış kabuğu süsleyeceğine karar vermesine olanak tanıyor.
Enzim Montaj Hatları Tasarlamak
Hem iç hem dış alanlar kontrol altına alındığında, yazarlar küçük enzimatik "montaj hatları" kuruyorlar. Bir örnekte, şekeri saldırgan bir ara ürüne dönüştüren bir enzim çerçevenin içine kilitlenirken, o ara ürünü güvenli şekilde parçalayacak ikinci bir enzim yüzeye yakın konumlandırılıyor. Bu iç-dış düzenleme, reaksiyonun geleneksel çekirdek-kabuk tasarımlarından veya rastgele enzim karışımlarından daha hızlı ve verimli çalışmasını sağlıyor. Dıştaki enzimler moleküller tarafından daha kolay ulaşılabilir olduğundan ve zararlı ara ürün hızlıca uzaklaştırıldığından, sistem birçok döngü boyunca aktif kalıyor ve ısıya, zorlu koşullara ve tekrarlı kullanıma daha iyi dayanıyor.
Akıllı Anti-Kanser ve Anti-Bakteriyel Paketler
Bu yaklaşımın gerçek gücü tıbba uygulandığında ortaya çıkıyor. Ekip, tek katmanlı bir partikülde tümör hedefleyen bir protein, glikozu tüketen bir enzim ve standart bir kemoterapi ilacını bir araya getiriyor. Yüzeydeki hedefleme bileşeni partikülü kanser hücrelerine yönlendiriyor, enzim yerel şekeri tüketerek hücrelerin enerji kaynağını boşaltıyor ve küçük moleküllü ilaç ek bir öldürücü darbe indiriyor. İnsan tümör implantlı farelerde bu üç parçalı paket, bileşenlerin tek başına veya daha basit düzenlenmiş karışımlardan çok daha etkili şekilde tümörleri küçültüyor. Ayrı bir tasarımda, yazarlar iskeleti enfekte deri yaraları için uyarlayarak antibakteriyel bir peptidi ve doku onarımını destekleyen bir enzimi aynı taşıyıcı içinde farklı bölgelere yerleştiriyorlar. Sıçan modellerinde bu partiküller enfeksiyonu önemli ölçüde azaltıyor ve zorlu yaraların kapanmasını geleneksel tedavilere kıyasla hızlandırıyor.

Bu Çalışma Tıbbı Nasıl İleri Taşıyor
Uzman olmayan bir okuyucu için temel mesaj şu: bu çalışma tek bir gözenekli kristali çok çeşitli terapötik moleküller için programlanabilir bir yuva haline getiriyor. Kimlerin içerde, kimlerin yüzeyde yaşayacağına ve hangi oranda bulunacaklarına karar vererek, araştırmacılar bir küçük nesne içinde aşamalı tedavileri—önce hedefleme, sonra saldırı, sonra onarım—koordine edebiliyor. Bu strateji yalnızca hassas biyolojik ilaçları korumakla kalmıyor, aynı zamanda onların birbirlerine yardımcı olmasına izin vererek daha güçlü, daha hassas anti-kanser ve anti-bakteriyel tedavilere yol açıyor. Aynı tasarım ilkeleri, birden çok bileşenin doğru zamanda ve doğru yerde birlikte çalışmasını gerektiren geleceğin "akıllı ilaçlarına" uyarlanabilir.
Atıf: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Anahtar kelimeler: metal-organik çerçeveler, enzim immobilizasyonu, kanser nanomedisini, yaraların iyileşmesi, biyofarmasötik taşıma