Clear Sky Science · tr
Hücresel dış ortam, üçlü negatif meme kanseri metastazında dolaşımdaki tümör hücresi kümelenmesini sağlar
Huyarsız Meme Kanseri Hücreleri Kan Dolaşımında Nasıl Takım Kuruyor
Meme kanseri yayıldığında, sıklıkla bunun nedeni gevşek kanser hücrelerinin kana kaçıp uzak organlarda tümör tohumlamasıdır. Bu çalışma, görünüşte basit ama etkisi büyük bir soruyu soruyor: normalde birbirine yapışmak için kullandıkları “cırt”ı kaybetmiş en saldırgan meme kanseri hücreleri, yine de nasıl sıkı kümeler halinde seyahat edebiliyor—ve bunun onları neden daha ölümcül kıldığı nedir?
Klasik Hücre Yapıştırıcısının Yerine Geçen Yapışkan Bir Şeker Kılıf
Yazarlar, özellikle agresif olup sıklıkla dolaşımdaki tümör hücreleri (CTC) salgılayan üçlü-negatif meme kanseri (TNBC) üzerine odaklanıyor. Birçok kanser türünde, CTC kümeleri tekil hücrelere göre çok daha yüksek oranda metastaz oluşturur. Tipik olarak bu kümeler, komşu hücreler arasında moleküler perçinler gibi görev yapan epitel adezuer bağlantıları tarafından bir arada tutulur. Ancak TNBC hücreleri sıklıkla bu bağlantı proteinlerini kaybeder; bu da bir paradoks yaratır: alışılmış yapıştırıcı yokken kümeleri ne tutuyor? Büyük kanser gen veri tabanlarını tarayarak, araştırmacılar TNBC tümörlerinin hücrenin dış iskeleti olarak bilinen ekstraselüler matriksle ilişkili genler bakımından zenginleştiğini buldular. Öne çıkan genlerden biri HAS2 idi; bu gen, hücreleri kaplayan uzun, şekerli bir polimer olan hiyaluronan (HA) üreten enzimi yapar. Yüksek HAS2 ve HA düzeyleri, agresif, metastatik tümör özellikleriyle güçlü bir şekilde ilişkilendirildi.
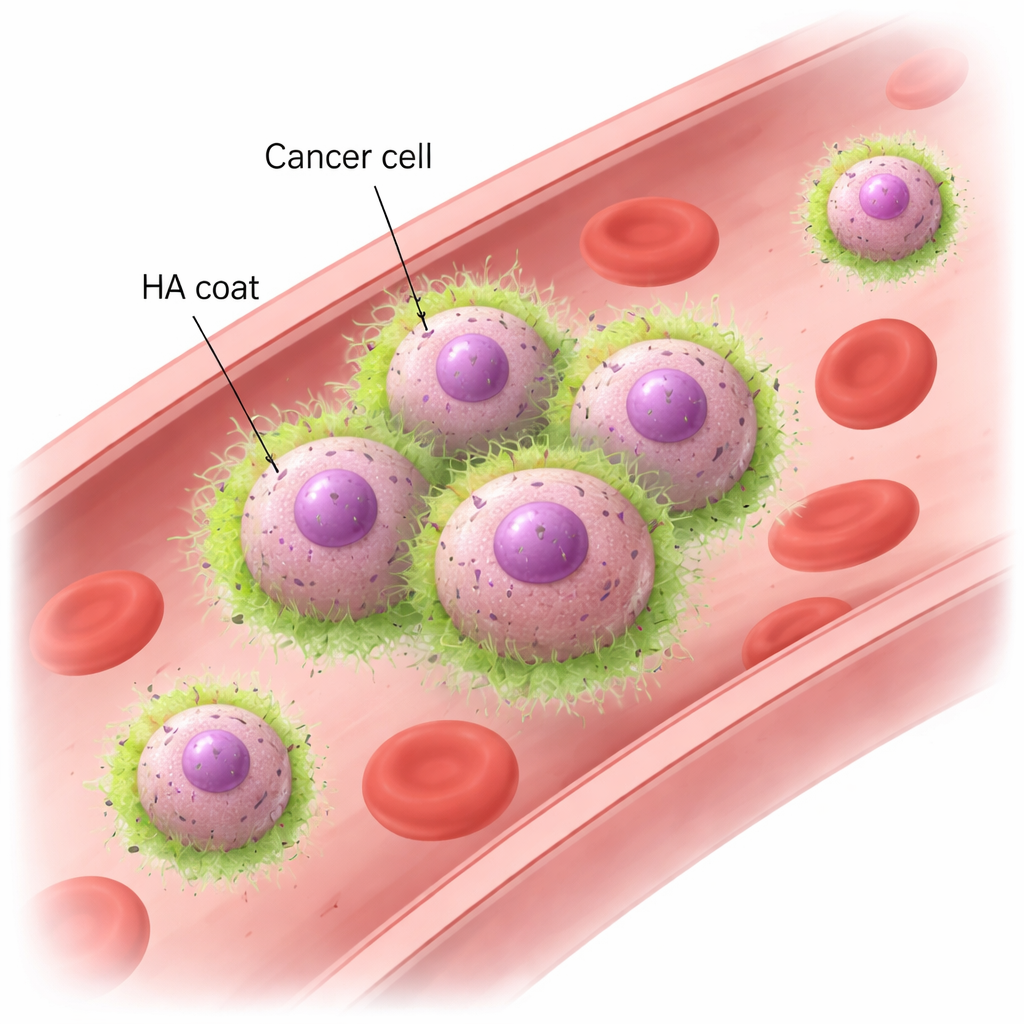
Hiyaluronan ve CD44: Hücrelerin El Ele Tutunmasının Yeni Bir Yolu
Fare modelleri ve insan meme kanseri hücre hatları kullanarak ekip, metastatik TNBC hücrelerinin kan akımını taklit eden dönen bir sıvıya maruz kaldıklarında hızla kümeler oluşturduğunu gösterdi. Bu kümeler gerçek kan damarlarındaki kuvvetlere benzer koşullar altında bile sağlam kalırken, daha az agresif meme kanseri hücreleri parçalanıp tek tek sürüklendi. Mikroskopi, metastatik hücrelerin bir HA “kılıfı” ile sarıldığını ve bu kılıfın hücrelerin birbirine değdiği yerlerde yoğunlaştığını ortaya koydu. HA’yı enzimlerle kaldırmak ya da HAS2’yi baskılamak, hücrelerin akış altında kümelenme yeteneğini kaybetmesine yol açtı; oysa hücreler rahatsız edilmeden bırakıldıklarında yine birlikte çökelip bir arada durabiliyordu. Hücre tarafındaki ana ortak CD44’tü; HA’ya bağlanan yaygın bir yüzey reseptörüdür. CD44 eksik hücreler artık yüzeylerinde HA tutamıyor ya da küme oluşturamıyordu. Tersine, hem HAS2 hem de CD44 üretecek şekilde genetik olarak değiştirilmiş kümelenmeyen hücreler güçlü bir kümelenme yeteneği kazandı. Bu deneyler, HA ile CD44 etkileşiminin kan gibi hızlı hareket eden akışlarda kanser hücrelerinin birbirine yapışması için gerekli ve yeterli olduğunu gösterdi.
İnce Çıkıntılar ve Mekanik Kilitler Güçlü Kümeler İnşa Ediyor
Yüksek çözünürlüklü görüntüleme, kümelerin nasıl oluştuğuna dair fiziksel koreografiyi ortaya çıkardı. Tekil TNBC hücreleri, CD44 ile kaplı ve uçları HA ile süslü çok sayıda ince, aktin-temelli zar çıkıntıları—adeta duyu organları—uzatıyor. İki hücre birbirine yaklaştığında, her bir hücrenin bu çıkıntıları ilk olarak karşılaşıp başlangıçta HA–CD44 köprüleri oluşturuyor. Zamanla, çıkıntılar birbirinin yanında kayarak tüm hücre gövdelerini daha da yakınlaştırıyor ve membranların geniş alanlarının neredeyse yan yana yatmasına kadar çekiyor. Bu süreç, normal epitel hücrelerinin adezyon bağlantıları kurma biçimini yansıtıyor, ancak burada sert protein zincirleri yerine esnek bir şeker kılıfı bunu sağlıyor. Temas bölgesi olgunlaştıkça başka yapılardan oluşan bir set devreye giriyor: sitoplazmik iskelete bağlanan sağlam bağlantılar olan desmozomlar. Desmozomal proteinler yalnızca HA tabanlı temas kurulduktan sonra birikiyor ve kümelerin kan akımının yırtıcı kuvvetlerine karşı direncini artıran mekanik “kilitler” görevi görüyor. Desmozom bileşenleri azaltıldığında, kümeler oluşsa da daha yüksek kayma geriliminde parçalanıyordu.
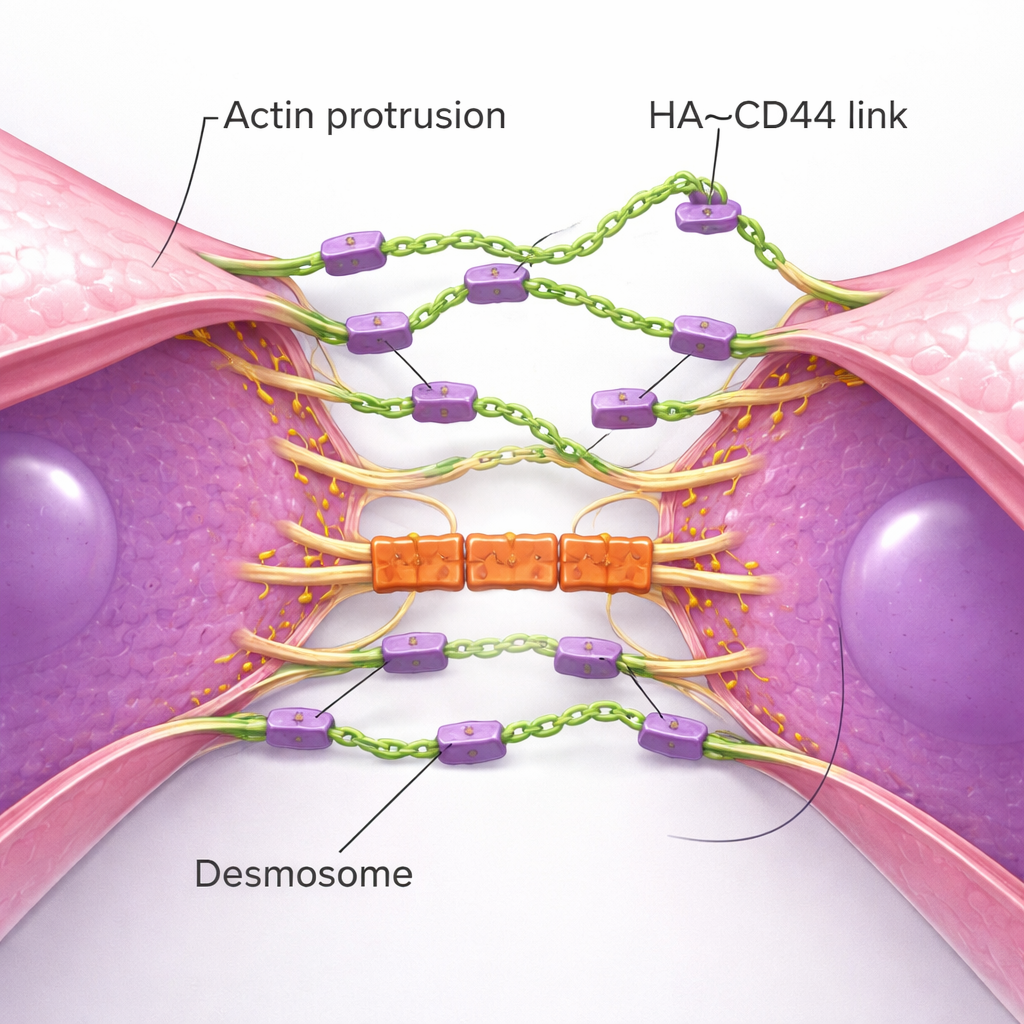
Kümelenmenin Hayatta Kalma ve Metastaz İçin Önemi
HA tabanlı kümelenme sistemi sadece birlikte kalmanın bir yolu olmaktan öte, doğrudan hayatta kalmayı artırıyordu. Uzun süreli simüle edilmiş kan akımı altında, HA açısından zengin kümeler, HA’sı azaltılmış tek hücrelere göre çok daha düşük düzeyde zararlı reaktif oksijen türleri gösterdi ve çok daha az hücre ölümü yaşadı. Fare modellerinde, HAS2 eksik TNBC hücreleri çok daha az CTC üretti, yalnızca küçük kümeler oluşturdu ve akciğer metastazı dramatik biçimde azaldı—oysa primer tümörleri aynı oranda büyüyordu. Kontrol ve HAS2-eksik hücrelerin önceden oluşturulmuş kümeleri farelere enjekte edildiğinde, HA fakiri hücreler akciğerleri koloniye dönüştürmede çok daha başarısız oldu. Dahası, HA kaplı CTC’ler, diğer hücreleri—HA’sı olmayan kanser hücrelerini ve nötrofiller gibi normal bağışıklık hücrelerini bile—CD44 ifade ettikleri sürece karışık kümelere “çağırabiliyordu.” Metastatik TNBC’li kadınlardan alınan hasta kan örnekleri aynı deseni gösterdi: CTC’ler sıkça bir HA kılıfı taşıyor ve HA, tümör hücreleri arasındaki ve tümör ile tümör-dışı hücreler arasındaki temas noktalarında zenginleşiyordu.
Hastalar ve Gelecek Tedaviler İçin Anlamı
Uzman olmayan bir kişi için çıkarılacak ana sonuç şu: en öldürücü meme kanseri hücrelerinin bazıları tek başına değil, klasikten farklı olarak dışlarında şekerli bir kılıf ve onun reseptörü tarafından değil de klasik doku içi “perçinler” tarafından değil tutulan küçük, işbirlikçi takımlar halinde yolculuk yapıyor. Bu HA–CD44 tabanlı mekanizma, tümör hücrelerinin zorlu kan akımından sağ çıkmasına, birbirleriyle ve destekleyici kan hücreleriyle birleşmesine ve uzak organlarda yeni tümörler oluşturma verimliliğini artırmasına yardımcı oluyor. HA üretimini hedeflemek (örneğin HAS2’yi inhibe ederek) ya da HA ile CD44 etkileşimini engellemek teoride bu kümeleri zayıflatabilir ve TNBC’nin metastaz yapmasını zorlaştırabilir; bu da gelecekteki anti-metastatik tedaviler için yeni bir yol sunuyor.
Atıf: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Anahtar kelimeler: üçlü-negatif meme kanseri, dolaşımdaki tümör hücreleri, hiyaluronan, CD44, metastaz