Clear Sky Science · tr
Escherichia coli, nötrofil ekstraselüler ağlar salarak güçlendirilen enhancer-promoter döngülerini sürdürerek kolorektal kanser metastazını teşvik ediyor
Bağırsak Mikropları ve Kanserin Gizli Otoyolu
Kolorektal kanser sıklıkla bağırsaktaki asıl tümörden değil, kanser hücrelerinin karaciğere gidip yerleşmesinden dolayı öldürür. Bu çalışma, o yolculukta beklenmedik bir suç ortakını ortaya koyuyor: yaygın bir bağırsak bakterisi, Escherichia coli. Bağırsaktaki bakterilerden karaciğerdeki agresif tümörlere uzanan olay zincirini izleyerek, araştırmacılar mikrobiler, bağışıklık hücreleri ve kanser hücrelerinin içindeki DNA mimarisinin nasıl birlikte metastazı besleyebileceğini gösteriyor—ve bu zinciri koparmanın yeni yollarını öneriyor.
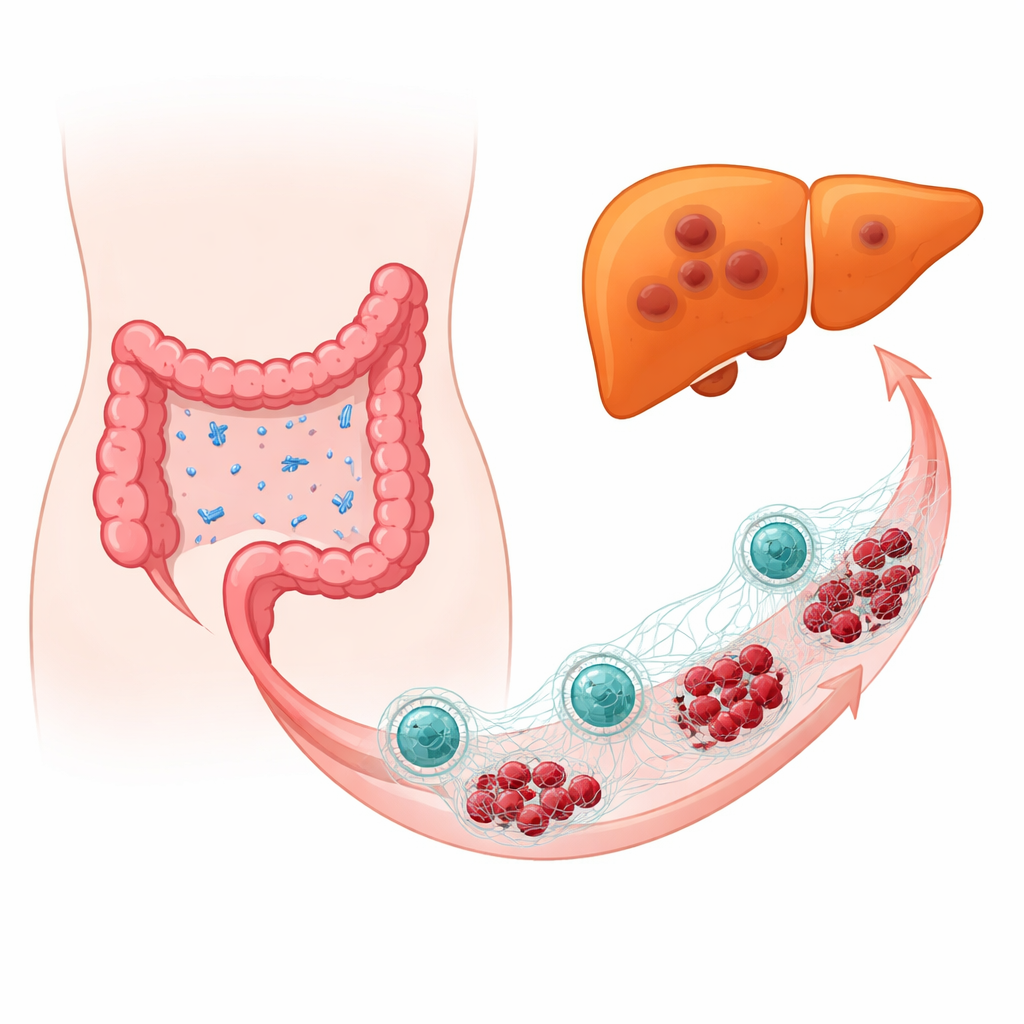
Dost Bakteriler Düşmanca Davranınca
Araştırma ekibi, kolorektal kanseri olan kişilerden alınmış tümör örneklerini, kanseri karaciğere yayılmış olanlarla yayılmamış olanlar arasında karşılaştırdı. Mikrobiyal profillemenin yüksek çözünürlüklü DNA tabanlı yöntemleriyle, E. coli’nin karaciğere tohumlanmış olan kanserlerde çok daha bol bulunduğunu saptadılar. Fare modellerinde ve insan bağışıklık sistemiyle “humanize” edilmiş farelerde, kolorektal tümörlerin yakınına kasıtlı olarak E. coli eklenmesi karaciğer metastazlarını daha büyük ve daha sık hale getirdi ve tümör hücrelerini daha hareketli, invaziv bir duruma itti. Normal bağırsak florasının çoğu antibiyotikle uzaklaştırılıp yalnızca E. coli geri verildiğinde bile bakteriler tümör büyümesini ve yayılmasını artırdı; bu da genel mikrobiyom bozulmasından çok E. coli’nin kendisinin rol oynadığını işaret ediyor.
Bazı Bağışıklık Ağları Kanserin Kaçmasına Yardım Ediyor
Normalde mikropları yakalayıp öldüren ön cephe bağışıklık hücreleri olan nötrofiller, kritik aracılar olarak öne çıktı. E. coli’ye yanıt olarak nötrofiller, DNA ve toksik proteinlerden oluşan ağ benzeri yapılar olan ekstraselüler tuzaklar (NET’ler) saldılar. Bu ağlar bakterileri yakalamak için tasarlanmıştır, ancak bu durumda yanlışlıkla kanser hücrelerini korudu ve güçlendirdi. Araştırmacılar ağları enzimlerle parçaladığında veya bunların oluşumu için gerekli anahtar enzimleri engellediklerinde, karaciğer metastazları küçüldü ve tümörler daha az agresif hale geldi. Nötrofil tükenmesi benzer koruyucu etki gösterdi; bu da paradoksal bir duruma işaret ediyor: enfeksiyonla savaşan bağışıklık yanıtı, kanserin yayılmasına yardım etmek üzere kaçırılmıştı.
Elektrik Sinyallerinden Gen Anahtarlarına
Tümör hücresi dışındaki yapışkan DNA ağları, hücrenin çekirdeği derininde neler olduğunu nasıl değiştirebilirdi? Yanıt, hücrelerde elektrik sinyali gibi görev yapan basit bir iyon olan kalsiyumdaydı. Çalışma, nötrofil ağlarının kolorektal kanser hücrelerinde TRPC1 adlı bir kanal proteinini artırdığını gösterdi. TRPC1 hücreye ekstra kalsiyumun akmasına izin verdi; bu da kalsiyuma duyarlı bir düzenleyici olan NFATC3’ü aktive etti ve TRPC1 düzeylerini yüksek tutan kendini güçlendiren bir döngü oluşturdu. Bu kalsiyum dalgası, iki küçük protein olan S100A8 ve S100A9’un birbirine yapışmasını ve ardından ana büyüme kontrol proteini STAT3’e bağlanmasını teşvik etti. Üçlü çekirdeğe girerek özellikle çarpıcı bir şey yaptı: uzak düzenleyici bölgeler ile gen başlangıç noktalarının temas etmesini sağlayarak DNA’yı büküp döngüleştirdiler; böylece belirli genleri açan “enhancer–promoter döngüleri” fiziksel olarak stabil hale geldi.
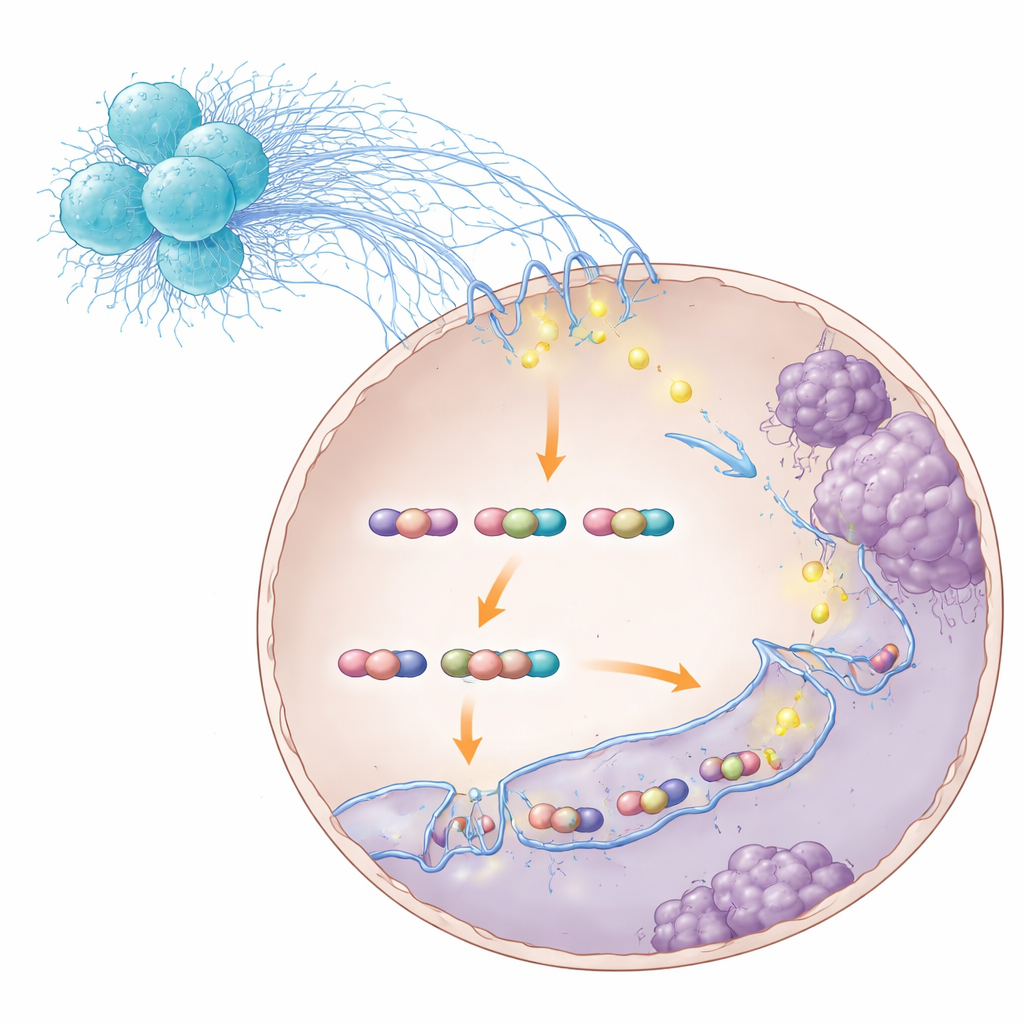
Kanser Hücrelerini Metastaz İçin Yeniden Devreleme
Genom boyunca üç boyutlu temasları haritalayarak, araştırmacılar STAT3–S100A8/9 kompleksinin hareket ve invazyonla ilgili genleri destekleyen döngüleri teşvik ettiğini buldular. Öne çıkan genlerden biri, hücrelerin yapışmalarını gevşetip daha kolay göç etmelerini sağlayan TNS1 idi. STAT3–S100A8/9 kompleksi bozulduğunda, bu döngülerin çoğu zayıfladı veya kayboldu, TNS1 düzeyleri düştü ve kanser hücreleri karaciğere yerleşme yeteneklerinin bir kısmını kaybetti. Önemli olarak, bu bozulma STAT3’ün DNA’ya tamamen bağlanmasını durdurmadı—özellikle metastatik programları aşırı etkinleştiren döngüsel mimariyi istikrarsızlaştırdı. Hayvan modellerinde, bu zincirdeki farklı adımlar—nötrofillerdeki bakteriyel algılayıcı RIPK2’den S100A8/9’a, STAT3’ün kendisine kadar—engellendiğinde karaciğer metastazı azaldı ve sağkalım iyileşti.
Bakteriler ile Tümörler Arasındaki Zinciri Kırmak
Uzman olmayanlar için ana mesaj şudur: yaygın bir bağırsak bakterisi, önce bağışıklık hücrelerini DNA ağları salgılamaya teşvik ederek, sonra bu ağları kalsiyum kaynaklı bir röleyle kullanıp kanser genlerinin nasıl açıldığını yeniden devreleyerek kolorektal kanserin yayılmasına yardım edebilir. Faydalı mikroplara zarar verip kanser immünoterapisini zayıflatabilecek geniş spektrumlu antibiyotiklere başvurmak yerine, çalışma daha hassas ilaç hedeflerine işaret ediyor: RIPK2 gibi bakteriyel sensörler, TRPC1–kalsiyum–S100A8/9 kaskadı ve metastazla ilişkili genleri yüksek vitese kilitleyen STAT3 kaynaklı DNA döngüleri. Bu zincirin bir veya daha fazla noktasını kesmek, kolorektal kanserin bağıstaki yerel bir sorundan karaciğerde ölümcül bir hastalığa dönüşmesini önlemeye yönelik yeni bir strateji sunabilir.
Atıf: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Anahtar kelimeler: kolorektal kanser metastazı, bağırsak mikrobiyomu, nötrofil ekstraselüler ağlar, STAT3 sinyalleşmesi, epigenetik gen regülasyonu