Clear Sky Science · tr
HaloTag teknolojisinden esinlenen bir glutamik asidin kovalent modifikasyonu
Protein “Çapalarını” İlaç Hedeflerine Dönüştürmek
Günümüz kanser ilaçlarının çoğu hücre içindeki proteinlere tutunarak çalışır. Ancak en önemli proteinlerin bazıları ilaçların tutunabileceği kolay bir “tutuşa” sahip değildir. Bu çalışma, laboratuvarda yaygın olarak kullanılan HaloTag adlı araçtan ilham alan zekice bir kimya hilesi sunuyor; kanserle ilgili büyüme sinyallerini kontrol eden bir proteindeki normalde erişilmesi güç bir bölgeye tutunmayı sağlıyor. Bu yaklaşım, tümörleri besleyen yolları daha kalıcı biçimde kapatabilecek yeni ilaç yollarını açabilir.
Neden Çoğu Kovalent İlaç Aynı Noktayı Hedefler
Sözde hedeflenmiş kovalent ilaçlar son yıllarda heyecan verici bir ilaç sınıfı haline geldi. Bu ilaçlar, proteindeki belirli bir aminoaside kalıcı bir bağ oluşturan hafif reaktif bir kimyasal grup taşır ve ilacı yerinde kilitler. Bu ilaçların neredeyse tamamı nispeten nadir ama yüksek reaktifliğe sahip olan sisteinine yönelir. Buna karşılık, apartat ve glutamat gibi iki başka aminoasit çok daha yaygındır ve sıklıkla bir proteinin şekli ve işlevi için kritik öneme sahiptir, ancak bunların asidik “karboksilat” grupları hücrenin sulu ortamında çok daha az reaktiftir. Bu durum, bunları seçici olarak modifiye etmeyi zorlaştırır ve bu çalışmadan önce glutamat- veya apartat-hedefli birkaç başarılı kovalent ilaç örneği mevcuttu.
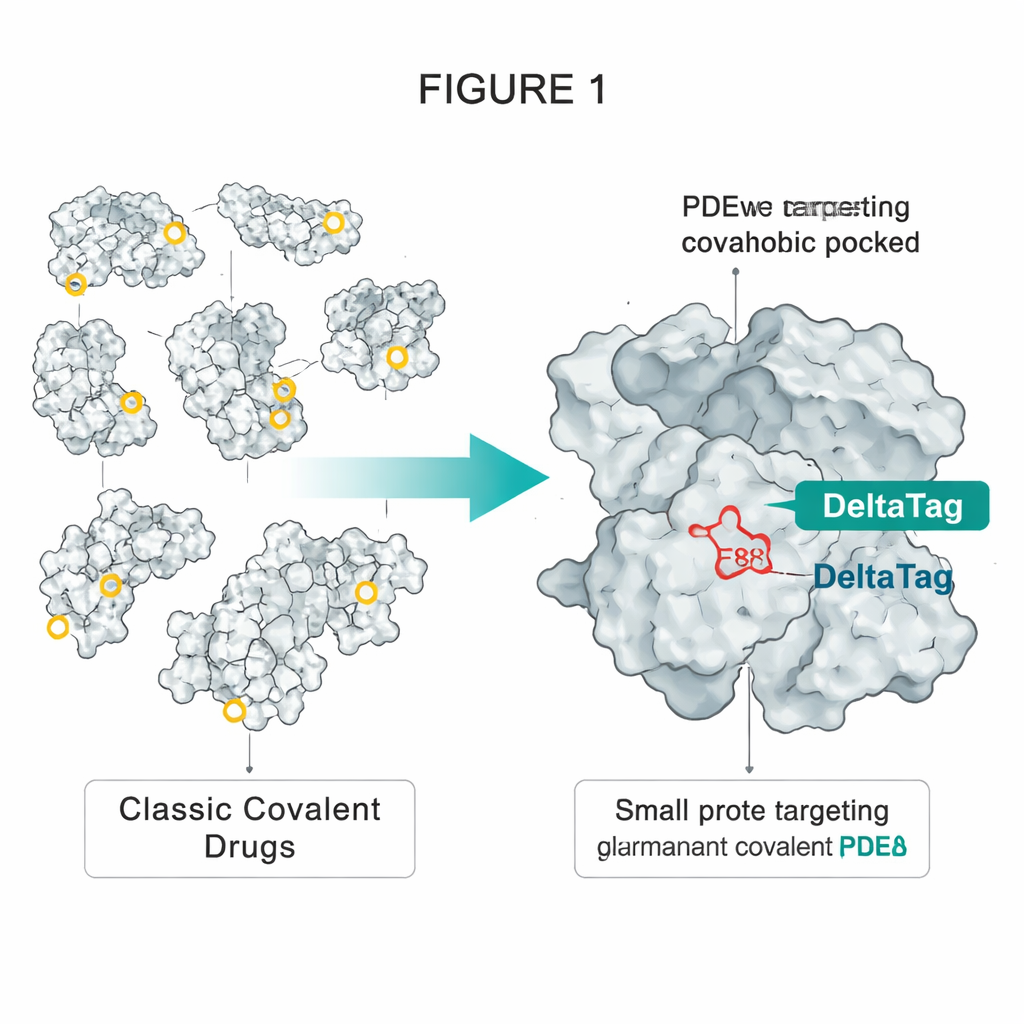
HaloTag Teknolojisinden Bir Hile Ödünç Almak
Yazarlar, floresan boyalarla kalıcı olarak etiketlenebilen geniş kullanıma sahip mühendislik ürünü bir protein olan HaloTag’ten ilham aldılar. HaloTag’te, yağlı bir cebin derinliklerindeki özel konumlandırılmış bir apartat, boyadaki basit bir kloroalkana zinciriyle reaksiyona girerek kararlı bir ester bağı oluşturur. Ekip, başka bir proteinin, PDEδ’nin, tek bir erişilebilir glutamat (E88) içeren benzer bir hidrofobik cebe sahip olduğunu fark etti. PDEδ, Rheb gibi lipid-modifiye sinyal proteinlerini hücre içinde taşıyarak bunların mTORC1 gibi büyümeyi teşvik eden komplekslerin aktive edildiği zarlara ulaşmasına yardımcı olur. Önceki kovalent olmayan PDEδ inhibitörleri bu taşıyıcıyı bloke edebiliyordu, ancak etkinlikleri sınırlıydı çünkü başka bir protein olan Arl2 zamanla bunları cebinden çıkarabiliyordu.
Glutamata Kilitlenen DeltaTag’i Tasarlamak
Bu “söküp atma” sorununu aşmak için araştırmacılar bilinen yüksek afiniteli bir PDEδ bloke ediciden yola çıktı ve yan zincirlerden birini HaloTag ligandlarında kullanılanlara benzer bir haloalken “savaş başlığı” taşıyacak şekilde yeniden tasarladı. Protein kristal yapılarının yol göstericiliğinde yapılan birkaç tur yapısal ince ayar sonucunda DeltaTag adını verdikleri bir bileşiğe ulaştılar. Temel özelliği, molekül PDEδ’nin lipid cebine yerleştiğinde bromürün E88 ile reaksiyona girecek biçimde hizalanmasını sağlayan bir fenetil bromid grubudur. Biyofiziksel ölçümler ve yüksek çözünürlüklü X-ışını yapıları DeltaTag’in özellikle bu glutamat ile kovalent bir ester bağı oluşturduğunu ve PDEδ üzerindeki diğer potansiyel olarak daha reaktif aminoasitlerin dokunulmadan kaldığını doğruladı. Bileşik, proteini verimli şekilde etiketleyecek kadar reaktif, ancak suda ve hücrenin ana kükürt bazlı antioksidantı glutatyon varlığında yaygın, ayrım gözetmeyen hasara yol açmayacak kadar stabil kaldı.
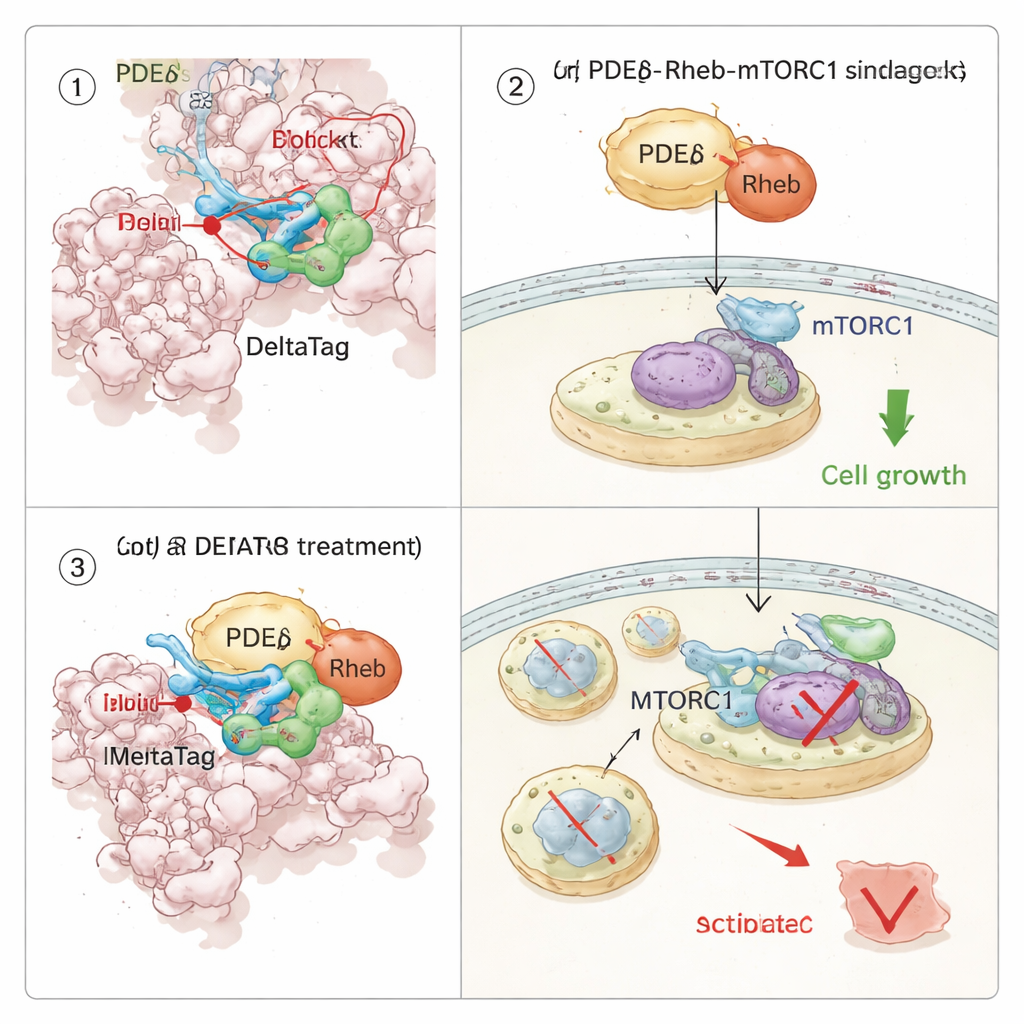
Kanser Hücrelerinde Bir Büyüme Yolunu Yeniden Bağlamak
PDEδ Rheb’i taşıdığı için ve Rheb de mTORC1 büyüme yolunu açtığı için ekip, PDEδ’nin kovalent inhibisyonunun hücre sinyalizasyonunu nasıl etkilediğini araştırdı. Binlerce protein genelinde termal stabilite profillemesi kullanarak DeltaTag’in hücre özütlerinde seçici olarak PDEδ’ye bağlandığını ve Rheb–mTOR ekseniyle ilişkili proteinleri etkilediğini gösterdiler. Canlı hücre görüntüleme deneylerinde DeltaTag, Rheb’in hücre içindeki dağınık deseninden daha kümelenmiş iç zar yapıları lehine yer değiştirmesine neden oldu; bu, normal taşımanın bozulmasıyla tutarlı bir sonuçtu. Global fosfoproteomik ve odaklı Western blot analizleri, ribozomal bir protein olan S6’nın fosforilasyonu ile izlenen mTORC1 aktivitesinin zamanla düştüğünü, buna karşılık ilişkili yollarda telafi edici sinyallerin arttığını ortaya koydu. Önemli olarak, KRAS mutantları tarafından sürülen ve güçlü mTOR sinyallemesine bağımlı birkaç insan kanser hücre hattında DeltaTag, yakın akraba tersinir inhibitörlere göre hücre proliferasyonunu daha etkili biçimde yavaşlattı ve PDEδ eksik hücrelerde etkisi zayıftı; bu da ana etkisinin hedefte olduğunu destekliyor.
Yeni Tür İlaç Hedeflerine Bir Kapı Açmak
Bu çalışma, HaloTag’ten ödünç alınan nispeten basit bir haloalkane kimyası kullanarak, bir proteindeki yağlı bir cebin içine gömülmüş tek bir glutamata kalıcı, son derece seçici bir bağ oluşturabilen küçük moleküller geliştirmenin mümkün olduğunu gösteriyor. Model sistem PDEδ’de bu kovalent bağ, önceki tersinir ilaçlardan daha dayanıklı bir kanserle ilişkili büyüme yolunun bloke edilmesini sağlıyor. Daha genel olarak, aynı tasarım mantığı, stratejik olarak yerleştirilmiş bir glutamat veya apartat sundukları sürece, tipik “reaktif” aminoasitlerden yoksun ama hidrofobik boşluklara sahip diğer proteinlere de uygulanabilir. Daha fazla optimizasyonla, DeltaTag benzeri glutamat-hedefli kovalent inhibitörler kimyasal biyoloji için yararlı araçlar ve nihayetinde şu anda ilaç geliştirmenin zor olduğu proteinleri hedef alan yeni tedavilere öncülük edebilecek adaylar haline gelebilir.
Atıf: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Anahtar kelimeler: kovalent inhibitörler, glutamat hedefleme, PDEδ, mTOR sinyal iletimi, kanser ilaç tasarımı