Clear Sky Science · tr
Vaksin analizleri için virüs glikoprotein nanodisk platformu
Virüs Proteinlerini Ölçülebilir Hedeflere Çevirmek
Modern aşılar giderek daha çok, virüs yüzeyini kaplayan proteinlerin hassas şekilde tasarlanmış versiyonlarına dayanıyor. Bu proteinler koruyucu antikorların başlıca hedefleri olsa da, doğal, zarla bağlı hallerinde incelemek zor oluyor. Bu makale, tam uzunluktaki viral yüzey proteinlerini nanodisk adı verilen küçük, düz lipid parçacıklarına yerleştiren yeni bir laboratuvar platformunu tanımlıyor. Bu düzenek, araştırmacılara aşı adaylarının gerçek virüsleri ne kadar iyi taklit ettiğini, antikorların nasıl bağlandığını ve aşıları daha iyi koruma sağlayacak şekilde nasıl yeniden tasarlayabileceklerini ölçme olanağı veriyor.
Viral Yüzeyin Yeniden Oluşturulmasının Önemi
En önemli viral proteinlerin birçoğu, gerçek bir virüste olduğu gibi yağlı bir zar içinde sabitlenmiş halde bulunur. Geleneksel laboratuvar yaklaşımları bu proteinleri üretmeyi ve çözeltide saflaştırmayı kolaylaştırmak için zar kısmını kesip atar. Ancak bu kestirme yol, antikorlar için özellikle değerli hedeflere ev sahipliği yapan, zar yakınındaki bölgeleri ortadan kaldırır; bunların arasında HIV’e özgü zar-proksimal dış bölge (MPER) adlı bir segment de vardır. Zar yakınındaki bu bölgeler gerçekçi bir lipid ortamına gömülmediklerinde farklı görünebilir ve farklı davranabilir; bu da çözünebilir protein parçalarının bir aşının vücutta nasıl performans göstereceği hakkında eksik veya yanıltıcı bir tablo sunabileceği anlamına gelir.
Çok Yönlü Bir Nanodisk Platformu Kurmak
Araştırmacılar, tam uzunluktaki viral yüzey proteinlerini insan hücrelerinden elde etmek, doğal zar geçiş segmentlerini korumak ve bunları kontrollü bir lipid diske yeniden yerleştirmek için beş günlük, sade bir iş akışı geliştirdiler. Önce mühendislik yapılan HIV ve Ebola glikoproteinlerini hücre yüzeyinde eksprese ettiler, sonra bunları deterjanla nazikçe çıkardılar ve bir saflaştırma matriksine tutturdular. Proteinler hâlâ bağlıyken, tanımlı lipidleri ve küçük disk şeklinde bir zar oluşturan kuşak benzeri bir iskelet proteini karışıma eklediler. Deterjan uzaklaştırıldıkça viral proteinler bu nanodisklerin içine yerleşti. Elde edilen preparatlar son derece saf, buzdolabında aylarca stabil ve düşük çözünebilirlikteki viral sivri uçlarda bulunanlara çok yakın glikan (şeker) kaplamaları taşıyordu. 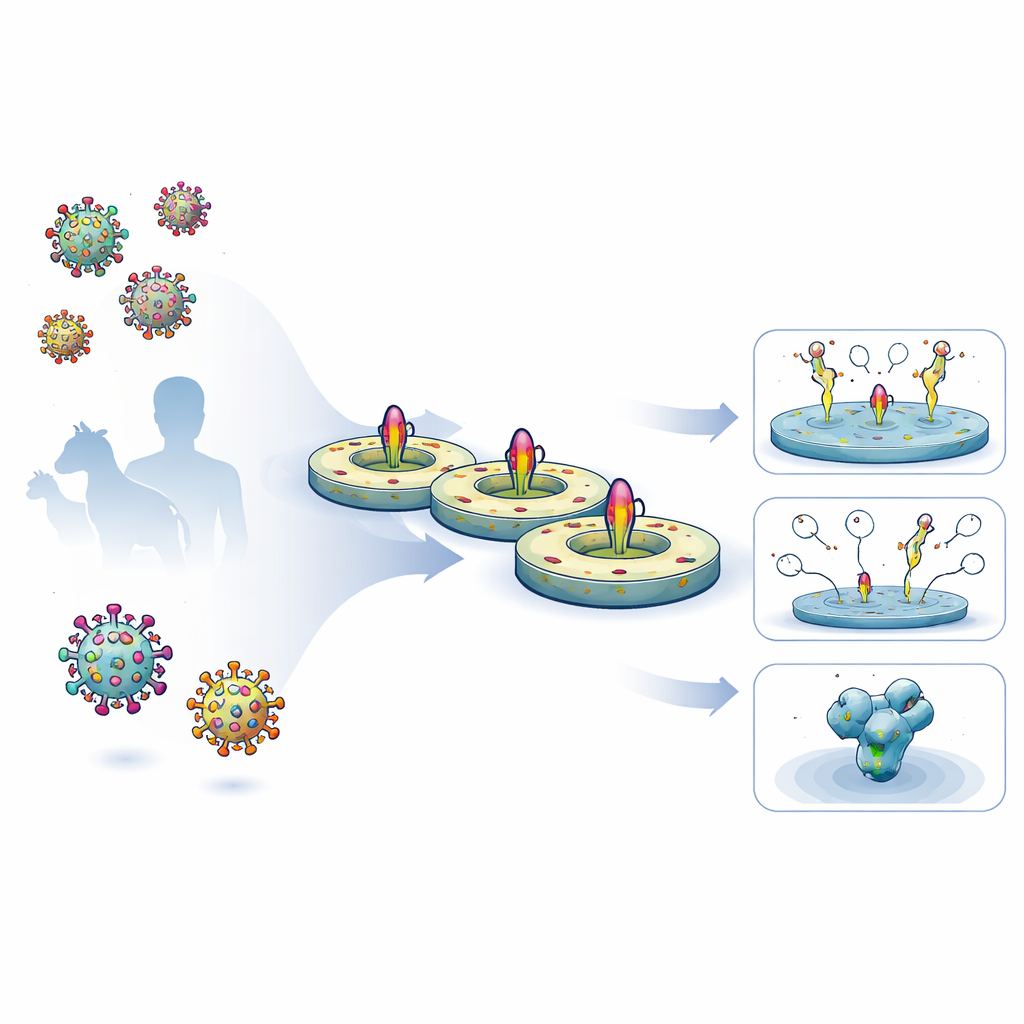
Antikor Bağlanmasını ve Bağışıklık Yanıtlarını Okumak
Nanodisk içine gömülü proteinlere sahip olarak ekip, çeşitli yüzey plazmon rezonansı (SPR) düzenekleri altında farklı antikorların ne kadar iyi bağlandığını test etti; bu teknik bağlanmayı gerçek zamanlı izliyor. MPER bölgesini açığa çıkarmak üzere tasarlanmış HIV nanodiskleri kullanarak, güçlü bir geniş nötralize edici antikor olan 10E8’in önceki tasarıma göre mühendislik yapılmış konstrükte yaklaşık 70 kat daha sıkı bağlandığını gösterdiler; bunun başlıca nedeni daha yavaş ayrılmasıydı. MPER bölgesini bozan kontrol mutasyonları 10E8 bağlanmasını tamamen ortadan kaldırdı ve platformun tasarım değişikliklerinin kilit epitopları nasıl etkilediğini hassas şekilde raporlayabildiğini doğruladı. Aynı nanodiskler, akım sitometrisi (flow cytometry) içinde problar olarak çalıştı; aşılanmış fare ve maymunlardan, standart çözünebilir problarda bulunmayan parçalar da dahil tam transmembran formunu tanıyan B hücrelerini yakalamaya yardımcı oldular. 
Atomik Detayda Tam Hedefi Görmek
Antikorların MPER’i doğal ortamında tam olarak nasıl tanıdığını anlamak için yazarlar, üç farklı geniş nötralize edici antikora bağlanmış mühendislik HIV nanodisklerini görüntülemek üzere kriyo-elektron mikroskopisini kullandılar. Bir antikor olan 10E8’in MPER segmentiyle etkileşim halinde iken HIV sivri ucunun geri kalanının lipid diskte sabit kaldığı 3.5 angström çözünürlüklü bir yapı elde ettiler. Bu, 10E8 ile hem MPER hem de dış proteinin yakın kısımları arasında sürekli bir temas ağı ortaya koydu; iki alt birim arasındaki birleşme noktasında derin bir oyuk da dahil. Bu yapıyı 10E8’in yalnızca kısa bir peptide bağlanmış önceki görüntüleriyle karşılaştırarak, membran ortamı ve tam uzunluktaki sivri uçağın, daha basit modellerde görünmez olan ek temaslara ve dinamik hareketlere izin verdiğini ve virüsteki belirli aminoasitlerin 10E8’in nötralizasyon etkinliğini güçlü şekilde etkilediğini gösterdiler.
Daha Akıllı Aşılar için Geniş Kullanım Alanları
Pratik açıdan bu nanodisk platformu, aşı tasarımcılarına transmembran aşı adaylarını uzun süredir çözünebilir protein parçaları için ayrılmış güçlü analitik araçlarla değerlendirme imkanı sağlıyor. Farklı virüslerde işe yarıyor, ayrıntılı bağlanma ölçümlerini destekliyor, aşı kaynaklı B hücrelerinin hassas sıralanması ve dizilenmesine olanak tanıyor ve gerçekçi zar-proksimal epitopları yakalayan yüksek çözünürlüklü yapılar veriyor. Genel bir okuyucu için çıkarım şudur: Bilim insanlarının artık viral yüzey proteinleri için, hangi aşı tasarımlarının gerçekten gerçek virüs gibi göründüğünü ve davrandığını ve bunları daha güçlü, daha geniş antikor yanıtları oluşturacak şekilde nasıl ayarlayabileceklerini gösterebilecek daha gerçekçi bir test ortamı var. Bu, yalnızca HIV için değil birçok diğer zarfla kaplı virüs için de bir sonraki nesil aşıların geliştirilmesini hızlandırmalıdır.
Atıf: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Anahtar kelimeler: nanodiskler, HIV aşıları, viral glikoproteinler, geniş nötralize edici antikorlar, kriy0-EM