Clear Sky Science · tr
Protein C-terminal variations impact proteostasis
Proteinlerin Kuyruk Ucu Sağlığı Nasıl Şekillendirir
Hücrelerimizdeki her proteinin sonu sadece birkaç yapı taşı içeren küçük bir “kuyruk”la biter. Bu kuyruklar sanki sonradan eklenmiş gibidir, ama bu çalışma onların hangi proteinlerin kalıp hangilerinin hızla ortadan kaldırılacağına sessizce karar verdiğini gösteriyor. Protein düzeyleri kanser, genetik hastalıklar ve hücrelerin strese yanıt vermesi gibi süreçlerin temelini oluşturduğundan, bu kuyrukları anlamak hastalık riskini okumak ve gelecekteki tedavileri tasarlamak için yeni yollar sunuyor.
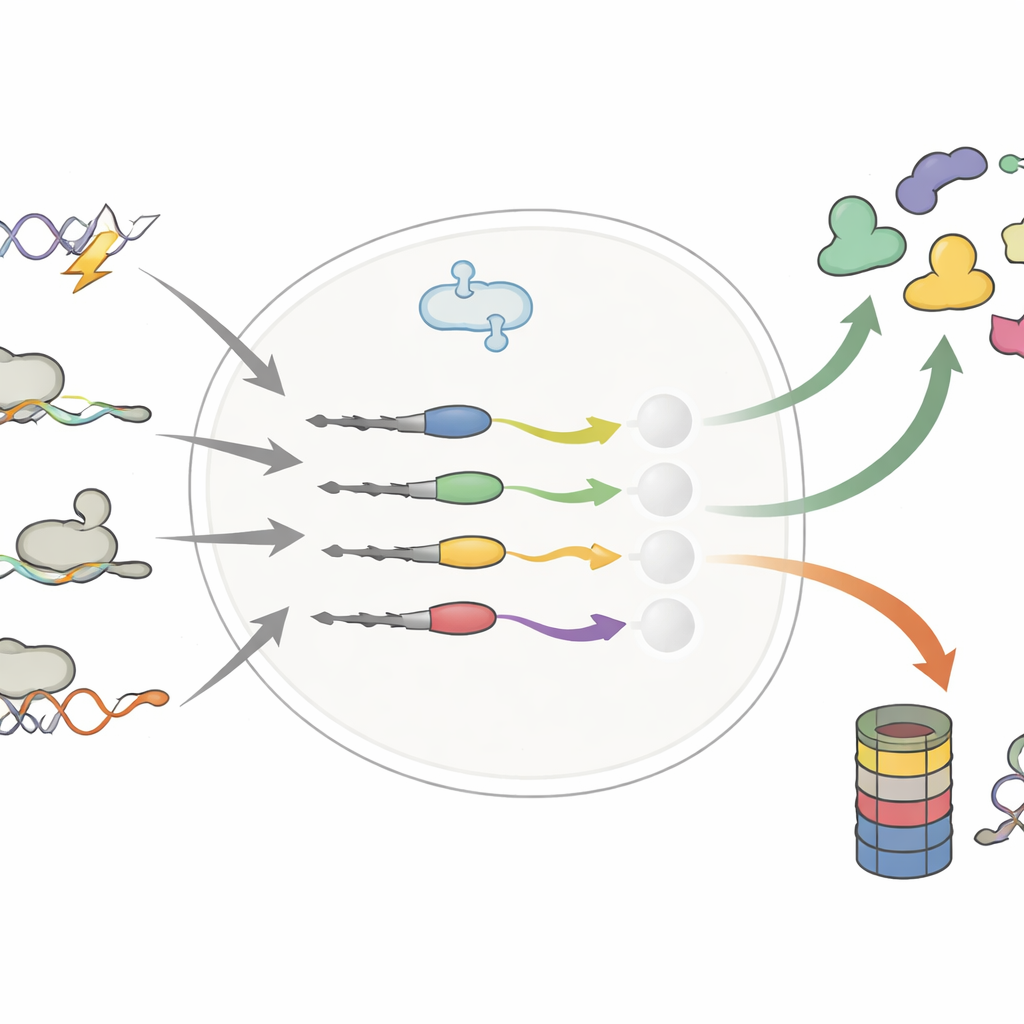
Proteinin Kuyruk Ucunda Küçük Değişiklikler, Yaşam Süresinde Büyük Kaymalar
Yazarlar, proteinlerin en uzak ucu olan C-terminal’e odaklandı; burada DNA mutasyonları, alternatif RNA kesme-birleştirmesi veya ribozomların olağan durdurma işaretini aşması sonucu birkaç ek veya yer değiştirmiş yapı taşı ortaya çıkabilir. Önceki çalışmalar bu “hatalı” kuyrukların çoğunlukla imha etiketi gibi davranıp kusurlu proteinleri hücrenin öğütücüsüne gönderdiğini öne sürmüştü. Binlerce normal ve değiştirilmiş kuyruğu sistematik olarak karşılaştırarak, bu çalışma bu basit görüşü çürütüyor. Ekip, değişmiş kuyrukların bir proteinin ömrünü ya kısaltabileceğini ya da uzatabileceğini; bazen kanser sürücülerini stabilize ederken bazen tümör baskılayıcılarını destabilize ettiğini gösteriyor.
Genetik Hatalar Proteinlere Ne Zaman Yardımcı Olur veya Zarar Verir
Kuyruk değişikliklerinin önemli bir kaynağı, normal durdurma sinyalini silen nonstop mutasyonlardır; bu durumda ribozom genellikle sessiz kalan bir RNA bölgesine devam eder. Araştırmacılar, her kuyruğun model bir proteini ne kadar koruduğunu veya zayıflattığını ölçen çift renkli bir raporlayıcı kullanarak 3.000’den fazla hastalıkla ilişkili nonstop varyantı test ettiler. Ortalama olarak mutant kuyruklar hâlâ proteinleri normal karşıtlarına göre daha az stabil hale getiriyordu, fakat kayda değer bir bölüm bunun tersini yapıyordu: nonstop mutasyonların yaklaşık onda biri proteinleri stabilize ederken, neredeyse üçte biri destabilize ediyordu. Bu değişimler iyi bilinen onkoproteinleri ve tümör baskılayıcıları etkileyerek, önemsiz görünen mutasyonların aslında hücre büyümesi ve ölümü dengesini değiştirebileceğini ima ediyor.
Splicing ve Readthrough’dan Kaynaklanan Doğal Çeşitlilik
Tüm kuyruk farkları kazadan ibaret değil. Genlerimiz, alternatif kesme-birleştirme ve programlı stop-kodon okunumu (readthrough) yoluyla rutin olarak birden fazla protein versiyonu üretir. İnsan gen kataloglarını tarayarak yazarlar, genlerin neredeyse üçte ikisinin birden fazla kuyruk tasarımına sahip proteinler ürettiğini ve birçok örneğin yalnızca son birkaç yapı taşında farklılık gösterdiğini buldular. Seçilen örneklerin test edilmesi, bu neredeyse aynı versiyonların sıklıkla belirgin şekilde farklı yarı-ömrü olduğunu gösterdi. Bazı readthrough ile oluşan kuyruklar proteinleri daha stabil hale getirirken, bazıları tam tersini yaptı. Bu, hücrelerin kuyruk varyasyonunu belirli protein formlarının farklı dokularda veya koşullarda ne kadar süreyle kalacağını ince ayarlamak için kullandığını düşündürüyor.
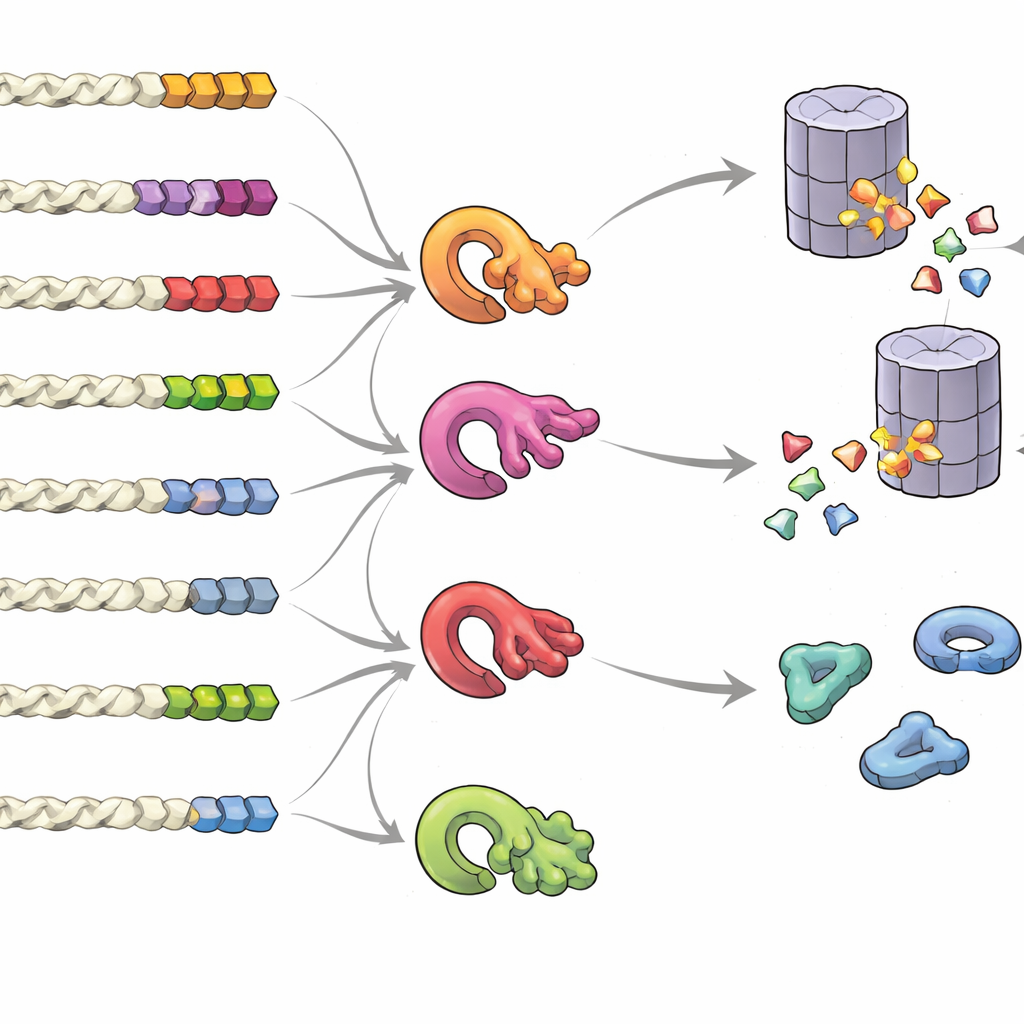
Bir Kuyruğu “Beni Tut” veya “Beni At” Sinyali Yapan Nedir
Bir kuyruğun protein kaderini nasıl etkilediğini anlamak için ekip rastgele kuyruk kütüphaneleri oluşturdu ve bunların toplu etkisini ölçtü. Tek bir sabit “motif” değil, genel bileşim, konum ve belirli yapı taşlarının kümelenmesinin önemli olduğunu buldular. Küçük veya yağlı bileşenlerce zengin, ya da daha nadir bulunan sistein ve triptofan içeren kuyruklar, özellikle bu kalıntılar kümelendiğinde, degradasyona davetiye çıkarma eğilimindeydi. Buna karşın asidik bileşenlerce zengin kuyruklar stabiliteyi destekliyordu. Birçok tür arasında bakıldığında, normal protein kuyruklarının riskli desenlerden kaçınma yönünde evrimsel baskı izleri gösterdiği, oysa readthrough veya çerçeve kayması gibi hata yatkın kuyrukların destabilize edici bileşimlere eğilimli olduğu görüldü. Grup ayrıca, farklı hidrofobik kuyruk desenlerini tanımada uzmanlaşmış birden çok kalite kontrol enzimi—farklı ubikitin ligazları—buldu; bu enzimler hangi proteinlerin yok edilmesine karar veren karmaşık bir ağ oluşturuyor.
Bu Konunun Tıp ve Biyoteknoloji İçin Önemi
Bu çalışma protein kuyruklarını pasif son noktalar olmaktan çıkarıp protein bolluğunun aktif düzenleyicileri olarak yeniden çerçeveliyor. Bir okur için bunun anlamı şudur: birçok hastalık sadece bozuk proteinlerden değil, aynı zamanda proteinlerin ne kadar süreyle hücrede kaldığını belirleyen uçlardaki küçük farklılıkların yol açtığı ince değişikliklerden de kaynaklanabilir. Ayrıca, bazı genetik bozuklukları tedavi etmek için kasıtlı olarak durdurma sinyallerinin readthrough’unu teşvik eden tedavilerin birçok normal proteinin ömrünü istemeden değiştirebileceği uyarısını da getiriyor. Aynı zamanda bulgular güçlü yeni stratejiler de öneriyor: kuyruk dizilerini mühendislik yoluyla değiştirmek veya hücreleri belirli splice formalarını ya da readthrough olaylarını tercih etmeye yönlendirmek suretiyle, bilim insanları bir gün protein düzeylerini olağanüstü bir hassasiyetle artırıp azaltabilirler.
Atıf: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Anahtar kelimeler: protein stability, C-terminal tail, protein degradation, genetic mutations, proteostasis