Clear Sky Science · tr
FCHo2, talin değil, eğimli adezyonlarda integrin ɑvβ5’in içeriden-dışarı aktive olmasını sağlar
Hücreler Çevrelerinin Şeklini Nasıl Hisseder
Vücudumuz, çevresine sürekli tutunan, çekip iten hücrelerden oluşur; böylece hareket eder, bölünür veya yerinde kalır. Bu çalışma gösteriyor ki hücreler yalnızca çevrelerinin ne kadar sert olduğunu hissetmekle kalmaz — aynı zamanda onun şeklini de okurlar. Hücre zarının belirgin şekilde kıvrıldığı yerlerde yalnızca devreye giren özel bir adezyon sisteminin keşfi, hücrelerin düz yüzeylere ve lifli ortamlara farklı iç “tutunma” biçimleri kullandığını ortaya koyuyor; bunun doku oluşumu ve kanserin yayılması üzerinde önemli sonuçları var.
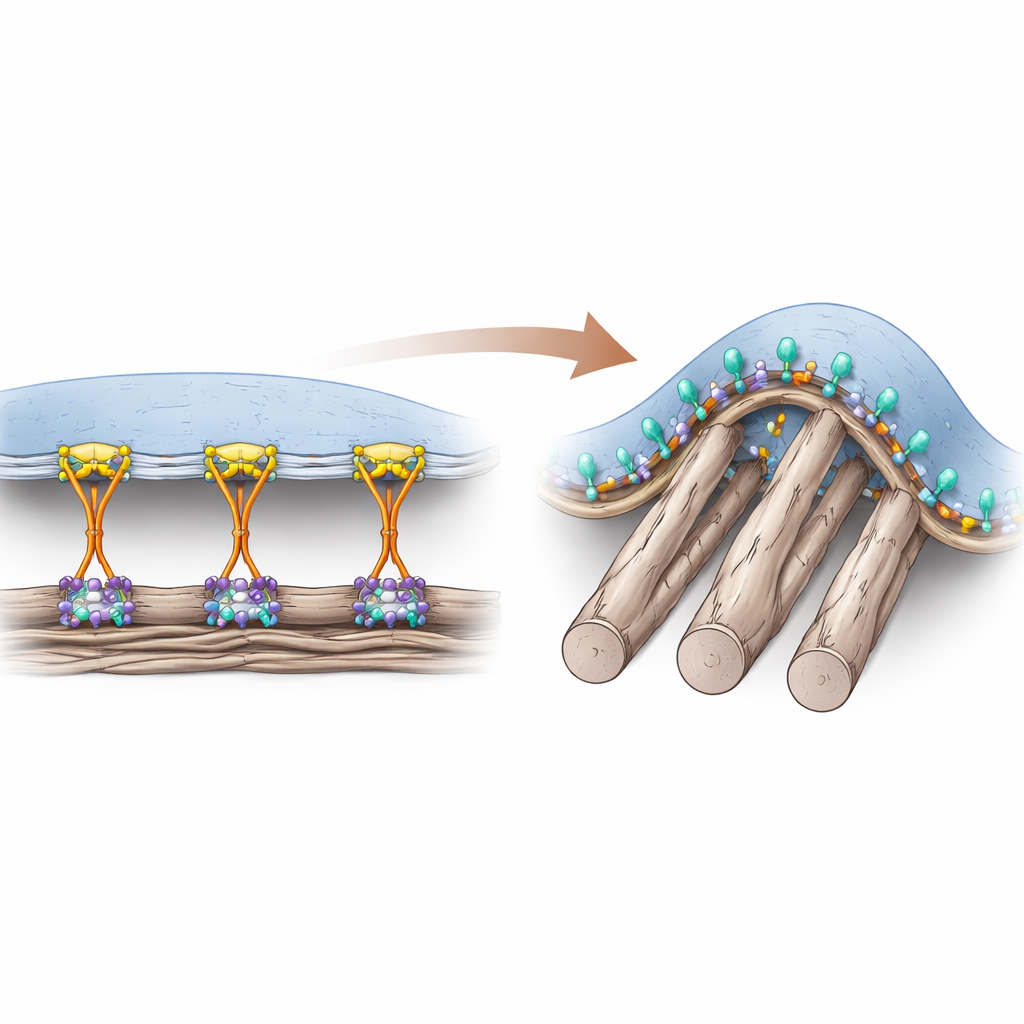
Hücrelerin Tutunma Biçimleri: İki Yol
Hücreler, çevrelerindeki protein açısından zengin matrikse integrin adı verilen yüzey reseptörleri aracılığıyla bağlanır. Yıllarca araştırmacılar, talin adlı yardımcı bir proteinin integrinleri hücrenin içinden “açmak” ve klasik odak adezyon adı verilen güçlü tutunma noktalarında sağlam bağlantı sağlamak için mutlaka gerekli olduğunu düşündü. Bu adezyonlar öncelikle düz, sert yüzeylerde oluşur ve hücre iskeleti üzerinden güçlü çekme kuvvetleri iletir. Ancak canlı dokularda çevreyi oluşturan birçok lif yumuşak ve silindirik olup, kuvvetleri kolayca taşıyamayan kıvrımlı temas noktaları yaratır. Yazarlar daha önce, zarın ince liflerin etrafında büküldüğü yerlerde beliren ve belirli bir integrine, αvβ5’e bağımlı olan farklı bir adezyon türü—eğimli adezyon—bulmuşlardı.
Eğimli Tutunmalar Farklı Bir Yardımcı Kullanır
Yeni çalışmada ekip, talinin hâlâ orada olmasına karşın eğimli adezyonlarda integrin αvβ5’in ana etkinleştiricisi olmadığını gösteriyor. Bunun yerine FCHo2 adlı bir eğrilik algılayıcı protein bu görevi üstleniyor. Hücre zarlarını kontrollü biçimde büken hassas olarak tasarlanmış nano boyutlu çubuklar ve sütunlar kullanarak, αvβ5’in eğrilik bölgelerinde güçlü şekilde kümelendiğini gözlemlediler; fakat bunun için FCHo2’nin β5 kuyruk kısmının hücre içindeki çok kısa bir dizisini—HDRRE motifini—bağlayabilmesi gerekiyordu. Bu motif bozulduğunda integrin hâlâ odak adezyonlarda işlev görüyordu ama eğimli adezyonları artık oluşturamıyordu. FCHo2’nin baskılanması klasik odak adezyonları büyük ölçüde korurken eğimli adezyonları yok ederken, talinin uzaklaştırılması odak adezyonlarını ciddi biçimde zayıflatıyor ama eğimli adezyonları büyük ölçüde etkilemiyordu.
Tek Bir Amino Asit Anahtarı: Şekil Seçici
Bir muamma, yakından ilişkili bir integrin olan αvβ3’ün iç kuyruğu β5’inkine çok benzemesine rağmen neden eğimli adezyon oluşturamamasıydı. İki integrin arasında domain takası yapıp nokta mutasyonlar uygulayarak yazarlar, talin bağlanma bölgesine yakın tek bir belirleyici konumu belirlediler: çoğu β integrininin yanında bir triptofan (W) bulunurken, β5 benzersiz olarak tirozin (Y766) taşır. β5’in tirozinini triptofana çevirdiklerinde integrin eğimli adezyonlara katılma yeteneğini kaybetti ve yalnızca odak adezyonları tercih eden β3 benzeri davranış gösterdi. Ters değişim—β3-benzeri chimera’ya tirozin koymak—eğrilik duyarlılığını geri getirdi. Bu tirosinin fosforile veya fosforile olmayan halleriyle taklit edilen varyantlarla yapılan ek deneyler, bu amino asit üzerindeki kimyasal değişikliğin integrini düz, yüksek-kuvvetli odak adezyonlarına veya eğimli, düşük-kuvvetli adezyonlara eğilimlendirebileceğini gösteriyor.
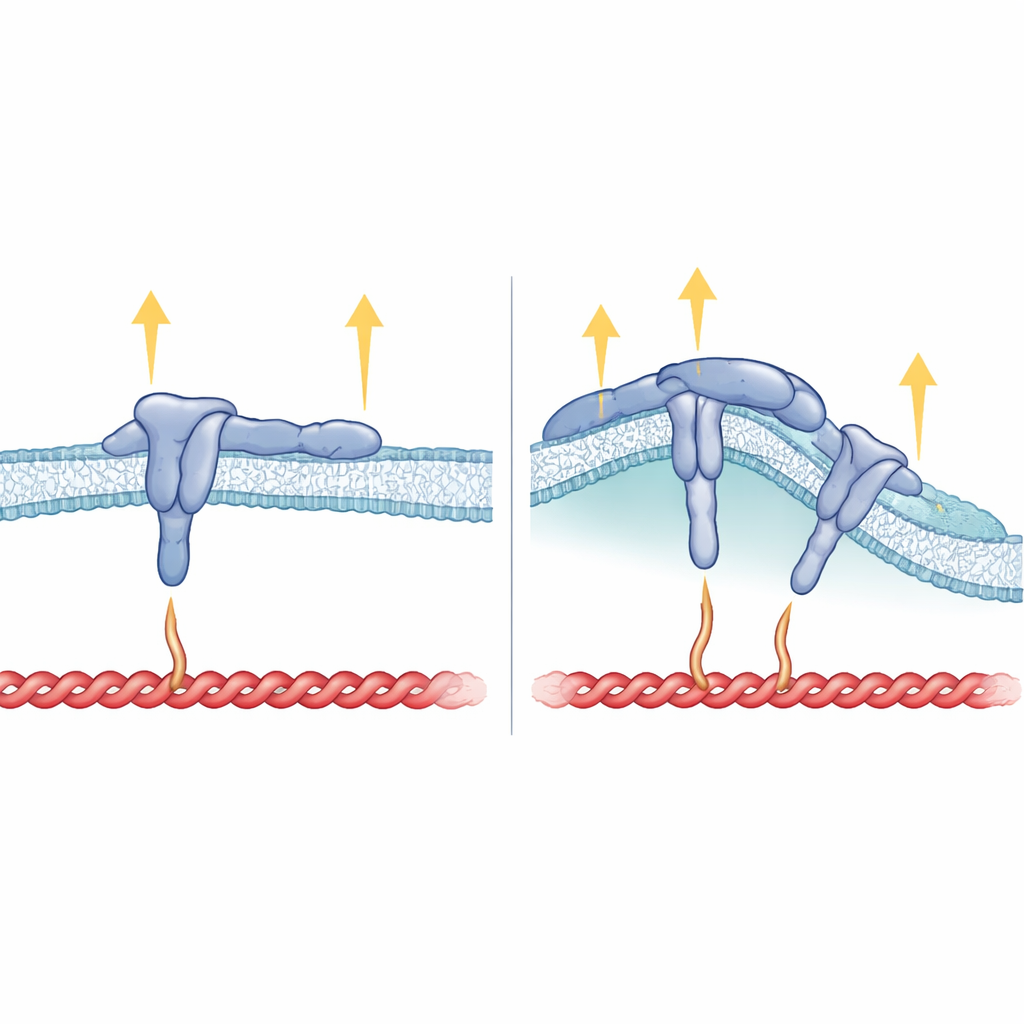
Zar Şekli, Integrin Yapısı ve Kuvvet Birbiriyle Nasıl Uyumlanır
İç kuyruğun ötesinde, zar boyunca uzanan β5’in transmembran bölgesi de kritik çıktı. Araştırmacılar β5’in transmembran segmentini β3’ünkiyle değiştirdiklerinde, ortaya çıkan integrin hâlâ odak adezyonlar oluşturabiliyordu ancak eğimli bölgeleri artık tercih etmiyor ve FCHo2 ile eşzamanlılık göstermiyordu. Bu, integrinin zar içindeki oturuş biçiminin HDRRE motifini FCHo2’nin eğimli bölgelerde tutunabileceği biçimde yönlendirmesine yardımcı olduğunu ve böylece ligand bağlı, aktif αvβ5’i stabilize ettiğini düşündürür. Eğimli adezyonlarda talin, integrin kuyruğunun yalnızca daha uzak bir bölgesine temas ediyor gibi görünür ve yüksek gerilim altına girmez; bu nedenle vinculin, tensin ve kindlin gibi kuvvet isteyen bileşenler büyük ölçüde orada yoktur. Buna karşılık odak adezyonlarda talin kuyruğun hem yakın hem uzak bölgelerini ve zarı kavrar, güçlü çekme kuvvetlerini destekler ancak FCHo2’nin aynı bölgeye erişmesini engeller.
Bu Hücre Davranışı İçin Ne Anlama Gelir
Bir gözlemci için bu çalışmanın mesajı şudur: Hücrelerin çevrelerine tutunmak için iki ayrı “tutunma modu” vardır. Düz, sert alanlarda talin kaynaklı odak adezyonlarıyla çok güçlü çekmeye uygundurlar. Yumuşak, lifli ve kıvrımlı yapılarda ise FCHo2 kaynaklı eğimli adezyonlara geçerler; bunlar integrin αvβ5’i çok daha düşük kuvvetle stabilize eder. Integrinin dizisindeki küçük bir değişiklik—ve bu bölgenin kimyasal olarak modifiye edilip edilmediği—hangi modun kullanılacağını belirlemeye yardımcı olur. Bu ikili sistem, hücrelerin üç boyutlu ortamlarda hem sertliği hem de şekli yorumlamasına olanak tanır; bu da göç, doku organizasyonu ve hastalık sırasında istila etme biçimleri üzerinde etkili olabilir.
Atıf: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Anahtar kelimeler: integrinler, hücre adezyonu, zar eğriliği, FCHo2, sitokeleton