Clear Sky Science · tr
Deneylerle Bilgilendirilen Bir Polimer Modeli, Genomik Lokusların Yüksek Çözünürlüklü Örgütlenmesini Ortaya Koyuyor
DNA Katlanması Hücre Kimliğini Nasıl Şekillendirir
Vücudunuzdaki her hücre temelde aynı DNA’yı taşır; buna rağmen beyin hücreleri, deri hücreleri ve kök hücreler çok farklı davranırlar. Bunun önemli bir nedeni, DNA’nın çekirdek içinde nasıl katlandığı ve paketlendiğidir. Bu çalışma, o katlanmayı olağanüstü ayrıntıda “görmenin” yeni bir yolunu sunuyor ve DNA’nın fiziksel düzenini önemli genlerin açık ya da kapalı olmasına bağlıyor. Deneyleri fizik temelli bilgisayar simülasyonlarıyla harmanlayarak, yazarlar genetik materyalin temel yapı taşları gibi davranıyor olabilecek gizli kümelenmeleri ortaya koyuyorlar.
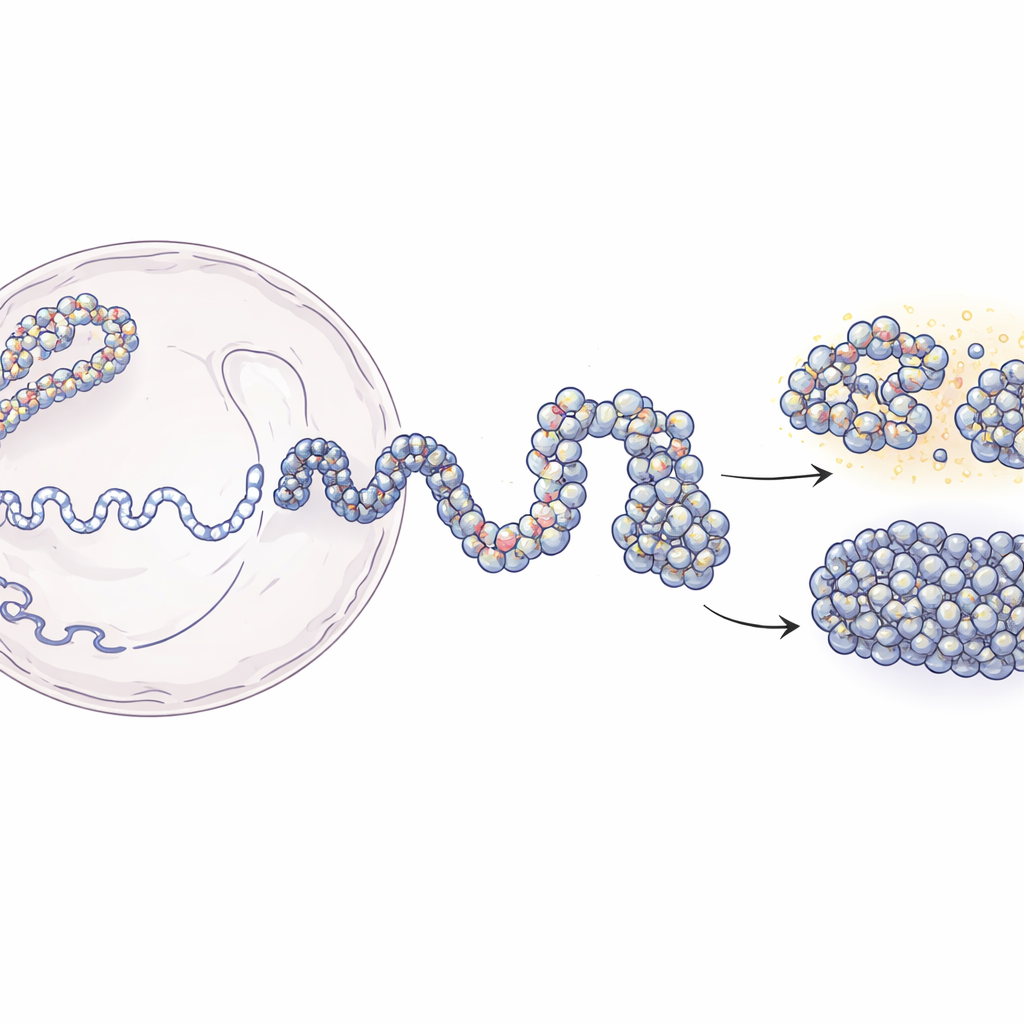
Uzun DNA İplikçiklerinden 3B Genom Haritalarına
Çekirdek içinde DNA, nükleozom adı verilen protein bobinleri etrafına sarılarak boncuk-üzeri bir yapı olan kromatini oluşturur. Hi-C ve Micro-C gibi modern teknikler, hangi DNA parçalarının 3B’de birbirine yakın olduğunu söyleyebilir, fakat genellikle bulanık, popülasyon ortalamasına dayalı kesitler sunarlar. Öte yandan bireysel nükleozomların yerini tespit eden deneyler yerel olarak çok keskin ayrıntı verir ama daha büyük yapının hissini az sağlar. Bu çalışma bu boşluğu kapatıyor. Yazarlar, uzak DNA segmentlerinin ne sıklıkta temas ettiğini bildiren düşük çözünürlüklü temas haritalarından başlayıp bunları nükleozom pozisyonlarının deneysel haritalarıyla birleştiriyor. Polimer fiziği ilkelerini kullanarak, deney verileriyle uyumlu ama birkaç düzine DNA bazına kadar çözünürlüğe inen simüle edilmiş 3B kromatin kümeleri inşa ediyorlar.
Kromatini Yeniden Kurmak İçin İki Aşamalı Bir Strateji
Modelleme yaklaşımı iki ana aşamada ilerliyor. İlk olarak ekip, Hi-C verilerini kullanarak 200.000 bazlık bir DNA parçasının çok sayıda olası büyük ölçekli şeklini üretiyor; kromatini, 5.000 bazlık segmentlerin deneylerde gözlenen temaslara göre yapılması ya da kaçınılması için nazikçe yönlendirildiği esnek bir zincir olarak ele alıyorlar. Bu kaba yapılar, hücredeki proteinlerin oluşturduğu genel katlanma desenini yakalıyor. İkinci aşamada ise her büyük boncuk, bireysel nükleozomlardan ve bunlar arasındaki kısa DNA bağlayıcılarından oluşan çok daha ince bir zincirle değiştiriliyor. Bu nükleozomların konumları, genom boyunca tipik olarak nerede yer aldıklarını gösteren bir enzim-temelli haritalama yöntemi (MNase-seq) ile elde ediliyor. İnce taneli zincirler daha sonra daha geniş mimariye saygı gösterirken katlanmaya izin veriliyor. Araştırmacılar yüksek çözünürlüklü modellerini deneysel çözünürlüklere “bulanıklaştırdıklarında”, hem Hi-C hem de Micro-C temas haritalarını yüksek doğrulukla yeniden üretiyorlar.
Yapısal Birimler Olarak Nükleozom Kümelerini Keşfetmek
Yazarlar simüle edilmiş yapılarına yakından baktıklarında çarpıcı bir desen ortaya çıktı: nükleozomlar eşit şekilde dağılmamış, bunun yerine düzensiz kümeler halinde toplanmıştı; yazarlar bu kümelere nükleozom kümeleri adını veriyor. Bu kümeler, gerçek hücrelerin süper-çözünürlüklü mikroskop görüntülerinde daha önce görülen topaklı yapılara benziyor. Binlerce simüle edilmiş kesiti analiz ederek ekip, bu kümelerin küresel değil uzamış olduğunu ve tipik olarak bir arada paketlenmiş birkaç nükleozom içerdiğini gösterdi. Kritik olarak, bu kümeler içindeki temaslar deneysel verilerde görülen alan-benzeri etkileşim bloklarıyla yakından örtüşüyor; bu da kümelerin rastgele kazalar değil, kromatin organizasyonunun temel 3B birimleri olduğunu gösteriyor. Simülasyonlar ayrıca deneysel olarak tespit edilmesi zor olan ek ince alan sınırları da öngörüyor; bu da bu fiziksel modelin gürültülü verilerde gizli ince ölçekli özellikleri ortaya çıkarabileceğini düşündürüyor.
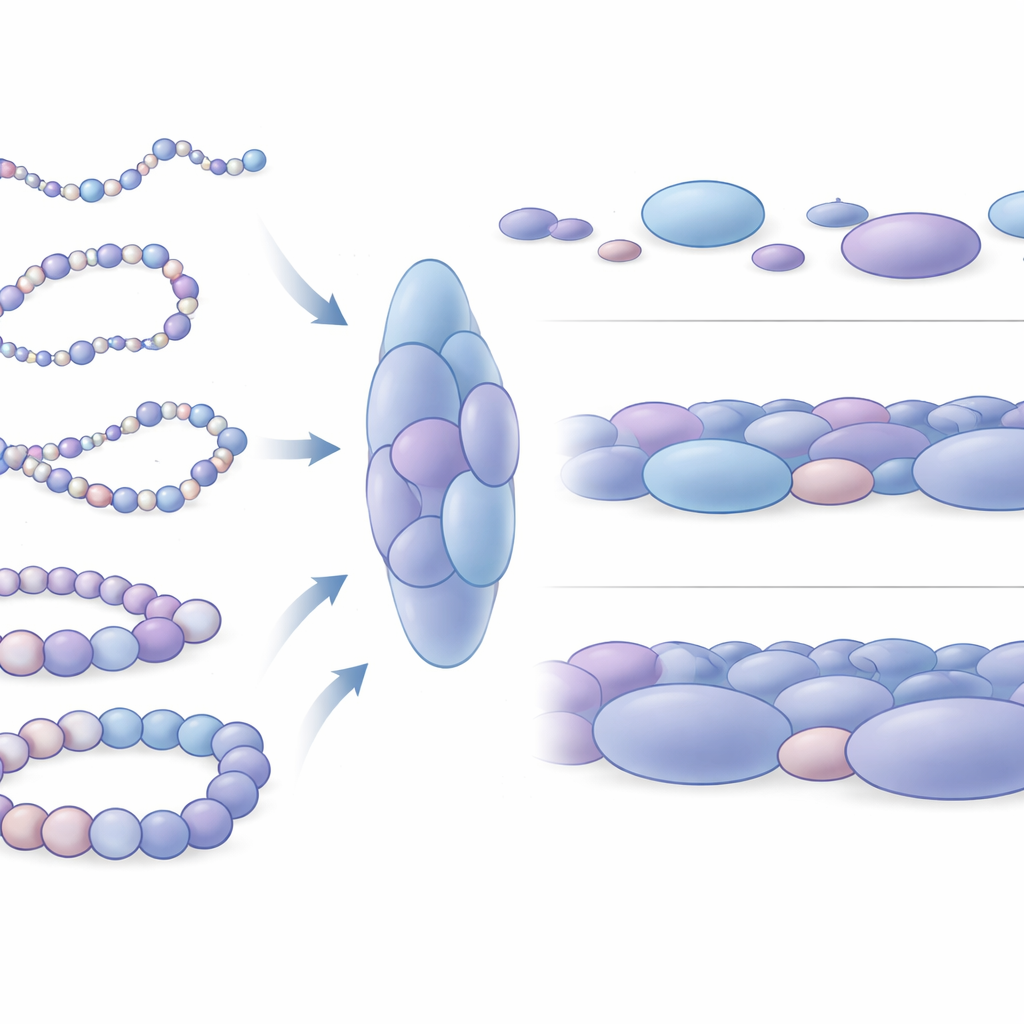
Paketlenme Farkları Gen Aktivitesini Nasıl Yansıtır
Araştırmacılar, bu kümelerin aktif genlerin çevresinde pasif olanlara kıyasla nasıl farklılaştığını incelediler. Kök hücreleri esnek, farklılaşmamış durumda tutmaya yardımcı olan iki gen (Nanog ve Lin28A) ve aynı hücrelerde kapalı olan iki gelişim kontrol geni (HoxB4 ve HoxA13) dahil olmak üzere iyi çalışılmış dört insan DNA bölgesine odaklandılar. Aktif olmayan genlerin çevresinde kümeler ortalamada daha büyük ve daha sıkı paketlenmişti; nükleozomlar daha tam kapanmış yerel düzenlemeler oluşturuyordu. Buna karşılık, aktif genlere yakın kümeler daha küçük, bir nebze daha gevşek ve daha değişkendi. Daha geniş ölçekte, aktif genlerin çevresindeki DNA çok daha fazla farklı şekil örüyordu ve mekanik olarak daha esnekti; oysa sessiz genlerin çevresindeki bölgeler kromatinin daha sert segmentleri gibi davranıyordu. Bu mekanik fark, uzak düzenleyici DNA öğelerinin gen anahtarlarıyla ne kadar kolay karşılaşıp işbirliği yapabileceğini muhtemelen etkiler.
Gen Kontrolünü Anlamada Neden Önemli
Birlikte ele alındığında bulgular, genomun boyutları, şekli ve aralığı yakın genlerin erişilebilir mi yoksa kilitli mi olacağını belirlemeye yardımcı olan dinamik nükleozom kümelerinden inşa edildiği resmini çiziyor. Yeni model, deneysel temas verilerini, nükleozom haritalarını ve fiziksel ilkeleri tek bir çerçevede birleştirerek kök hücre genlerinin esnek ve etkileşimli kalmasını sağlarken gelişim genlerinin daha sert, daha sıkışık mahallelerde saklanmasını açıklıyor. Uzman olmayanlar için kilit fikir şudur: gen aktivitesi yalnızca DNA dizisiyle yönetilmez; aynı zamanda o DNA’nın üç boyutlu yapılara nasıl katlandığına da bağlıdır. Nükleozom kümelerini bu katlanmanın temel yapı taşları olarak ortaya koyarak, bu çalışma mikroskopik genom mimarisini gelişim, hücre kimliği ve hastalık gibi büyük ölçekli süreçlere bağlamanın güçlü bir yolunu sunuyor.
Atıf: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
Anahtar kelimeler: kromatin katlanması, nükleozom kümeleri, 3B genom organizasyonu, gen düzenlenmesi, polimer modelleme