Clear Sky Science · tr
Lecanemab ile ilişkili ARIA'da sitotoksik CD8⁺ T hücrelerinin klonal genişlemesi
Alzheimer hastaları için bunun önemi
Lecanemab, beyindeki amiloidi temizleyebilen ve Alzheimer hastalığında hafıza kaybını ılımlı şekilde yavaşlatabilen ilk ilaçlardan biridir. Ancak bu tedaviyi alan bazı hastalarda manyetik rezonans görüntülemede (MR) görülen beyin ödemi veya küçük beyin kanamaları gelişir; bu değişiklikler amiloide bağlı görüntüleme anormallikleri (ARIA) başlığı altında toplanır. Bu çalışma hastalar ve aileler için kritik bir soruyu gündeme getiriyor: ARIA ortaya çıktığında bağışıklık sisteminde neler oluyor ve bir gün basit bir kan testinin kimin daha yüksek risk taşıdığını öngörmeye yardımcı olup olamayacağı?
Yeni bir Alzheimer tedavisinin vaatleri ve riskleri
Lecanemab, amiloid‑beta adlı proteinin kümelerine yönelik infüzyonla verilen bir antikordur; amiloid, Alzheimer hastalığının karakteristik özelliklerinden biridir. Vücudun amiloidi temizlemesine yardımcı olarak bilişsel gerilemeyi ılımlı biçimde yavaşlatabilir. Ancak bu fayda güvenlik kaygısını da beraberinde getirir: bazı kişilerde beyin ödemi veya mikroskobik kanamalar içeren ARIA gelişebilir. Bu yan etkiler sık MR izlemeyi gerektirir ve ilacı kime verebileceğimizi sınırlayabilir. Herkes aynı derecede duyarlı değildir—APOE4 adı verilen bir gen varyantını taşıyanlar daha yüksek risk altındadır—ancak genler tek başına ARIA'nın neden özellikle tedavi başladıktan hemen sonra ortaya çıktığını açıklamaz. Lecanemab dolaşıma verildiği için yazarlar, kanda bulunan bağışıklık hücrelerini yakından incelemenin erken uyarı işaretleri veya tedavi ile beyindeki damar hasarı arasındaki mekanizmaları ortaya koyabileceğini düşündüler. 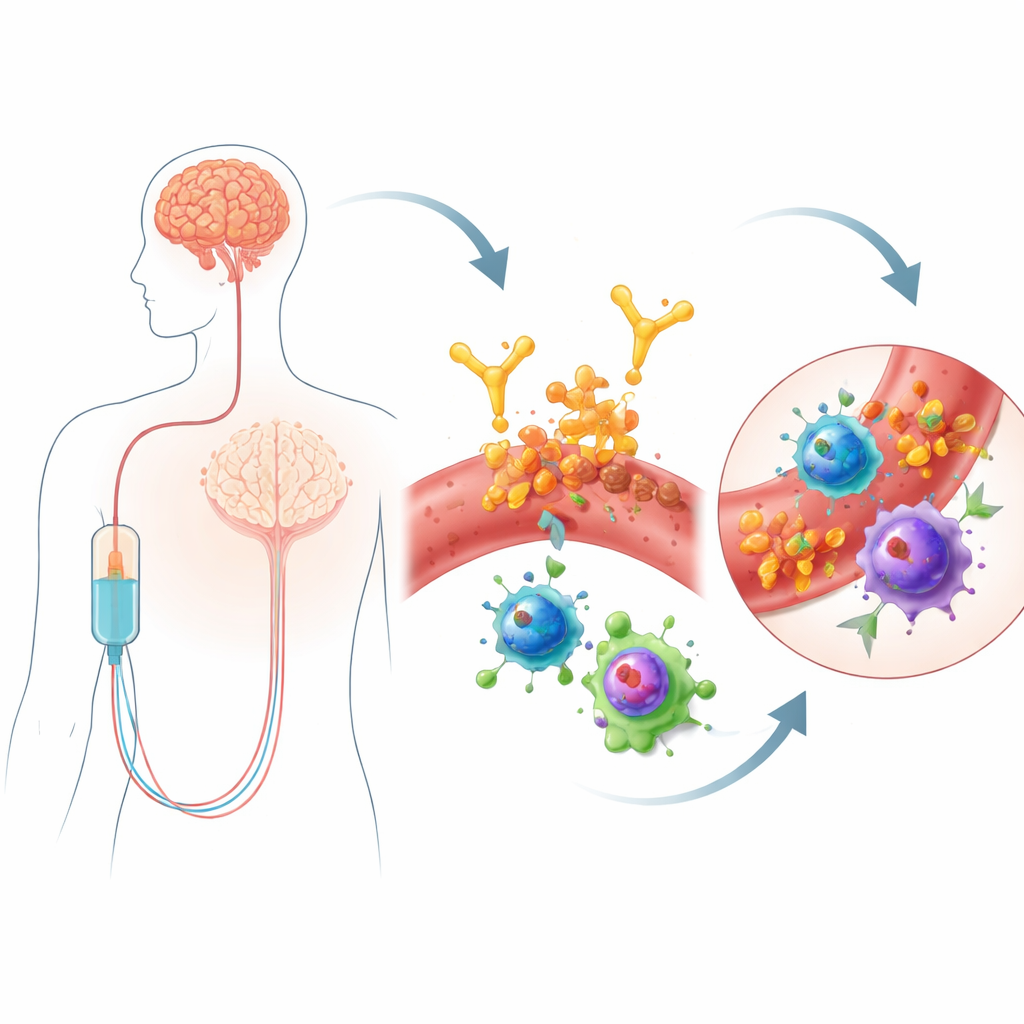
ARIA gelişen ve gelişmeyen hastalarda bağışıklık hücrelerini izlemek
Araştırmacılar bölgesel bir hafıza kliniğinde lecanemab alan altı Alzheimer hastasını inceledi. Üçünde çeşitli ARIA formları gelişti, üçü ise yaş, cinsiyet, APOE genotipi ve infüzyon sayısı bakımından eşleştirilmiş kontrol grubunu oluşturdu. Kan infüzyondan hemen önce alındı ve ekip çok yönlü bir "multi‑omik" yaklaşım kullandı: binlerce tek bir bağışıklık hücresinde hangi genlerin aktif olduğunu okumak için tek hücre RNA dizileme, hücre tiplerini tanımlamak için antikor bazlı etiketler, klonları izlemek için T‑hücre reseptörü dizilemesi ve hücre metabolizmasında rol alan yüzlerce küçük molekülü ölçmek için hedefe yönelik metabolomik. Bu sayede yalnızca hangi hücre tiplerinin var olduğunu değil, ne kadar aktif olduklarını, hangi yakıtları kullandıklarını ve belirli T‑hücre ailelerinin bir tetikleyiciye yanıt olarak çoğalıp çoğalmadıklarını sorgulayabildiler.
Yüksek donanımlı öldürücü T hücrelerinin genişlemesi
ARIA gelişen hastalarda belirgin bir desen ortaya çıktı. Kontrollerle karşılaştırıldığında, bu hastalarda CD8 "öldürücü" T hücrelerinin oranı daha yüksekti, CD4 yardımcı T hücrelerinin oranı daha düşüktü. CD8 havuzunda iki alt grup öne çıktı: efektor bellek hücreleri ve TEMRA olarak bilinen terminal olarak farklılaşmış bir form. Bu TEMRA hücreleri, hedef hücreleri öldürme konusunda güçlü mekanizmalara sahip, saldırı için yüksek düzeyde uzmanlaşmış adeta deneyimli askerler gibidir. ARIA‑pozitif hastalarda TEMRA hücreleri daha fazla sayıda, klonal olarak daha genişlemiş (yani belirli T‑hücre aileleri çoğalmış) ve sitotoksisite, damar yoluyla göç ve kronik uyarı işaretleriyle ilişkili gen programlarını taşıyordu. Benzer T‑hücre durumları yaşlanma, kronik enfeksiyonlar, multipl skleroz ve Alzheimer’lı kişilerin omurilik sıvısında gözlemlenmiş; bu hücreler damarlar ve beyin yüzeyinin yakınında birikebilir.
Metabolik yeniden programlanma ve diğer bağışıklık hücreleriyle iletişim
Ekip ayrıca bu CD8 efektor hücrelerinin metabolizmalarını yeniden programladığını buldu. Mitozondride verimli enerji üretimine dayanmaktansa, daha hızlı ancak daha az verimli olan glikolize yönelmişlerdi; bu, kısa ömürlü yüksek yoğunluklu etkinliği destekleyen bir enerji yolu. Kan hücrelerindeki metabolit ölçümleri bunu doğruladı: laktat ve piruvat düzeyleri artmış, sitrik asit döngüsünün ana bileşenleri azalmıştı; bu desen inflamatuar bağışıklık hücrelerine tipiktir. Monositler (başka bir beyaz kan hücresi türü) tamamlayıcı değişiklikler gösterdi. ARIA‑pozitif hastalarda monositler antijen sunumu, hücrelere yapışma ve T hücrelerini çeken kemokin üretimi için genleri açmıştı. Ligand‑reseptör çiftlerinin hesaplamalı modellemesi, monositlerin CD8 efektor hücrelere daha güçlü aktive edici ve yönlendirici sinyaller gönderdiğini; bunun da bu öldürücü hücrelerin damar duvarlarıyla etkileşime girmesini teşvik eden bir ortam yarattığını öne sürdü.
T hücrelerini beyin damarlarına yönlendiren adres kodları
Bu çalışma yalnızca kandan örnek aldığı için yazarlar, aynı T‑hücre programlarının beyindeki vasküler nişlerle ilişkili olup olmadığını sormak üzere lecanemab tedavisi görmüş hastaların beyinlerine ait bağımsız bir tek‑hücre veri setine başvurdular. CD8 alt gruplarını bu beyin haritasına yansıttıklarında, ARIA‑pozitif hastalardan gelen TEMRA ve efektor bellek hücreleri, endotel (kan damarı) hücreleriyle eşleşen yapışma molekülleri ve kemokin reseptörlerinden oluşan transkripsiyonel "adres kodları" gösterdi. Bu imzalar, genişlemiş öldürücü T hücrelerinin yalnızca iyi donanımlı ve metabolik olarak hazırlıklı olmakla kalmayıp, aynı zamanda amiloid temizliği sırasında strese girmiş beyin kan damarlarına yönelip etkileşime girmeye programlı olduğunu düşündürüyor. 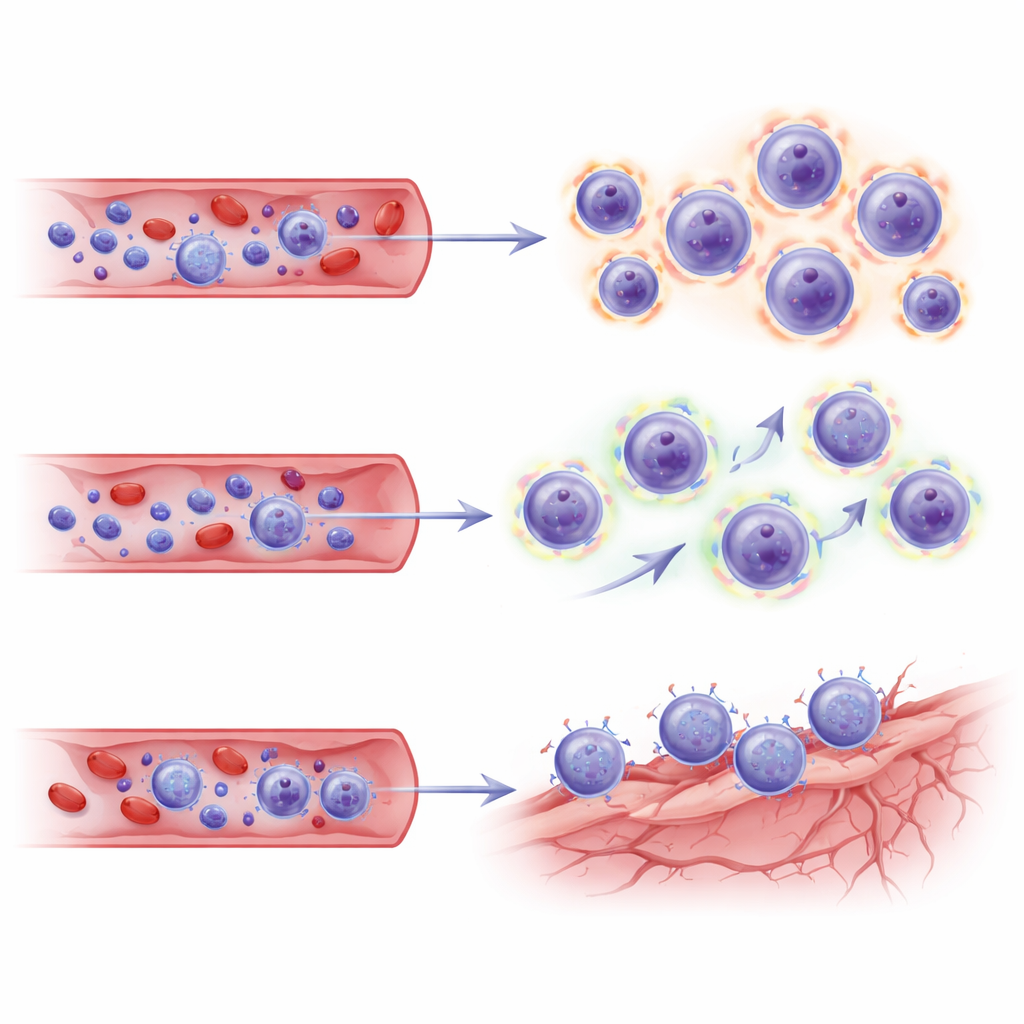
Hastalar ve gelecekteki bakım için olası anlamı
Bir araya getirildiğinde, bu küçük ama ayrıntılı çalışma ARIA'yı amiloid temizliğinin pasif bir yan etkisinden daha fazlası olarak resmediyor. Bunun yerine, kana yansıyıp koordineli bir bağışıklık yanıtıyla ilişkili görünüyor: belirli öldürücü T‑hücre klonlarının genişlemesi ve metabolik aktivasyonu, monositlerden güçlenen sinyalleşme ve beyin kan damarlarıyla etkileşime eğilimli moleküler özellikler. Bu çalışma bu hücrelerin ARIA'ya neden olduğunu kanıtlamıyor—bağışıklık değişiklikleri damar hasarına bir tepki da olabilir—ancak test edilebilir hipotezler ve kan temelli biyobelirteçler için bir yol haritası sunuyor. İleride CD8 TEMRA hücrelerinin bolluğunu ve metabolik durumunu, ilgili ana sinyal molekülleriyle birlikte ölçmek, ARIA için en yüksek riske sahip hastaları saptamaya, izlemeyi yönlendirmeye veya amiloid temizleyici tedavilerin faydalarını korurken bu bağışıklık yanıtını geçici olarak baskılayacak hedefe yönelik stratejileri ilham vermeye yardımcı olabilir.
Atıf: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Anahtar kelimeler: Alzheimer hastalığı, lecanemab, bağışıklık hücreleri, beyin kan damarları, tedavi yan etkileri