Clear Sky Science · tr
TDP-43'e bağlı gizli eklemeden kaynaklanan nörotoksik bir kriptik peptit: PKN1
Hücre içindeki gizli tehditler
Amyotrofik lateral skleroz (ALS) ve Alzheimer hastalığı da dahil olmak üzere birçok beyin hastalığında TDP-43 adlı bir proteinin kümelenmeleri görülür. Bilim insanları, bu protein düzgün çalışmayı kestiğinde sinir hücrelerinin hayati mesajları kaybettiğini ve sonunda öldüğünü biliyor. Bu çalışma daha şaşırtıcı bir ayrıntıyı ortaya koyuyor: TDP-43 işlev bozukluğu, beyin hücrelerinin daha önce bilinmeyen, toksik bir mini‑protein üretmesine de yol açabiliyor; bu mini‑protein ise bellek devrelerine zarar veriyor. Bu gizli oyuncunun anlaşılması, yıkıcı demanslarda tanı ve tedavi için yeni yollar açabilir.
Bir hücresel düzeltmeni nasıl RNA’yı dizginli tutar
Sinir hücreleri içinde TDP-43, DNA ile proteinler arasındaki ara mesajlar olan RNA için bir düzeltmen (proofreader) gibi davranır. Belirli kısa dizilere bağlanır ve bu mesajlara yabancı “fazladan parçaların” eklenmesini engeller. TDP-43 kaybolduğunda veya yanlış konumlandığında —ALS ve birçok Alzheimer vakasında görüldüğü gibi— bu fazladan parçalar, kriptik ekzonlar olarak adlandırılan diziler, RNA’ya sızabilir. Bugüne dek bilinen kriptik ekzonların çoğu, mesajı dengesizleştirip hızla yok edilmesine yol açarak normal proteinin kaybına sebep oluyordu. Bu tür olayların yeni, zararlı proteinler oluşturup oluşturmayacağı net değildi.
Bir kriptik ekleme toksik bir fragman yaratıyor
Yazarlar, nöronların iç iskelesini ve sinyal akışını korumaya yardımcı olan PKN1 adlı bir gène odaklandı. TDP-43’ün azaltıldığı hücre modellerinde, PKN1 RNA’sının iki normal segmenti arasına PKN1‑5a1 adını verdikleri daha önce tanınmamış bir kriptik ekzonun eklendiğini keşfettiler. Bu ekleme erken bir durdurma işareti (stop codon) getirerek kısaltılmış bir RNA üretilmesine neden oluyor. Dikkat çekici şekilde, hatalı mesajın bir kısmı hücrenin kalite kontrol sisteminden kaçıyor ve PKN1 proteininin yalnızca ilk 207 amino asidini içeren stabil bir fragmana çevriliyor. Ekip bu kesilmiş ürüne PKN207 adını verdi. TDP-43’ün normalde bu hatayı, kriptik ekzonu çevreleyen birkaç UG‑zengin bölgeye bağlanarak önlediğini; bu bağlanma kaybolduğunda ekzonun eklendiğini ve PKN207’nin üretildiğini gösterdiler.
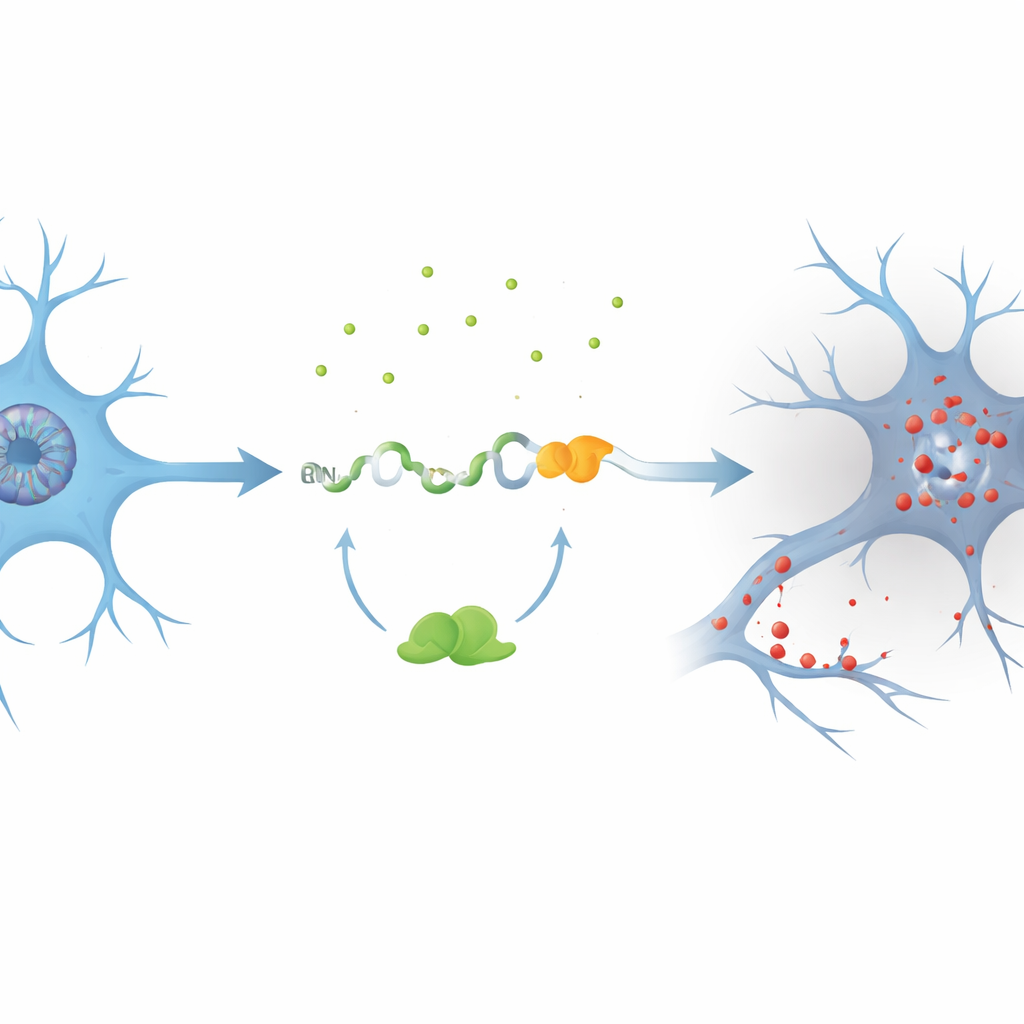
Hastaların beyinleri ve büyük veri kümelerinden kanıtlar
Bu olayın insan hastalığında olup olmadığını görmek için araştırmacılar yüzlerce ALS beyin ve omurilik doku örneğinden elde edilen RNA dizileme verilerini taradılar. PKN1‑5a1 kriptik ekzonunun, motor korteks ve omurilik gibi TDP-43 patolojisinden etkilenen bölgelerde yaygın şekilde aktive olduğunu, nispeten korunmuş olan serebellumda ise bulunmadığını tespit ettiler. Ardından yalnızca PKN207’nin benzersiz kuyruğunu tanıyan, tam uzunluk PKN1 proteinini tanımayan yüksek özgüllükte antikorlar ürettiler. Anormal, fosforillenmiş TDP-43 gösteren Alzheimer hastalarının hipokampus dokusunda bu antikorlar PKN207’ye karşı belirgin bir bant saptadı; kontrol beyinlerde böyle bir bant yoktu. Ek Alzheimer veri kümeleri, kriptik ekzonun hastalığın erken evrelerinde bile etkinleştiğini doğrulayarak bu moleküler hatanın semptomlar ortaya çıkmadan çok önce başlayabileceğini gösterdi.
Bellek üzerinde büyük etkisi olan bir mini‑protein
PKN207’nin hasta insan beyninde bulunması temel soruyu gündeme getirdi: bu zararlı mı? Bunu test etmek için ekip, genç farelerin hipokampusuna —bellek için kritik bir beyin bölgesi— ya normal PKN1 ya da PKN207 üretimini sağlayan virüsleri kullandı. Aylar sonra, her iki fare grubunda da Morris su labirentinde öğrenme bozukluğu görüldü; gizli platformu bulmak için daha uzun yüzüyorlardı. Omurilik sıvılarında akson hasarının bir göstergesi olan nörofilament hafif zincir düzeyi yükselmişti. Kültürdeki nöronlarda PKN207 artışı, membran hasarını gösteren bir enzimin sızmasıyla hücre yaralanmasına yol açtı. Hipokampustaki ayrıntılı protein profillemesi, sinaptik güç (uzun dönem potansiyasyon) ve iyi bilinen nörodejeneratif hastalıklarla bağlantılı yolaklarda geniş değişiklikler ortaya koydu; özellikle etkili sinyal iletimi ve sağlam bir sinir lifi iskelesini destekleyen moleküllerde güçlü bozulma görüldü.
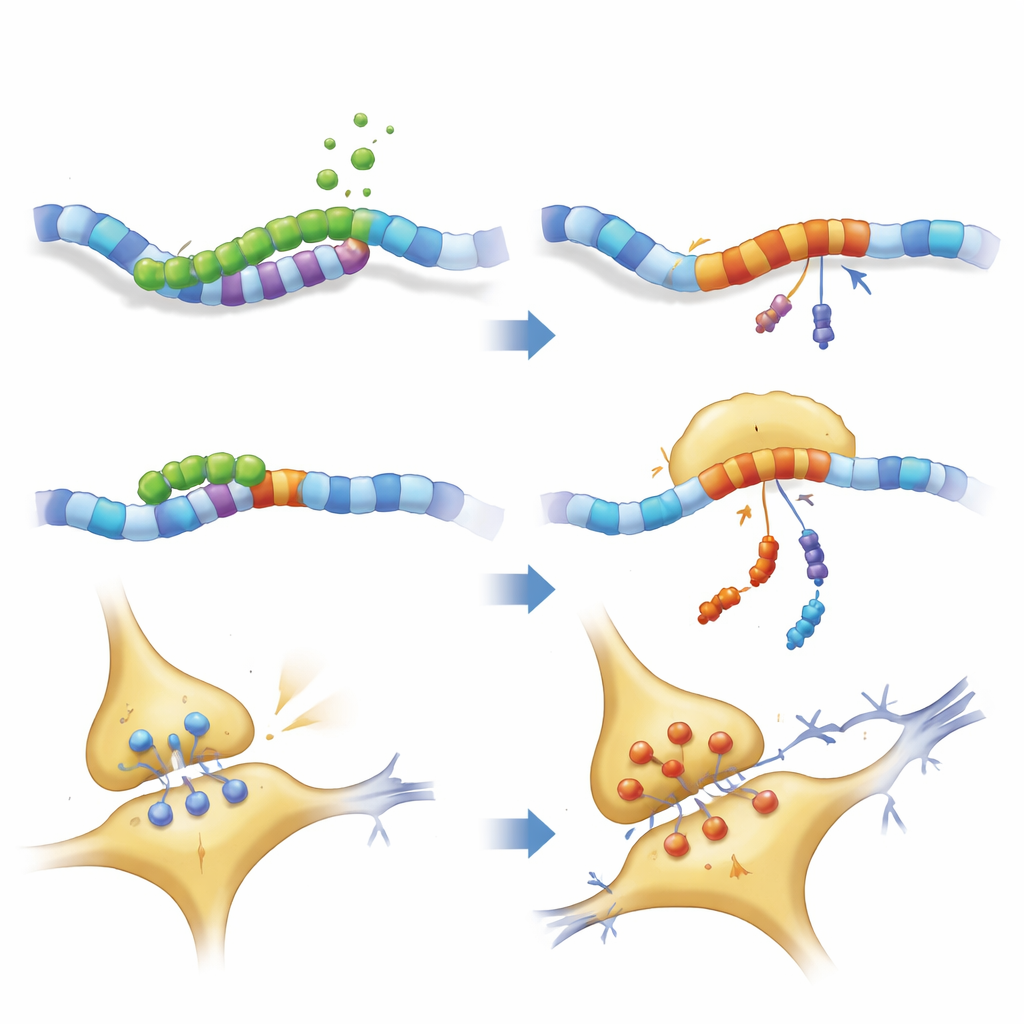
Fragmanın beyin bağlantılarını nasıl bozduğu
Nöronal yapının daha yakından incelenmesi, hem tam uzunluk PKN1’in hem de PKN207’nin aksonlara şekil veren ve taşımayı kolaylaştıran nörofilament ağını bozduğunu gösterdi. Temel motor ve iskelet proteinleri azalmış, bazı nörofilament bileşenleri ise birikmişti; bu durum trafik sıkışmaları ve olası kümeleşmelere işaret ediyor. Hipokampal dilimlerden yapılan elektrik kayıtları, PKN207 eksprese eden farelerde uzun dönem potansiyasyonun zayıfladığını doğruladı — tekrar eden aktivite sonrası sinapsların güçlendiği ve öğrenme ile belleğin hücresel temeli olarak kabul edilen süreç. PKN207, PKN1’in enzim domainine sahip olmamasına rağmen, varlığı tam proteinin yol açtığı bozulmaları taklit etmeye ve bazen aşmaya yetiyordu; bu da paylaşılan N‑terminus bölgesinin tek başına nöronal homeostazı bozabileceğini düşündürüyor.
Bu keşfin beyin hastalıkları için önemi
Bu çalışma TDP-43 ilişkili bozukluklara dair anlayışımıza yeni bir katman ekliyor. TDP-43 eksikliği yalnızca hayati RNA’ların kaybına neden olmakla kalmıyor; aynı zamanda sinapsları ve bilişi zayıflatan stabil, toksik bir mikro‑protein de ortaya çıkarabiliyor. Kriptik PKN1‑5a1 ekzonu ve onun peptit ürünü PKN207, erken TDP-43 disfonksiyonunun potansiyel biyobelirteçleri ve splicing hatasını düzeltmeye veya zararlı fragmanı engellemeye yönelik terapilerin aday hedefleri olarak öne çıkıyor. Daha geniş anlamda, çalışma diğer gizli ekzonların da hastalığa yol açan peptitler üretiyor olabileceğini öne sürerek araştırmacıları nörodejenerasyonda daha önce gözden kaçmış zengin bir moleküler suçlu manzarasına yönlendiriyor.
Atıf: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Anahtar kelimeler: TDP-43, kriptik ekleme, PKN1, nörodejenerasyon, Alzheimer ve ALS