Clear Sky Science · tr
Bir metabolik tiolaz kompleksinin evrimsel amacı değiştirilmesi, antibiyotik biyosentezini mümkün kılıyor
Günlük mikroplar kimyalarını nasıl yeniden icat ediyor
Güvendiğimiz birçok antibiyotik ve ilaç, bakteriler tarafından sessizce üretilir. Bu küçük kimyagerler, karmaşık savunma bileşikleri inşa etmek için enzimler—moleküler makineler—kullanır. Bu çalışma, temel hücresel işlevler için kullanılan bir metabolik enzim kompleksinin, ağız bakterilerinde güçlü bir antibiyotik üretmek üzere evrimsel olarak nasıl yeniden kablajlandığını ortaya koyuyor. Bu dönüşümü anlamak yalnızca doğanın yeni kimya nasıl icat ettiğini açığa çıkarmakla kalmaz, aynı zamanda bir sonraki nesil ilaçlar ve biyokatalizörler tasarlamak için ipuçları sunar.
Temel metabolisizmden kimyasal silaha
Bütün yaşayan hücreler, yağları parçalamak ve temel moleküller inşa etmek gibi merkezi metabolizmalarını yürüten korunmuş enzimlere bağımlıdır. Tiolaz süper ailesi olarak adlandırılan bu gruplaşma, normalde asetil-CoA gibi küçük enerji açısından zengin moleküllerle uğraşmaya yardımcı olur ve lipidler ile diğer hücre bileşenlerinin yapımı için hayati yolları destekler. Yazarlar, birkaç oral Streptococcus türünde HMGS, ACAT ve üçüncü bir yardımcı proteine ilişkin proteinlerden oluşan üç parçalı tiolaz bazlı bir kompleksin atalarının metabolik rolünü terk ettiğini keşfettiler. Bunun yerine bu kompleks şimdi, bu bakterilerin ağızdaki yoğun rekabet ortamında avantaj sağlayan reutericyclin A adlı bir antibiyotiğin biyosentezini tamamlıyor.
Antibiyotik iskeleti üzerinde yeni tür bir enzim reaksiyonu
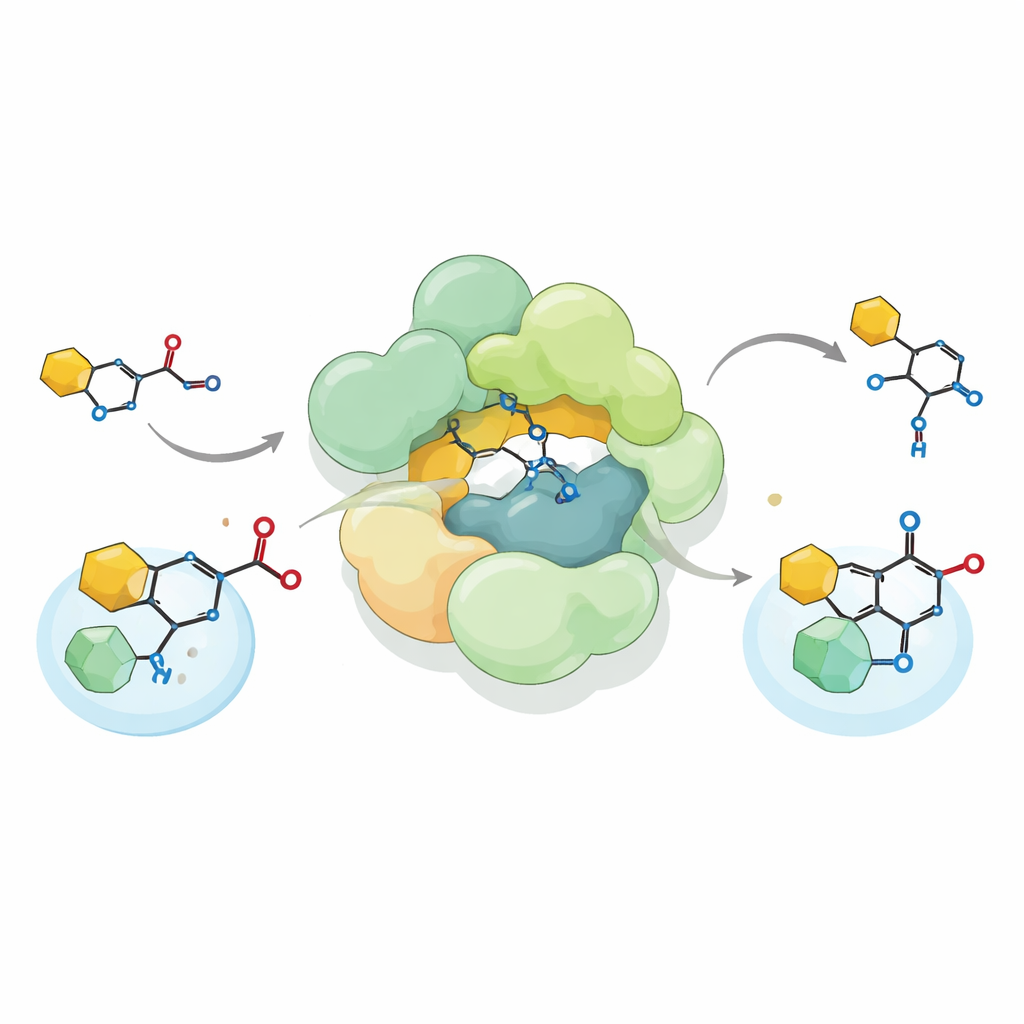
Streptococcus kompleksini laboratuvarda yeniden oluşturup ona reutericyclin A’nın kimyasal olarak sentezlenmiş bir öncülünü vererek, araştırmacılar kompleksin Friedel–Crafts C-asilasyonu olarak bilinen sıra dışı bir karbon–karbon bağ oluşturma reaksiyonunu gerçekleştirdiğini gösterdiler. Pek çok enzimin oksijene asetil grubunu bağlamasının aksine, bu kompleks asetil grubunu reutericyclin iskeletinin önemli bir parçası olan pirrolidin-2,4-dion halkasının bir karbon atomuna doğrudan yerleştiriyor. Kompleks hem asetil-CoA gibi doğal asetil vericilerini hem de birkaç yapay vericiyi kabul ediyor ve hatta oluşturduğu bağı tersine çalıştırıp kırabiliyor. Bu esneklik biyolojik asiltransferazların bilinen repertuarını genişletiyor ve bu tür enzimlerin çeşitli kimyasal ürünleri inşa etmek üzere nasıl uyarlanabileceğine dair ipuçları veriyor.
Korunmuş bir protein iskeletinin amaç değiştirmesi
Yüksek çözünürlüklü kriyo-elektron mikroskobu kullanarak ekip, SmaATase olarak adlandırılan Streptococcus kompleksinin üç boyutlu yapısını çözdü. Yeni işlevine rağmen, SmaATase izoprenoid lipidlerin yapımı için mevalonat yoluna katılan arkeal bir ilgili komplekse çarpıcı bir mimari benzerlik gösteriyor. Her ikisi de tekrarlayan modüllerden oluşan büyük multimetrik yapılardır ve KoA kofaktörünün bağlanabileceği ve aktif bölgeler arasında hareket edebileceği ortak bir boşluğu paylaşır. Ancak orijinal metabolik reaksiyon için gerekli anahtar katalitik residueller bakteriyel versiyonda eksik veya değiştirilmiştir. Biyokimyasal testler, SmaATase’in artık atasal ürünü HMG-CoA yapamadığını ve bunun yerine asetil-CoA’yı yeni küçük molekül alt katmanları için yalnızca bir verici olarak kullandığını doğruluyor.
Metabolisizmden antibiyotiklere uzanan evrimsel bir iz
Böyle bir amaç değişikliğinin nasıl gelişmiş olabileceğini anlamak için yazarlar, ilgili komplekslerin dizilerini ve aktivitelerini birçok bakteri ve arkede karşılaştırdılar. Aynı üçlü enzim tipini içeren binin üzerinde gen kümesi belirlediler. Bazıları klasik tiolaz kimyasını hala destekliyor; Pseudomonas’taki bazıları ise farklı küçük-molekül antibiyotikleri besliyor. Pseudomonas fluorescens’den temsilî bir kompleks bu evrimsel yol boyunca kısmen ilerlemiş gibi görünüyor: HMGS-benzeri domaini etkisizleştirilmiş, ancak ACAT-benzeri birimi hâlâ KoA-bağlı substratlar üzerinde daha geleneksel bir reaksiyon gerçekleştiriyor. SmaATase ve tarımı koruyucu DAPG bileşiğini yapan Pseudomonas muadili gibi örneklerde, aktif bölgelerin çevresindeki daha ileri değişiklikler enzimleri aromatik halkalar veya tetramik asit çekirdekleri gibi standart olmayan kabul edicileri tanıyacak şekilde şekillendirmiştir.
Neden küçük bir asetil grubu büyük fark yaratır
Sonuç olarak, bu moleküler makyajın biyolojik getirisi açıktır. Ekip asetillenmiş antibiyotikler reutericyclin A ve DAPG’yi Gram-pozitif bakteriler paneline karşı test ettiğinde, bu moleküller güçlü öldürücü aktivite gösterirken, asetillenmemiş öncülleri çok daha zayıf veya neredeyse etkisizdi. Yeniden amaçlanmış enzim kompleksi tarafından tam doğru konuma yerleştirilen bu küçük asetil grubu, mütevazı bir iskeleti güçlü bir silaha çeviriyor; ağızdaki Streptococcus’un veya bitki kökleri çevresindeki Pseudomonas’ın komşularını geride bırakmasını sağlıyor. Bu çalışma, evrimin mevcut enzim çerçevelerini asgari ama stratejik mutasyonlarla nasıl geri dönüştürebileceğini, rutin metabolik makineleri kimyasal savunma için uzmanlaşmış araçlara nasıl dönüştürebileceğini gösteriyor—ve ilaç keşfi ile sentetik biyoloji için karbon–karbon bağları oluşturan yeni katalizörler tasarlamak isteyen mühendisler için bir yol haritası sunuyor.
Atıf: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Anahtar kelimeler: enzim evrimi, doğal ürün biyosentezi, antibiyotik kimyası, metabolik amaç değiştirme, Friedel–Crafts asilasyon