Clear Sky Science · tr
İnsan iPSC Tabanlı Akciğer Fibrozisi Modellemesi: p300/CBP İnhibisyonunun Alveolar Geçiş Hücre Durumunu Bastırdığını Ortaya Koyuyor
Neden yara dokusu oluşan akciğerler hepimizi ilgilendirir
İdiopatik pulmoner fibrozis (IPF), akciğerlerin yavaşça yara dokusuna dönüşerek her nefesi zorlaştırdığı amansız bir hastalıktır. Mevcut ilaçlar bu süreci yalnızca yavaşlatabiliyor ve sıklıkla rahatsız edici yan etkilere yol açıyor. Bu çalışma, yara bağlamış akciğerleri laboratuvarda yeniden yaratmak için son teknoloji kök hücre ve genomik araçlar kullanıyor ve basit ama hayati bir soruyu soruyor: hasar görmüş akciğer hücrelerini zararlı bir durumdan uzaklaştırıp iyileşmeye doğru yönlendirebilecek bir anahtar bulabilir miyiz?
Laboratuvarda büyütülmüş bir yara akciğerine bakış
IPF’yi incelemek için araştırmacılar, insan indüklenmiş pluripotent kök hücrelerinden (iPSC’ler) mini akciğerler inşa ettiler. Bu iPSC’ler, oksijenin kana geçtiği küçük hava keseciklerini döşeyen alveolar hücrelere yönlendirildi ve yara dokusu oluşturan bağ dokusu hücreleri olan akciğer fibroblastlarıyla birlikte büyütüldü. Yumuşak bir jelin içine yerleştirilen bu “alveolar organoidler” gerçek akciğer dokusuna çok benzer davrandı. Kemoterapi ilacı bleomisine maruz bırakıldıklarında—akciğer hasarını tetikleyen bilinen bir ajan—jeller fibroblastların çekmesiyle küçüldü ve fibroziste görülen doku büzüşmesini taklit etti.
Bu sistemi kullanarak ekip 264 küçük molekülden oluşan bir kütüphaneyi taradı ve her bir ilacın jelin büzülmesini ne ölçüde engellediğini otomatik olarak ölçtü; objektif sonuçlar için derin öğrenme tabanlı görüntü analiz aracı kullanıldı. Birçok bileşik etkisizdi, ancak bir aile açıkça öne çıktı: DNA’nın paketlenmesini ve hangi genlerin açık olduğunu kontrol etmeye yardımcı olan p300 ve CBP proteinlerinin inhibitörleri. Kütüphanedeki p300/CBP hedefli sekiz bileşiğin tamamı düşük dozlarda büzülmeyi azalttı ve bu yolun fibrozise müdahale etmek için umut verici bir hedef olduğunu vurguladı. 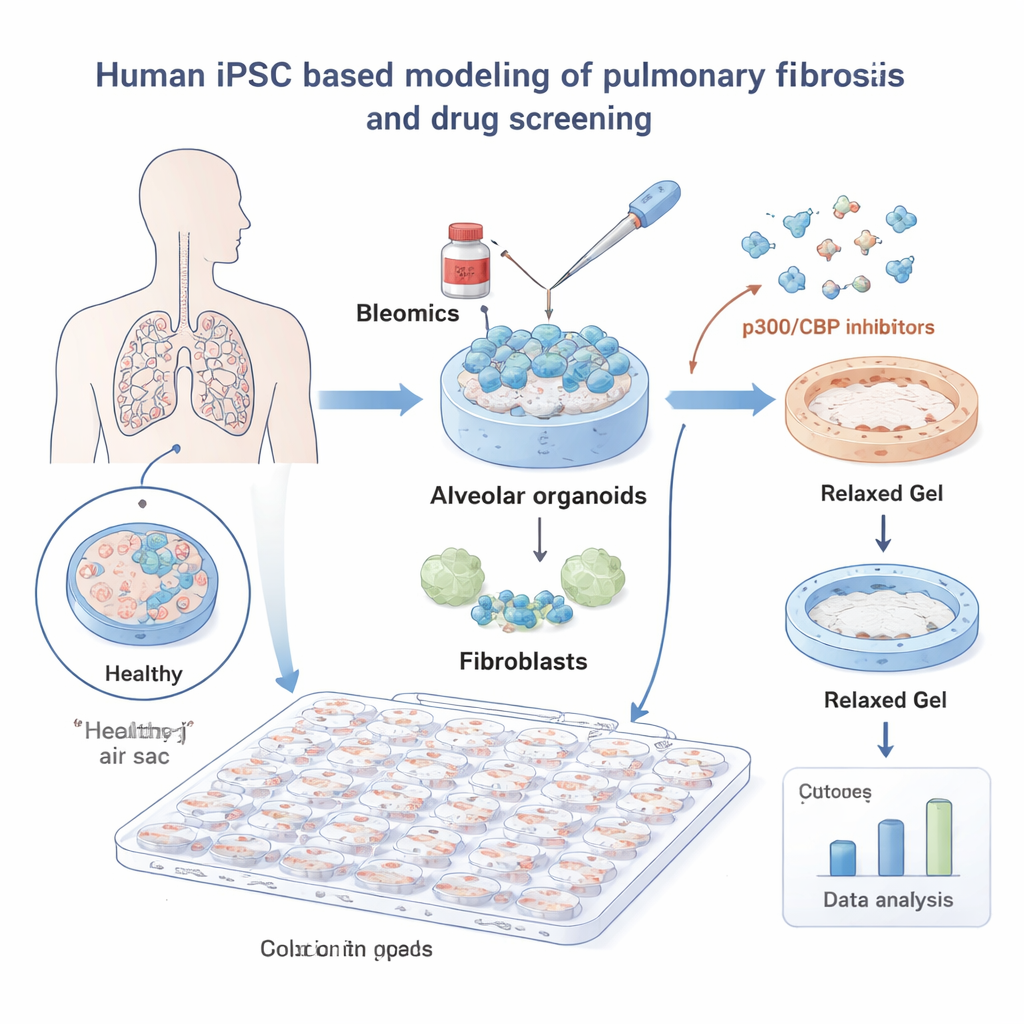
Sorun çıkaranlar: geçiş halindeki akciğer hücreleri
Son çalışmalar, hastalıklı akciğerlerde problem yaratan “arada” bir hücre tipi olduğunu açığa çıkardı: alveolar geçiş hücre durumu. Normalde AT2 olarak bilinen destek hücreleri, hava keseciklerini örten ve gaz değişimini sağlayan ince AT1 hücrelerine olgunlaşır. Ancak IPF’de AT2 hücreleri sık sık bu geçiş durumunda takılı kalır, stres ve onarım genlerini ifade ederler ama tam işlevli AT1 hücrelerine dönüşümü tamamlayamazlar. Bu geçiş hücreleri fibrotik bölgelerde kümelenir ve fibroblastlarla güçlü iletişim kurar; ancak onların yalnızca hasarın bir yan ürünü mü yoksa yara oluşumunun aktif sürücüleri mi olduğu belirsizdi.
Organoidlerinde RNA dizileme ve açık kromatin profillemesi yaparak, yazarlar modellerinde ortaya çıkan geçiş hücrelerinin IPF hastalarından alınan akciğerlerde bulunanlarla yakından eşleştiğini gösterdiler. Bu indüklenmiş geçiş hücreleri stres, iltihap ve matris yeniden düzenlemesine dair gen imzaları sergiledi ve ortak kültürde bulunan erişkin akciğer fibroblastlarını güçlü biçimde aktive etti. Kritik olarak, p300/CBP bloke edildiğinde geçiş durumunun belirteçleri düştü, AT2 kimliği daha iyi korundu ve fibroblast aktivasyonu azaldı. Başka bir deyişle, ilaçlar hücreleri genel olarak zehirlemedi; bunun yerine AT2 hücrelerinin bu zararlı ara duruma takılmasını seçici olarak engelledi.
Moleküler anahtarları çözmek
p300/CBP’nin bu kader kararını nasıl şekillendirdiğini anlamak için ekip, DNA’yı paketlemeye yardımcı olan histonlar üzerindeki kimyasal işaretleri inceledi. Özellikle H3K27 asetilasyonu adı verilen bir işaret, etkin enhance ve promotör bölgelerine p300/CBP tarafından sıklıkla konur. Geçiş hücrelerinde stres yanıtı ve pro‑fibrotik genlerin yakınındaki bölgeler güçlü H3K27 asetilasyonu taşıyor ve AP‑1 ve HNF1B gibi transkripsiyon faktörlerinin bağlanma bölgeleri açısından zengindi. Hücreler p300/CBP inhibitörleriyle tedavi edildiğinde, bu bölgelerdeki asetil işaretleri azaldı ve birçok pro‑fibrotik genin ifadesi düştü. AP‑1’i doğrudan engellemek ya da küçük interfering RNA’larla AP‑1 ve HNF1B’yi azaltmak da benzer şekilde geçiş programını ve organoid büzülmesini kısıtladı; bu da p300/CBP, AP‑1 ve HNF1B üçlüsünü fibrotik yeniden yapılanmayı besleyen motorla ilişkilendiriyor.
Plak ötesinde, çalışma bir inhibitörü, CBP30’u, bleomisin ile indüklenen akciğer hasarı olan farelerde test etti. CBP30 verilen hayvanlarda daha az geçiş epitelyal hücresi, yara oluşturan miyofibroblastların daha az aktivasyonu ve fibrozis belirteçlerinin azalmış ifadesi görüldü. İnsan kök hücre modelleri ile hayvan modeli arasındaki bu çapraz doğrulama, p300/CBP’nin yalnızca laboratuvar yapaylığı olmadığını, akciğer skarlaşmasının gerçek bir düzenleyicisi olduğunu güçlendiriyor. 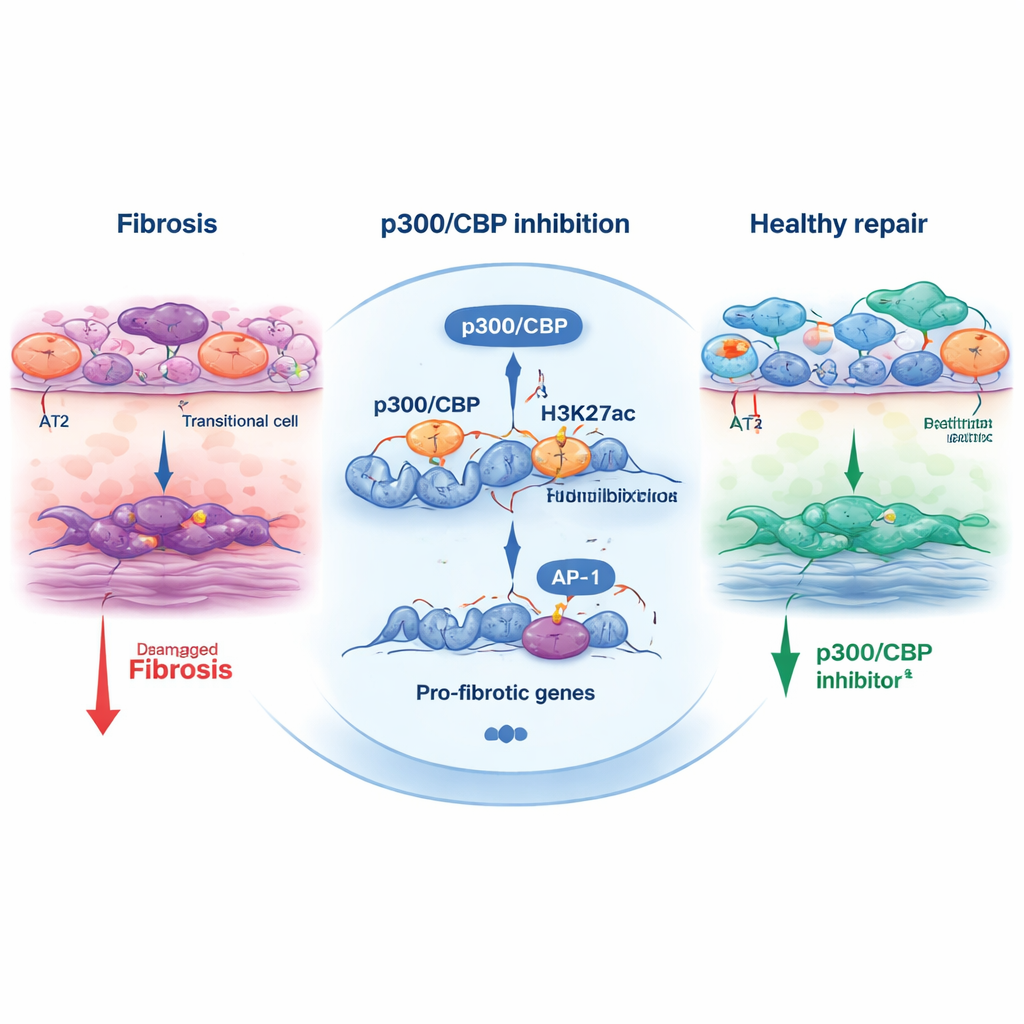
Gelecekteki tedaviler için ne anlama geliyor
Uzman olmayanların anlaması için ana çıkarım şudur: yazarlar fibrotik akciğerlerin gerçekçi bir insan modelini kurdu ve bunu yeni bir ilaç hedefini ön plana çıkarmak için kullandı. Bulguları, akciğer skarlaşmasının kısmen çevre dokuyu yanlış yönlendiren geri döndürülebilir, stres kaynaklı bir geçiş hücre durumu tarafından yönlendirildiğini öne sürüyor. p300/CBP’yi azaltarak bu durum susturulabilir, alveolar hücrelerin sağlıklı bir gelişim yolunda kalması sağlanabilir ve fibroblastları aşırı çalışmaya iten sinyaller azaltılabilir. p300/CBP inhibitörlerinin güvenlik açısından optimize edilmesi ve klinik olarak test edilmesi gerekse de bu çalışma, IPF’de sadece sonuçları yavaşlatmak yerine altta yatan hücresel iletişimsizliği hedef alan tedavilere işaret ediyor.
Atıf: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
Anahtar kelimeler: idiopatik pulmoner fibrozis, alveolar organoidler, p300/CBP inhibitörleri, geçiş epitel hücreleri, akciğer kök hücreleri