Clear Sky Science · tr
Sentetik replikasyon kökenlerine sahip plazmitlerin tasarımı
Mikrobiyel DNA’yı Yeniden Yazmanın Önemi
İnsülin üretiminden gelişmiş gen devrelerine kadar modern biyoteknolojinin arkasındaki birçok araç, plazmit adı verilen küçük DNA halkalarına dayanır. Bu genetik işçilerin görevi, mühendislik ürünü genleri bakterilere taşımaktır, ancak temel tasarımları onlarca yıldır neredeyse değişmedi. Bu çalışma, plazmitlerin tam merkezinde yer alan — hücrelere ne zaman ve ne sıklıkta kopyalanacaklarını söyleyen — dizilerin tamamen yeniden tasarlanabileceğini gösteriyor. Bu "kopyalama motorunu" baştan inşa ederek yazarlar, ayarlanması, birleştirilmesi ve programlanması daha kolay plazmitler yaratıyor; bu da daha esnek tanı yöntemleri, biyolojik üretim ve sentetik biyoloji için yeni imkânlar açıyor.
Gizli Sınırlara Sahip Eski Araçlar
Plazmitler doğal olarak hareketli DNA olarak evrimleşti; bakterilerin antibiyotik direnci veya yeni besinleri sindirme gibi özellikleri paylaşmasına yardımcı oldular. Laboratuvarda mühendisler bu plazmitleri faydalı genleri taşımak için ödünç alır, fakat çoğu, 1980’lerde keşfedilen birkaç klasik tasarıma dayanır. Bu eski tasarımlar, bir plazmitin her hücrede kaç kopya bulunduğunu ve farklı plazmitlerin uyum içinde birlikte yaşayabilip yaşayamayacağını kontrol eden birbirine geçmiş genetik parçalar yumağını saklar. Bu parçalar birbirine bağlı olduğunda bir özelliği değiştirmek başka bir özelliği öngörülemeyen şekilde bozabilir. Sonuç olarak, bilim insanları sabit kopya sayılarına ve sınırlı uyumluluğa sahip sınırlı bir plazmit menüsüyle kısıtlanmış durumda; bu da karmaşık mühendislik sistemlerinin sınırlarını daraltıyor.
Kopyalama Motorunu Baştan İnşa Etmek
Araştırmacılar, pMB1 plazmit ailesinden yaygın olarak kullanılan bir replikasyon kökenine odaklandı. Doğal formunda bu köken, plazmit sayısını kontrol altında tutmak için birini başlatan ve diğerinin kapatan iki RNA arasında ince dengelenmiş bir konuşma kullanır. Ekip ilk olarak bu sistemi "yeniden düzenledi": örtüşen genleri ayırdılar, gömülü bir promotörü devre dışı bıraktılar ve ana parçaları ayrı, temiz genetik kasetlere yerleştirdiler. Bu adım, kökenin temel işlevinin korunabileceğini ve düzenin basitleştirilebileceğini göstererek, evrim tarafından şekillendirilmiş karışık bir parçayı daha modüler, erişilebilir bileşenlere sahip bir makineye dönüştürdü.
Sentetik Kontrol Düğmelerinin Takılması
Orijinal kontrol mantığı açığa çıkınca yazarlar bunu tamamen sentetik düzenleyicilerle değiştirdiler. Replikasyon primerini, dimmer düğmeleri gibi davranan tasarlanmış RNA anahtarlarına bağladılar: küçük kontrol RNA’ları bu anahtarları açıp kapatarak primer üretimini ve dolayısıyla plazmit kopyalanmasını izin verebilir veya engelleyebilir. Farklı anahtar varyantları ve farklı güçte promotörlerle eşleştirerek plazmit kopya sayılarını iki kat mertebeden fazla bir aralıkta ayarladılar. Ayrıca kontrol kasetlerinin DNA üzerindeki farklı fiziksel düzenlerini araştırdılar; bu, stabiliteyi artıran düzenlemeleri keşfetmelerini sağladı ve replikasyon bölgesini kompakt, işlevsel bir çekirdeğe küçültürken sorunlu plazmit etkileşimlerini önleyen doğal yardımcı sistemlerin eklenmesine izin verdi.
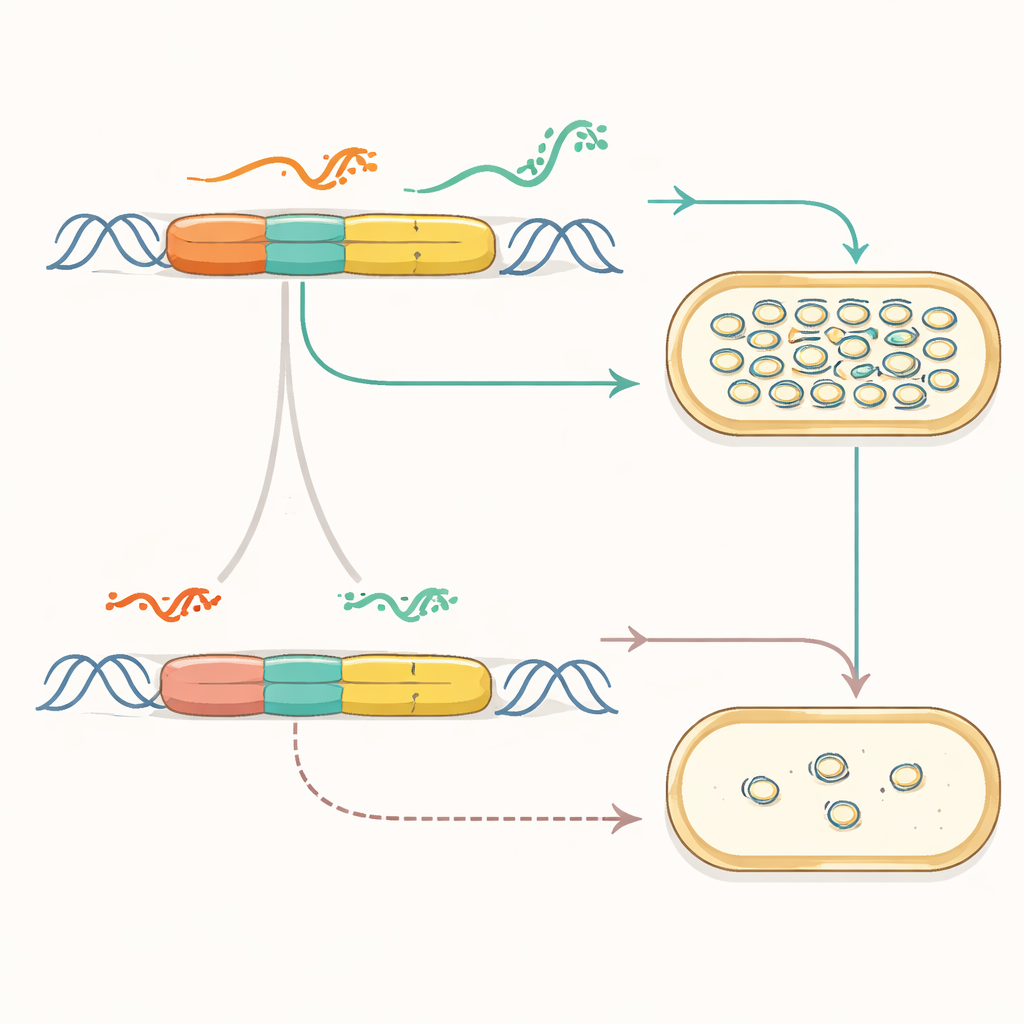
Kimyasal Sinyalleri DNA Kopya Sayısına Çevirmek
Kopyalama motoru modüler hale geldiğinde ekip bunun dış dünyayı algılayacak şekilde bağlanabileceğini gösterdi. Sentetik kökeni indüklenebilir promotörlere ve küçük moleküllere yanıt verip şekil değiştiren riboswitch adı verilen RNA yapılara bağladılar. Bu yeni plazmitlerde IPTG veya cumate gibi bir kimyasal eklendiğinde plazmit kopya sayısı — dolayısıyla bir rapor sinyali — yükseldi veya düştü. Birden çok sinyal birleştirilebiliyordu; örneğin bir kimyasal kopyalamayı tetiklerken başka bir kimyasal bunu sınırlayabiliyordu. Araştırmacılar, her biri farklı bir kimyasala yanıt veren plazmit çiftleri bile inşa etti ve aynı hücrede DNA dizilemesi kullanarak bunların değişen kopya sayılarını izlediler; böylece plazmit sayımlarını çevresel geçmişin bir barkoduna dönüştürdüler.
Tek Bir Hücrede Birden Çok Özel Plazmit
Bu yaklaşımın kilit testi, birkaç bağımsız kontrollü plazmitin birlikte var olup olamayacağıydı. Ortogonal RNA düzenleyiciler kütüphanesinden yararlanarak ekip, her biri kendi sentetik kökenine ve antibiyotik belirtecine sahip altı farklı plazmit inşa etti ve hepsini aynı anda E. coli’ye tanıttı. Birkaç gün boyunca yapılan tam plazmit dizilemesi, hepsinin varlığını sürdürdüğünü doğruladı; her ne kadar göreli bollukları değişse de. Aynı işlemi altı geleneksel plazmitle yapma girişimleri başarısız oldu; bu da yeniden düzenlenmiş tasarım ve eklenen stabilite sistemlerinin yeni plazmitleri tek bir hücrede bir araya geldiklerinde daha uyumlu ve dayanıklı kıldığını vurguluyor.
Geleceğin Biyoteknolojisi İçin Anlamı
Uzman olmayan birine çıkarılacak sonuç basit: yazarlar plazmitleri katı, tek beden araçlardan özelleştirilebilir bir platforma dönüştürdü. Onların sentetik replikasyon kökenleri, hızı, hassasiyeti ve girdileri istenildiği gibi seçilebilen tak-çalıştır motorlar gibi davranıyor. Bu, bakterilerin kimyasal maruziyetleri DNA kopya sayısındaki değişiklikler olarak kaydetmesini, birçok genetik yolun paralel olarak test edilmesini (bunları birden çok plazmit arasında dağıtarak) veya endüstriyel suşlarda büyüme ile üretimi hassas biçimde dengelemesini mümkün kılıyor. Bazı stabilite ödünleri devam etse de bu çalışma, plazmit replikasyonunun temel mekaniğinin artık mühendislik dışı olmadığını gösteriyor ve sentetik biyoloji alanında yeni yeniliklere alan açıyor.
Atıf: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Anahtar kelimeler: sentetik plazmitler, replikasyon kökeni, RNA düzenleyicileri, kopya sayısı kontrolü, sentetik biyoloji