Clear Sky Science · tr
Potansiyel bağımlı polaron oluşumu TiO2'yi hidrojen evrimi reaksiyonu için aktive ediyor
Pas Benzeri Malzemeleri Temiz Yakıt Üreticilerine Dönüştürmek
Su moleküllerini hidrojen yakıtına ayırmak genellikle pahalı değerli metallere dayanır. Bu çalışma, titanyum dioksit (TiO2) adıyla bilinen yaygın ve kararlı bir oksidin, üzerine uygulanan elektrik potansiyelinin değiştirilmesiyle yavaş reaksiyon veren halden son derece aktif bir hale geçirilebileceğini gösteriyor. Anahtar, yüzeyde oluşan küçük, geri dönüşümlü yük ceplerinin — polaronların — yaratılması; bunlar hidrojen gazı üretimi için yeni ve verimli yollar açıyor.
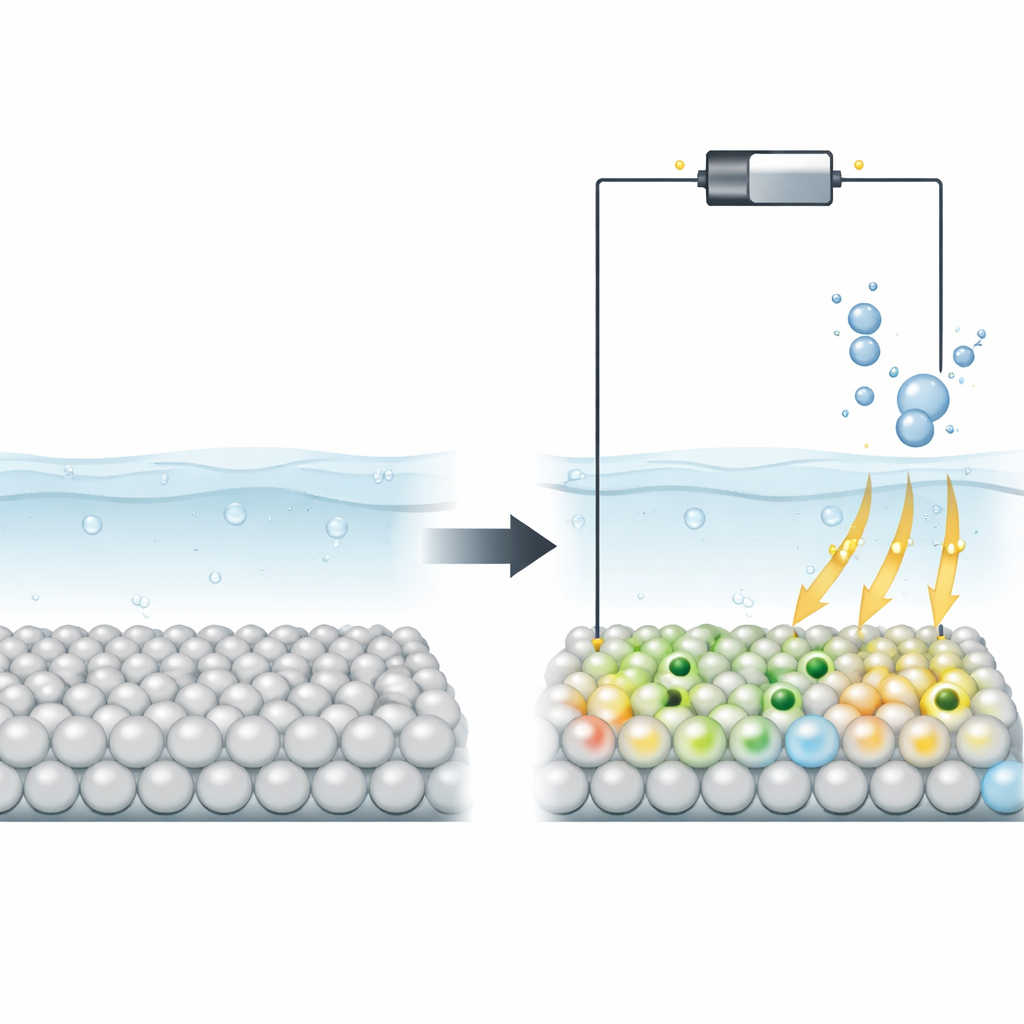
Yarıiletkenlerin Neden Zorlandığı ve Kusurların Nasıl Yardımcı Olduğu
TiO2 gibi yarıiletkenler, ucuz, bol bulunan ve güneş ile fotokatalitik uygulamalarda zaten yaygın olarak kullanıldıkları için temiz enerji açısından çekici. Ancak saf halleriyle elektrik iletkenlikleri zayıf olabilir ve reaksiyon ara ürünlerine ya çok güçlü ya da çok zayıf bağlar vererek vasat katalizörler haline gelirler. Araştırmacılar bunu sentez sırasında eksik atomlar veya yapısal bozukluklar gibi kalıcı kusurlar oluşturarak düzeltmeye çalıştı. Bu kalıcı değişiklikler performansı artırabilse de hassas kontrolü zor ve atomik ölçekte bu kusurların hidrojen evrimi gibi reaksiyonları hızlandırmak için yüzeyi nasıl değiştirdiği belirsiz kaldı.
Voltajla Anahtarlanabilen Yük Cepleri Oluşturmak
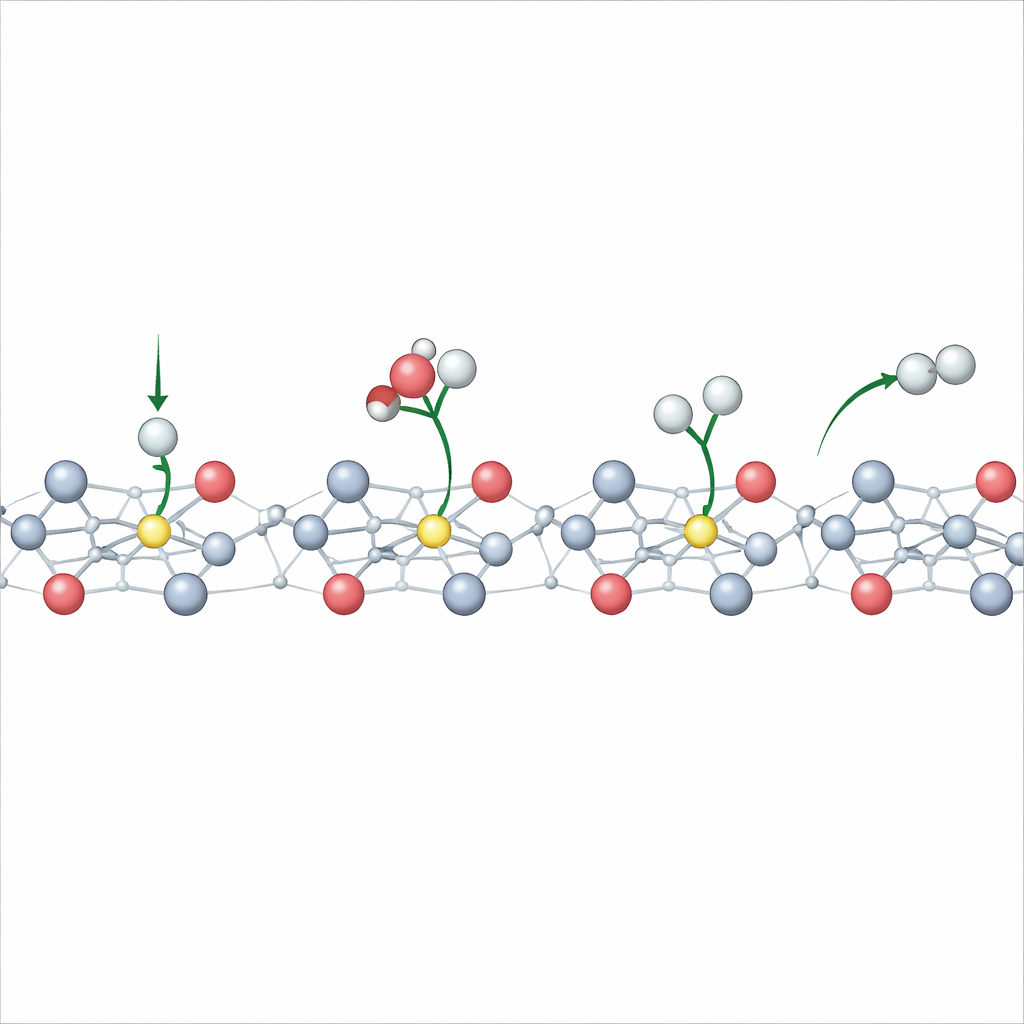
Yazarlar farklı bir strateji öneriyor: TiO2'nin elektronik yapısını çalışma voltajını kullanarak gerçek zamanlı olarak şekillendirmek. Yeterince negatif bir potansiyel uygulandığında, yüzeydeki bazı titanyum iyonları daha yüksek oksidasyon halinden daha düşük bir hale geçer ve ekstra elektronları polaron olarak bilinen lokalize bölgelerde tuzaklar. İleri düzey sabit-potansiyel kuantum hesaplamaları ile in situ spektroskopik ölçümleri birleştiren ekip, bu polaronların yalnızca indirgenme koşullarında oluştuğunu, en üst atomik tabakayla sınırlı olduğunu ve potansiyel çevrildikçe görünür ve kaybolur şekilde geri dönüşümlü davrandığını gösteriyor. Bu, katalizörün aktif yüzeyinin imalat sırasında sabitlenmek yerine işletme sırasında dinamik olarak ayarlanabileceği anlamına geliyor.
Kusurlar, Hareket Eden Yükler ve Daha Hızlı Hidrojen Salımı
Çalışma ayrıca TiO2 yüzeyinde zaten bulunan oksijen boşlukları — gerçek malzemelerde yaygın olan eksik oksijen atomları — olduğunda neler olduğunu inceliyor. Bu boşluklar ekstra elektronların belirli titanyum atomları yakınında kalmasını teşvik ederek, polaronların daha az negatif voltajlarda oluşmasını kolaylaştırıyor. Simülasyonlar birden fazla polaronun zincirler halinde hizalanıp komşu atomlar arasında atlayabildiğini ve böylece yüzey iletkenliğini büyük ölçüde artırdığını ortaya koyuyor. Manyetik sinyalleri ve yük transferini izleyen deneyler, kusurlu TiO2'nin bu yük ceplerini daha fazla biriktirdiğini ve elektronları saf TiO2'ye kıyasla daha kolay taşıdığını doğruluyor. Sonuç olarak oksijen boşlukları içeren elektrotlar, hidrojen evrimi reaksiyonunu çok daha düşük aşım gerilimlerinde ve çok daha yüksek akımlarla gerçekleştiriyor.
Reaksiyon Enerjileri İçin Basit Kuralları Yeniden Düşünmek
Metal elektrotlarda kimyagerler genellikle reaksiyon enerjileri, aktivasyon bariyerleri ve uygulanan voltaj arasında düzenli lineer ilişkilerden yararlanır. Yazarlar, polaronlar devreye girdiğinde bu kuralların TiO2 üzerinde bozulmaya başladığını gösteriyor. Yüzeyde hidrojen bağlama enerjisi artık potansiyelle düzgünce değişmiyor; onun yerine yeni polaron durumları devreye girerken eğrilerde kırılmalar ve bükülmeler oluşuyor. İlginç bir şekilde, bu basit voltaj–enerji bağlantısı başarısız olsa da, reaksiyon bariyerlerini reaksiyon enerjilerine bağlayan daha genel bir ilişki hâlâ geçerli kalıyor. Bu, polaronların ne zaman ve nerede ortaya çıktığını dikkatle hesaba katarak, bu yarıiletken yüzeylerde hidrojenin ne kadar hızlı oluşacağını hâlâ öngörebileceğiniz anlamına geliyor.
Daha Akıllı, Ayarlanabilir Katalizörler Tasarlamak
Genel olarak sonuçlar, TiO2'nin performansının yalnızca bileşimiyle sabitlenmediği, işletme potansiyeliyle aktif olarak ayarlanabileceği bir katalizör olarak resmediyor. Oksijen boşlukları gibi yerleşik kusurları voltaj kontrollü polaron oluşumuyla birleştirerek, yüzey hidrojen evrimi için yoğun, yüksek aktiviteye sahip iletken bölgeler ağına dönüştürülebilir. Gayri uzman bir okuyucu için ana mesaj, ucuz yarıiletken malzemelerin bu küçük yük ceplerini işletme sırasında "açıp" yönlendirmeyi öğrenerek asil metallere rakip olacak şekilde iyileştirilebileceği; bu da verimli, ölçeklenebilir hidrojen üretimi ve diğer temiz elektrokimyasal teknolojiler için yeni yollar açıyor.
Atıf: Wu, T., Guo, X., Zhang, G. et al. Potential-dependent polaron formation activates TiO2 for the hydrogen evolution reaction. Nat Commun 17, 2104 (2026). https://doi.org/10.1038/s41467-026-68892-5
Anahtar kelimeler: hidrojen evrimi reaksiyonu, titanyum dioksit, polaronlar, yarıiletken elektrokataliz, oksijen boşlukları