Clear Sky Science · tr
Anti-TLR2 immünoterapisi, fare ve insan modellerinde α-sinükleinin nörondan oligodendrosite geçişini değiştirir
Bu araştırma neden önemli
Multipl sistem atrofisi (MSA), Parkinson’a benzer hareket bozukluklarını denge ve otonomik yetmezliklerle (örneğin kan basıncı düşmeleri) birleştiren, nadir fakat hızla ilerleyen bir beyin hastalığıdır. Hekimler semptomları hafifletebiliyor, ancak hastalığın ilerleyişini şu anda yavaşlatamıyorlar. Bu çalışma, yanlış katlanmış bir proteinin beyin hücreleri arasında nasıl yayılarak beynin "kablolama yalıtımına" zarar verdiğini ortaya koyuyor ve hedefe yönelik bir antikor tedavisinin hayvan ve hücre modellerinde bu süreci kesintiye uğratabildiğini gösteriyor. Çalışma, semptomları tedavi etmek yerine bir gün MSA’nın gidişatını değiştirebilecek somut, ilaç benzeri bir stratejiye işaret ediyor.
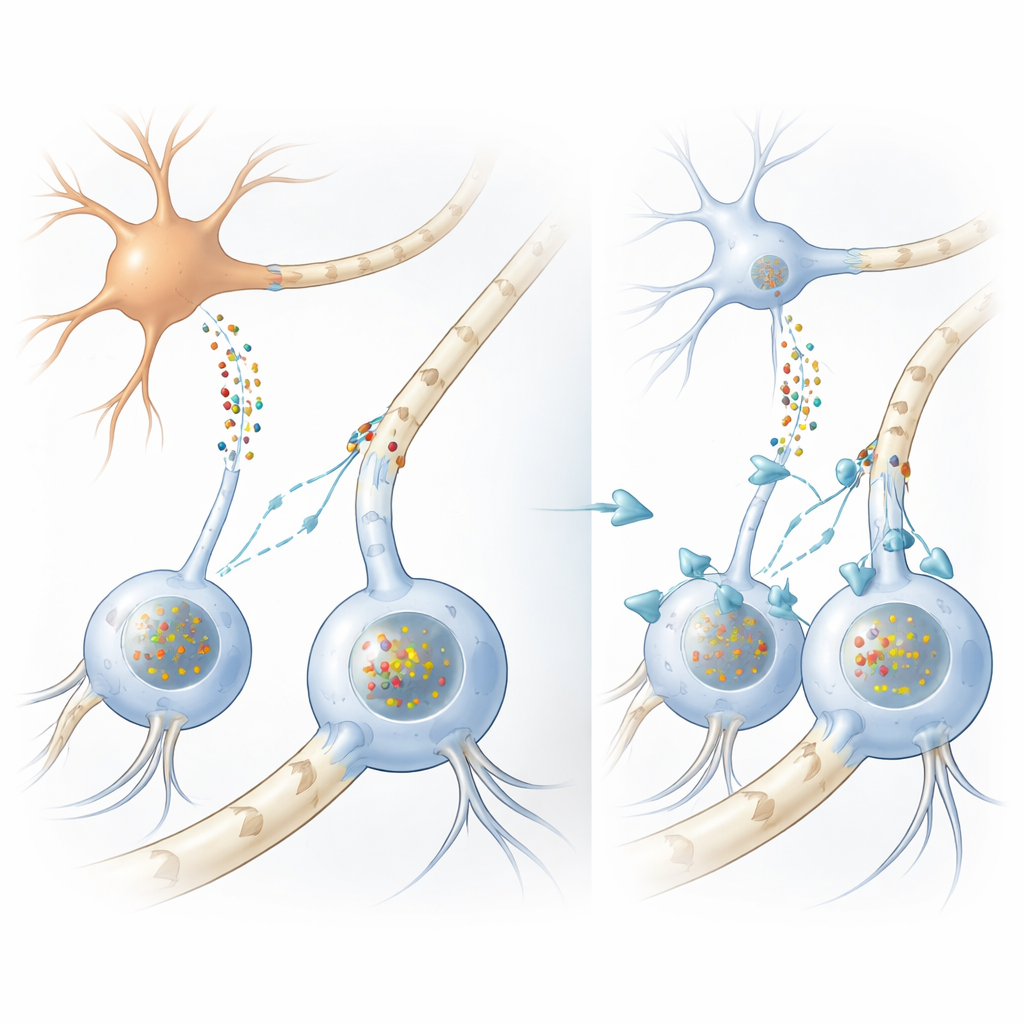
Beyin kablolaması nasıl bozuluyor
Parkinson hastalığı da dahil olmak üzere birçok hareket bozukluğunda alfa-sinüklein adlı proteinin pıhtılaşmaları sinir hücreleri içinde birikir. Ancak MSA’da en dikkat çekici kümeler destek hücreleri olarak adlandırılan oligodendrositler içinde oluşur; bu hücreler normalde sinir liflerini elektriksel iletimi hızlandıran yağlı miyelin kılıflarla sararlar. İlginç şekilde, oligodendrositler kendileri çok az alfa-sinüklein üretir; bu da uzun süredir devam eden bir bilmecedir: bu hücrelerdeki büyük protein birikintileri nereden geliyor? Yazarlar önce insan beyin örnekleri ve geniş ölçekli RNA analizleri kullanarak oligodendrositlerin gerçekten nöronlara kıyasla çok daha az alfa-sinüklein ürettiğini doğruladılar ve zararlı proteinin dışarıdan gelmesi gerektiği fikrini güçlendirdiler.
Proteinin nörondan destek hücresine geçişi
Bunu test etmek için ekip birkaç tamamlayıcı model kurdu. Kültürlerde, insan nöral kök hücrelerinden oligodendrosit-benzeri hücreler yetiştirdiler ve bunları büyük miktarda alfa-sinüklein salacak şekilde tasarlanmış nöron-benzeri hücrelerden toplanan sıvıyla muamele ettiler. Destek hücreleri bu proteini aldı ve MSA beyinlerinde görülen glial inklüzyonlara yakından benzeyen pıhtılar geliştirdi; aynı kimyasal etiketler ve yardımcı proteinleri taşıyordu. Araştırmacılar, insan mutant alfa-sinükleini yalnızca nöronlarda üreten bir fare soyunda incelediklerinde, bu hücrelerin insan geni ifade etmemesine rağmen beyaz cevherde oligodendrositler içinde yine insan protein pıhtıları buldular. Bu deneyler bir arada, alfa-sinükleinin nöronlardan oligodendrositlere geçebildiğini ve orada hastalığa benzer inklüzyonlar oluşturabildiğini gösteriyor.
Hücresel yüzeydeki kapı
Sırada bilim insanları proteinin oligodendrositlere nasıl girdiğini sordular. Önceki çalışmalar, bağışıklık algılayıcısı Toll-benzeri reseptör 2 (TLR2) yüzeyde nöronlarda ve mikroglialarda alfa-sinüklein için bir bağlanma yeri olarak rol aldığını göstermişti. MSA beyinlerinden alınan gen ifadesi veri setlerini inceleyen ekip, hastalardaki oligodendrositlerin kontrol grubuna kıyasla olağandışı derecede yüksek düzeyde TLR2 taşıdığını ve daha yüksek TLR2 seviyelerinin miyelin temel protein gibi miyelinle ilişkili genlerin daha düşük ifadesiyle bağlantılı olduğunu buldu. Bu ilişki birkaç bağımsız Parkinson veri setinde görünmedi; bu da oligodendrositlerin TLR2 aracılığıyla alfa-sinükleine olan duyarlılığının tüm sinüklein bozukluklarının genel bir özelliği değil, MSA’ya özgü bir özellik olabileceğini düşündürüyor.
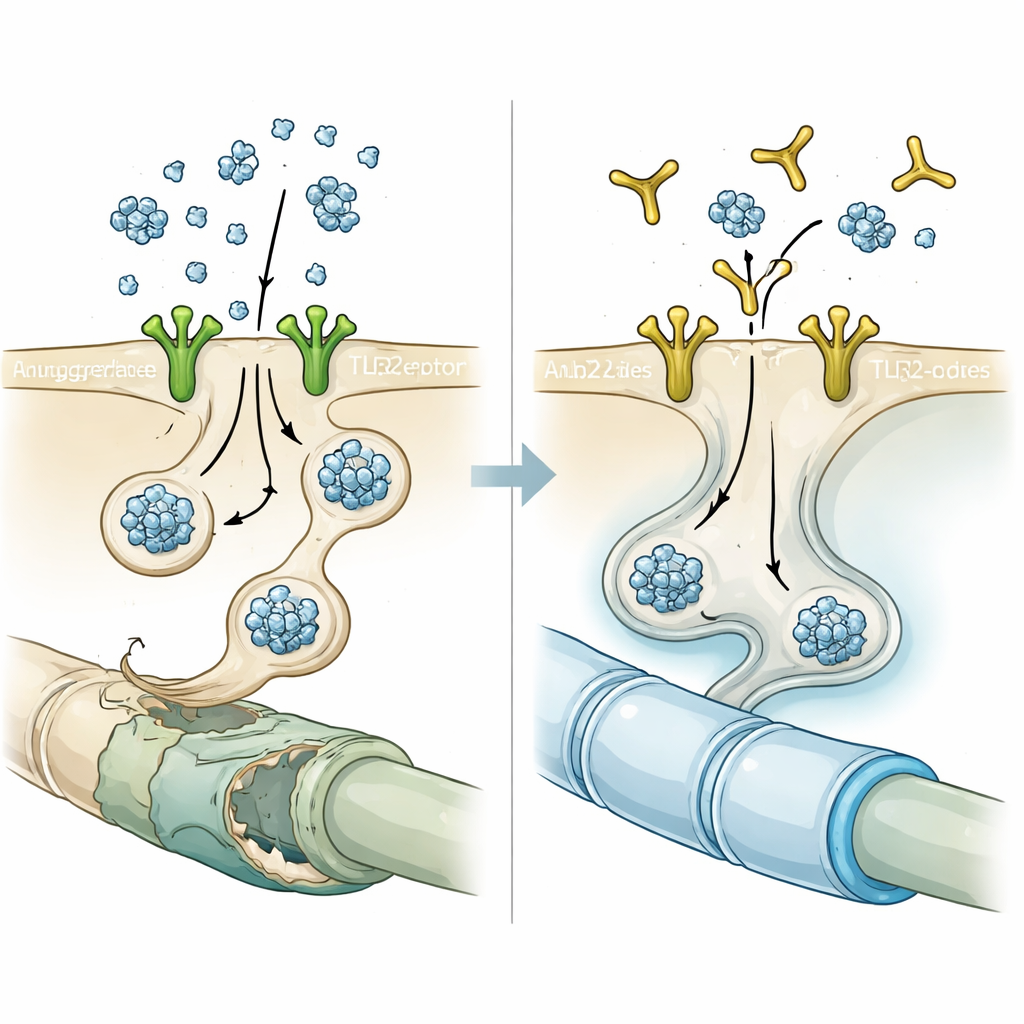
Antikorla kapıyı kapamak
Bu ipucuyla donanmış olarak araştırmacılar, TLR2’ye bağlanıp onun aktivasyonunu engelleyecek şekilde tasarlanmış NM-101 adlı antikoru test ettiler. Hücre kültürlerinde, oligodendrositleri nöron kaynaklı alfa-sinüklein eklemeden kısa süre önce NM-101 ile ön işlemeye tabi tutmak, inklüzyon benzeri pıhtıların sayısını ve yoğunluğunu belirgin şekilde azalttı. Nöronal alfa-sinükleini aşırı üreten veya önceden oluşmuş alfa-sinüklein fibrilleri enjekte edilen farelerde, haftalık NM-101 infüzyonları beyaz maddede toplanmış proteinleri azalttı, mikroglia ve astrositlerden kaynaklanan iltihabi yanıtları yatıştırdı ve oligodendrositler içinde kaspaz-1 adlı iltihaplayıcı bir enzimin aktivasyonunu düşürdü. Tedavi edilmiş hayvanlar daha uzun yaşadı ve motor testlerde daha iyi performans gösterdi; bu da antikorun koruyucu etkilerinin yalnızca mikroskobik bir merak değil, fonksiyonel olarak anlamlı olduğunu öneriyor.
Hasarlı yalıtımı kurtarmak
Oligodendrositler beynin miyelin yapıcıları olduğundan, ekip alfa-sinüklein transferinin miyeline zarar verip vermediğini ve TLR2 engellenmesinin yardımcı olup olmayacağını inceledi. Nöron-diyere kondisyonlanmış alfa-sinükleine maruz kalan insan kökenli oligodendrositlerin tek hücre RNA dizilemesi, olgun, miyelin üreten bir durumdan geniş çapta uzaklaşıp daha olgunlaşmamış, progenitör-benzeri bir profile kayma gösterdi; birçok kilit miyelin geni aşağı doğru düzenlenmişti. Lazerle yakalanmış oligodendrositlerin gen ifadesi çalışmaları, MSA hastalarından ve fare modelinden alınan örneklerde ortak bir imza ortaya koydu: miyelin oluşturma ve sürdürmeyle ilişkili genlerin azalmış ifadesi. Elektron mikroskop altında, alfa-sinüklein farelerinde beyaz maddede daha ince, düzensiz miyelin kılıfları görüldü. NM-101 tedavisi bu değişikliklerin birçoğunu tersine çevirdi, miyelini kalınlaştırdı, miyelin proteinlerinin seviyelerini geri döndürdü ve oligodendrosit olgunlaşması için gerekli genlerin ifadesini normalize etti.
Gelecekteki tedaviler için ne anlama geliyor
Çalışma açık bir anlatıyı destekliyor: MSA’da nöronlar tarafından üretilen alfa-sinüklein, oligodendrositlerin yüzeyindeki TLR2 aracılığıyla bu hücrelere yayılabilir; orada biriktikçe iltihaplanmayı tetikler, hücrelerin gelişimsel programını bozar ve beyindeki kablolamanın miyelin kaplamasını aşındırır. TLR2’yi hedef alan bir antikorla engellemek, araştırmacıların bu olay zincirini farelerde ve insan hücre modellerinde kesmesine, toksik inklüzyonları azaltmasına, iltihabı yatıştırmasına, miyelini onarmasına ve hayatta kalma ile hareket kabiliyetini iyileştirmesine olanak sağladı. NM-101’in kendisi insanlarda hâlâ titiz testlere ihtiyaç duysa da, çalışma TLR2-bağımlı protein transferini MSA-benzeri patolojinin merkezi bir itici gücü olarak tanımlıyor ve anti-TLR2 immünoterapisini bu yıkıcı hastalığı yavaşlatma veya önleme konusunda umut verici bir strateji olarak öne çıkarıyor.
Atıf: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Anahtar kelimeler: multipl sistem atrofisi, alfa-sinüklein, oligodendrositler, miyelin hasarı, immünoterapi