Clear Sky Science · tr
Ölen hücrelerden nükleositoz yoluyla nukleer DNA çıkararak cGAS-IFN-I tepkileri
Bağışıklık Sistemimiz Ölülerden Gelen DNA’yı Nasıl Okuyor
Hücrelerimiz enfeksiyon, kanser veya günlük yıpranma sırasında öldüğünde, artıklarının çok fazla iltihaplanmaya yol açmadan temizlenmesi gerekir. Bu çalışma, bağışıklık hücrelerinin şaşırtıcı bir şekilde ölen hücrelerin çekirdeklerine tünel açıp DNA’yı çekebildiğini ve bunu tehlike sinali olarak kullanabildiğini ortaya koyuyor. Bu gizli temizleme-ve-uyarı sisteminin anlaşılması antiviral ilaçlar, otoimmünite, kanser tedavileri ve ilaç yan etkileri hakkındaki düşüncelerimizi değiştirebilir.
Bağışıklık Hücreleri İçinde Gizli Bir DNA Alarmı
Hücrelerimiz çekirdek veya mitokondride güvenli şekilde paketlenmiş olması gereken DNA’yı—hücre sıvısında yanlış yerde bulunan DNA’yı—algılayan cGAS adlı bir sensör içerir. cGAS böyle bir DNA ile karşılaştığında, tip I interferonları üreten güçlü bir alarm programını açar; bu proteinler antiviral ve bağışıklık düzenleyici olarak anahtar görevler görür. Bilim insanları virüslerin genetik materyallerini hücrelere sokarak bu yolu tetikleyebildiğini ve kendi DNA’mızın da bazen sızarak otoimmün hastalığa yol açabildiğini biliyordu. Ancak temel bir bilmece kalıyordu: özellikle ölü hücrelerden gelen büyük miktarda kendi DNA’mız, hücresel “mide” denen lizozomlarda sindirilmeden nasıl cGAS’a ulaşabiliyordu?
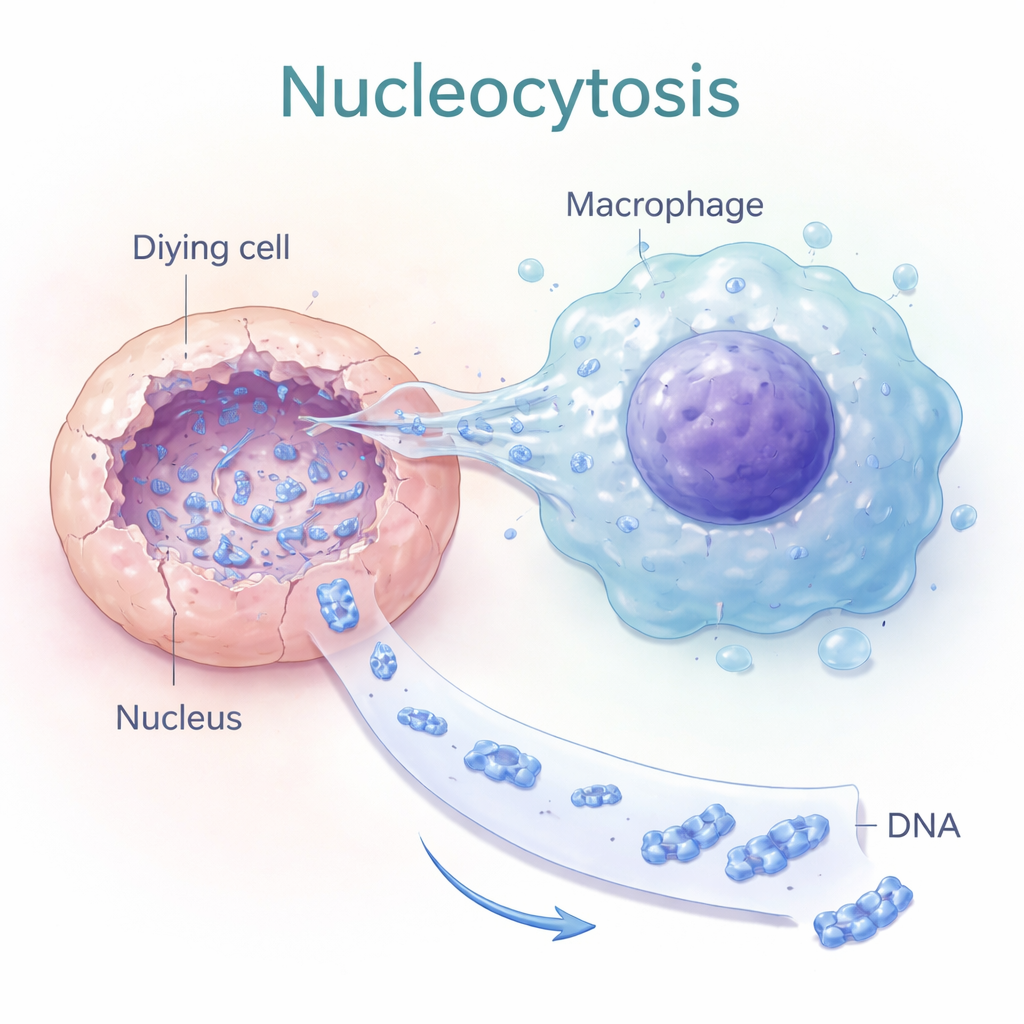
Nükleositoz: Ölü Hücre Çekirdeklerine Tünelleme
Yazarlar “nükleositoz” adını verdikleri bir süreç keşfettiler; burada belirli makrofajlar—normalde artık yutarak temizleyen bağışıklık hücreleri—çok daha hedefe yönelik bir davranış sergiliyor. Bütün bir ölü hücreyi yutmak yerine, ölen hücrenin çekirdeğine doğrudan ince, parmak benzeri çıkıntılar uzatıyorlar. Canlı hücre görüntülemesi, ölen hücrenin çekirdeğinde DNA yoğunluğunun azalırken, bağlı makrofaj içinde arttığını gösterdi; bu da nukleer DNA’nın aktif olarak çıkarıldığını gösteriyor. Bu aktarım hücrenin iç iskeleti (aktin) ve hücre şekliyi kontrol eden sinyal moleküllerine bağlıydı; bu da nükleositozun pasif bir sızıntı değil, amaçlı mekanik bir davranış olduğunu düşündürüyor.
Antiviral İlaçlar DNA Alarmını Ne Zaman Açıyor
COVID-19 pandemisi sırasında hidroksiklorokin gibi ilaçlar yaygın şekilde antiviral olarak sınandı, ancak bunların vücuttaki kesin etkileri belirsiz kaldı. Araştırmacılar hidroksiklorokin ve birkaç ilişkili “katyonik amfifilik” ilacın cGAS–STING–interferon yolunu güçlü şekilde aktive edebildiğini, fakat yalnızca bir makrofaj alt grubunda bunu yaptığını buldu. Bu ilaçlar lizozomların pH’ını yükselterek ve proteinlerdeki yağlı etiketlerin parçalanmasına yardımcı olan PPT1 adlı enzimi bloke ederek lizozomları bozuyor. Bu birleşik etki, bazı hücreleri calreticulin adlı proteinin çekirdekte biriktiği özel bir ölüm biçimine itiyor. Makrofajlar daha sonra öncelikle bu calreticulin-zengin çekirdeklere doğru çıkıntılar uzatıyor, nükleositoz yoluyla DNA’yı çıkarıyor ve sadece birkaç hücrede yoğun interferon üretimini tetikleyerek tüm vücudu değil, güçlü bir yerel antiviral sinyal oluşturuyor.
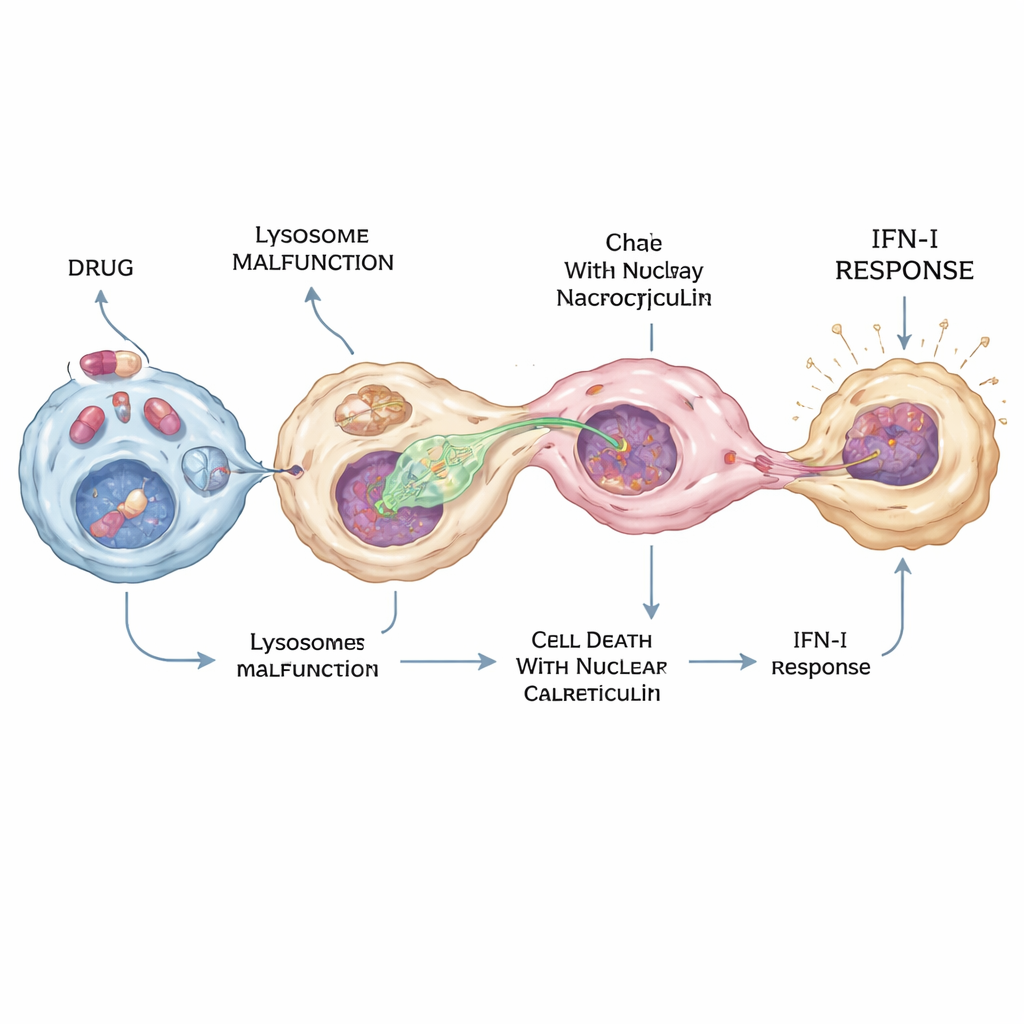
Yerel Savunmadan Hastalık ve Yan Etkilere
Hücre kültürleri ve fare akciğerleri üzerinde çalışarak ekip, ilaçla muamele edilmiş makrofajların büyük ölçüde yerel kalan—örneğin akciğerde—STING-bağımlı bir interferon yanıtını başlatabileceğini gösterdi; bu yanıt sistemik hale gelmiyor. Bu, hidroksiklorokin benzeri ilaçların bazı dokularda antiviral veya anti-tümör faydalar gösterebilmesini ama uzun süre kullanıldığında göz veya kalp toksisitesi gibi organ-spesifik yan etkilere neden olabilmesini açıklamaya yardımcı olur. Aynı nükleositoz süreci, ölü hücreler ve lizozomal stres bir araya geldiğinde otoimmün veya inflamatuvar hastalıklara makul bir katkı sağlayabilir; çünkü kendi DNA’mızın cGAS alarmını doğrudan açması için bir yol sunuyor.
Gelecek Tedaviler İçin Neden Önemli
Bir uzman olmayan için temel mesaj şudur: bağışıklık hücreleri ölü hücreleri sadece pasifçe yutmaz; çekirdeklerinden DNA’yı aktif şekilde çıkarıp yardım çağırmak için sinyal olarak kullanabilirler. Bu nükleositoz yolu, kendi DNA’mızın güçlü antiviral savunmaları odaklanmış, yerel bir biçimde nasıl güvenli şekilde aktive edebileceğini açıklar; aynı zamanda lizozomları veya PPT1’i bozan ilaçların istemeden bu anahtarı nasıl açabileceğini de vurgular. Nükleositozu artırmayı ya da azaltmayı—daha akıllı antiviral ve kanser tedavileri tasarlayarak veya otoimmün hastalıkta istenmeyen kendi-DNA sinyallerinden kaçınarak—öğrenerek, araştırmacılar bu yeni keşfedilmiş mekanizmayı daha güvenli, daha hassas tedaviler için kullanmayı umuyor.
Atıf: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Anahtar kelimeler: nükleositoz, cGAS-STING, hidroksiklorokin, tip I interferon, makrofajlar