Clear Sky Science · tr
Primerizasyon ve yayılma: bağışıklık kontrol noktası inhibisyonu ile birleştirildiğinde alfa- ile beta-parçacık yayan radyofarmasötiklerin farelerde farklı bağışıklık etkileri
Radyasyonu Bağışıklığın Dostu Hale Getirmek
Kanser hekimleri giderek daha fazla tümörlerle savaşmak için bağışıklık sistemini görevlendirmeye çalışıyor, ancak birçok kanser bu ilaçları görmezden geliyor veya onlara direnç gösteriyor. Bu çalışma güncel bir soruyu soruyor: farklı hedeflenmiş radyasyon türleri yalnızca tümörleri doğrudan küçültmek için değil, bağışıklık sistemini daha etkin hale getirmek için de kullanılabilir mi — ve radyoaktif ilacın seçimi bu “eğitimin” nasıl işlediğini değiştirir mi?
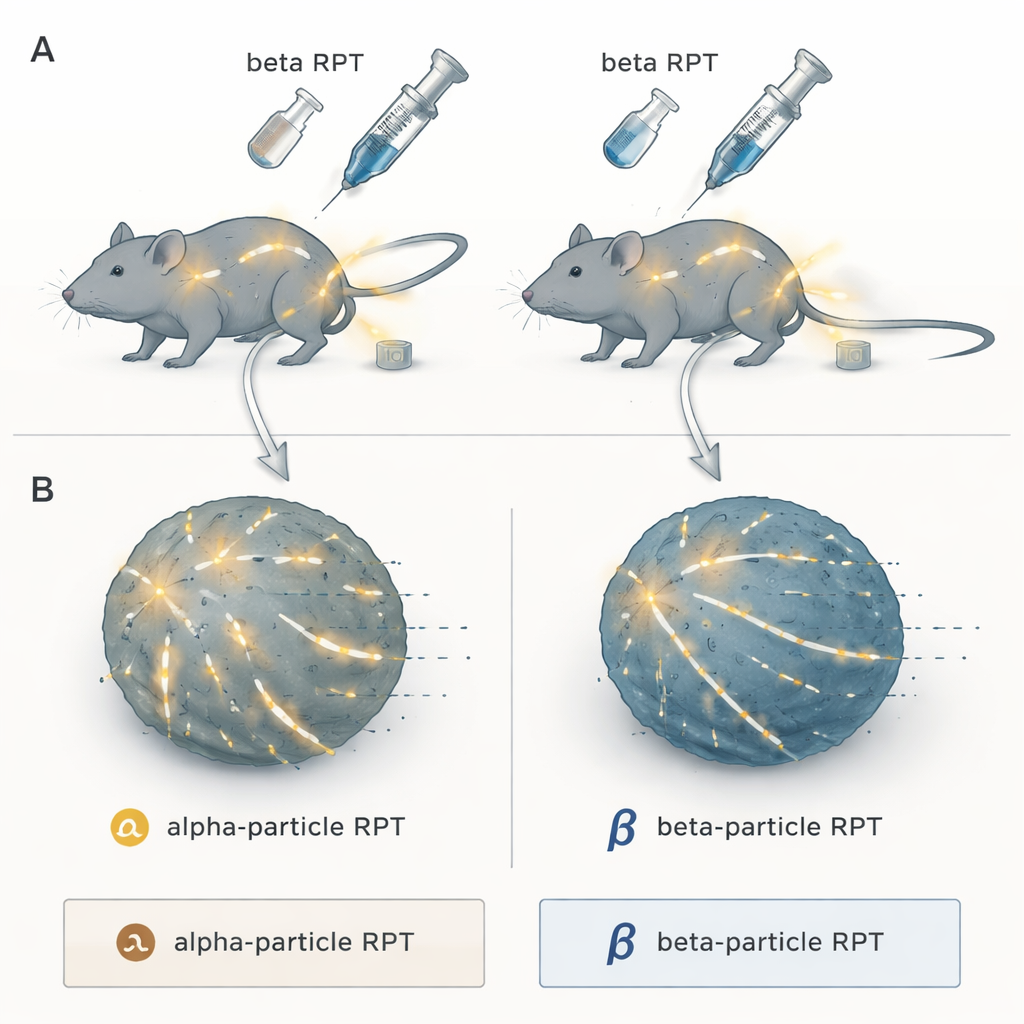
İki Tür Hassas Radyasyon
Araştırmacılar, radyofarmasötik tedaviye odaklandı: radyoaktif bir yükün doğal olarak tümörlere yerleşen bir moleküle bağlandığı bir “ara ve yok et” yaklaşımı. Enjekte edildiğinde vücutta dolaşır ve yayılmış hastalıkta sıradan dış ışın tedavisinin kolayca ulaşamadığı kanser bölgelerine radyasyon gönderir. Ekip iki ana kategoriyi karşılaştırdı: çok kısa mesafede son derece yoğun enerji patlamaları salan alfa-parçacık yayıcılar ve dokuda daha uzaklara ulaşan daha düşük yoğunluklu radyasyon yayan beta-parçacık yayıcılar. Hepsi aynı tümör hedefleyen bileşik NM600'e bağlanmıştı, böylece farklı olan tek şey hedefleme değil, radyasyon türü oldu.
Radyasyonun Bağışıklık Kontrol Blokörleriyle Eşleştirilmesi
Tek başına anti-PD-L1 ve anti-CTLA4 gibi kontrol noktası inhibitörleri bağışıklık hücrelerinin frenini kaldırabilir, ancak tümör zaten bağışıklık sistemi tarafından görüldüğünde en iyi şekilde çalışırlar. Melanom, prostat kanseri ve kolorektal kanserin fare modellerinde bilim insanları, alfa- veya beta-tabanlı NM600’den dikkatle seçilmiş düşük bir radyasyon dozu verdiler; bunun yanında ya tek başına ya da kombinasyon halinde kontrol noktası inhibitörleri uyguladılar. Ayrıca bağışıklık ilaçlarının ne zaman verildiğini—radyoterapiden önce, hemen sonra veya çok sonra—değiştirerek zamanlamanın tümör büyümesi, sağkalım ve uzun vadeli bağışıklık belleği gibi sonuçları nasıl etkilediğini gözlemlediler.
Beta Radyasyon Parladığında: Mevcut Yanıtı Güçlendirmek
İmmunoterapiye zaten yanıt veren “bağışıklık-sıcak” bir kolorektal kanser modelinde en iyi sonuçlar beta-yayan NM600’den geldi; özellikle bağışıklık ilaçları erken veya orta bir dönemde başlatıldığında. Tümörler daha fazla küçüldü, farelerin yaşam süreleri uzadı ve iyileşen hayvanlar aylar sonra aynı kanser yeniden verildiğinde sıklıkla bunu reddetti. Ayrıntılı bağışıklık profillemesi, beta-tabanlı tedavi artı kontrol noktası blokajının yeni bir yanıt oluşturmak yerine zaten var olan bir yanıtı çoğalttığını gösterdi: mevcut tümör-spesifik katil T hücreleri genişledi, daha aktive oldu ve daha fazla savaş sinyali üretti. Kısacası, beta yayıcılar devam eden bir bağışıklık yanıtını yaymada çok iyiydi.
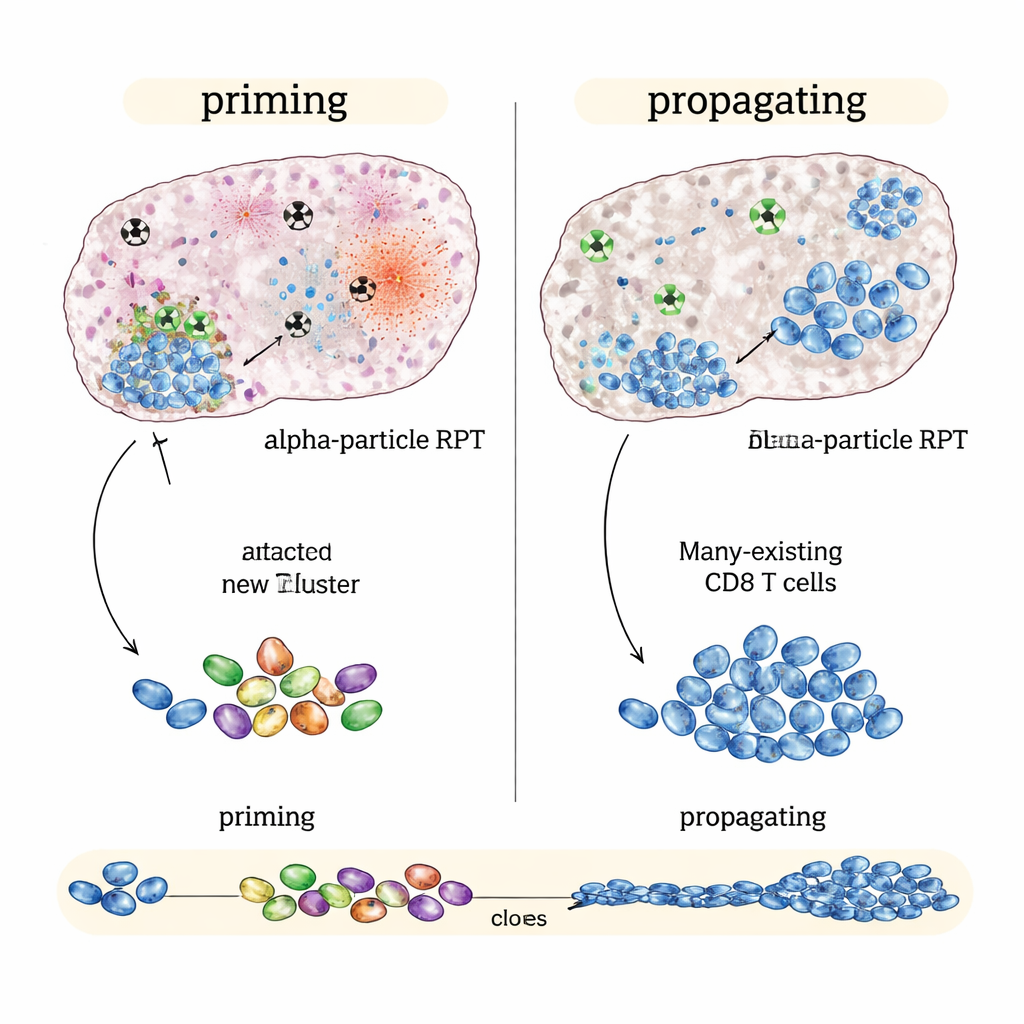
Alfa Radyasyon Parladığında: Yeni Bir Bağışıklık Saldırısı Tetiklemek
Buna karşılık, bağışıklık‑soğuk tümörlerde — kontrol noktası ilaçlarına neredeyse yanıt vermeyen bir melanom ve bir prostat kanseri modeli gibi — alfa-yayan versiyon aynı ortalama tümör dozunda beta yayıcılardan daha iyi performans gösterdi. Alfa-tabanlı tedavi artı bağışıklık ilaçları tümör büyümesini daha çok yavaşlattı ve sağkalımı daha da uzattı. Tek hücreli genetik analizler bunun nedenini önerdi: alfa radyasyonu yoğun, lokalize hasara yol açtı ve tümör içinde güçlü alarm sinyalleri ürettiği görülürken yakınındaki bağışıklık yapıları nispeten korunuyordu. Bu desen, daha geniş ve daha çeşitli T hücre tepkileri ile ve yeni tümör-tanıyan katil T hücrelerinin oluştuğuna ve uzun ömürlü bellek hücreleriyle ilişkilendiğine dair işaretlerle bağlantılıydı—bu, sırf çoğaltma değil, bağışıklık primerizasyonunun kanıtıydı.
Radyasyon Türü ve Zamanlamasının Neden Önemli Olduğu
Farklı modellerde, kontrol noktası inhibitörlerinin erken veya orta zamanlaması—radyasyonun tetiklediği tehlike sinyallerinin zirve yaptığı zamanlarla yaklaşık çakışan—gecikmiş tedaviden sürekli olarak daha iyi performans gösterdi. Bu çalışma pratik bir fikir veriyor: bağışıklık sistemi tarafından zaten görülen kanserlerde, düşük doz beta-tabanlı radyofarmasötikler kontrol noktası inhibitörleriyle birlikte mevcut bağışıklığı yaymak ve güçlendirmek için ideal ortak olabilir. Daha bağışıklık dirençli kanserlerde ise yüksek etkili alfa yayıcılar taze T hücre yanıtlarını primerize etmek ve “soğuk” bir tümörü “sıcak” hale getirmek için daha uygun olabilir. Hastalar için bunun anlamı şudur: tüm radyoaktif ilaçlar birbirinin yerine kullanılamaz; izotopu ve zamanlamayı tümörün bağışıklık kişiliğine göre eşleştirmek kombinasyon radio‑immünoterapisini hem daha etkili hem de daha kalıcı kılabilir.
Atıf: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Anahtar kelimeler: radyofarmasötik tedavi, alfa vs beta radyasyon, bağışıklık kontrol inhibitörleri, kanser immünoterapisi, tümör mikroçevresi