Clear Sky Science · tr
Hücrelerde kararlı etkileşim merkezleri oluşturmak için peptid koaservatlarının teslimi
Hücre İçinde Yeni “İş İstasyonları” Kurmak
Hücrelerimiz, enerji üretimi veya stres yanıtları gibi önemli işlerin yürütüldüğü küçük çalışma alanlarıyla doludur. Zamanla ya da hastalık durumunda bu doğal iş istasyonları işlevini yitirebilir. Bu çalışma, laboratuvarda üretilen kısa peptidlerden oluşan basit damlacıklar kullanarak canlı hücrelere yepyeni “etkileşim merkezleri” eklemenin bir yolunu araştırıyor. Bu sentetik merkezler belirli proteinleri yakalayabilir, yoğunlaştırabilir ve hatta onları yok etmeye yardımcı olabilir; bu da gelecekteki terapiler ve hücre mühendisliği için yeni stratejiler öneriyor.
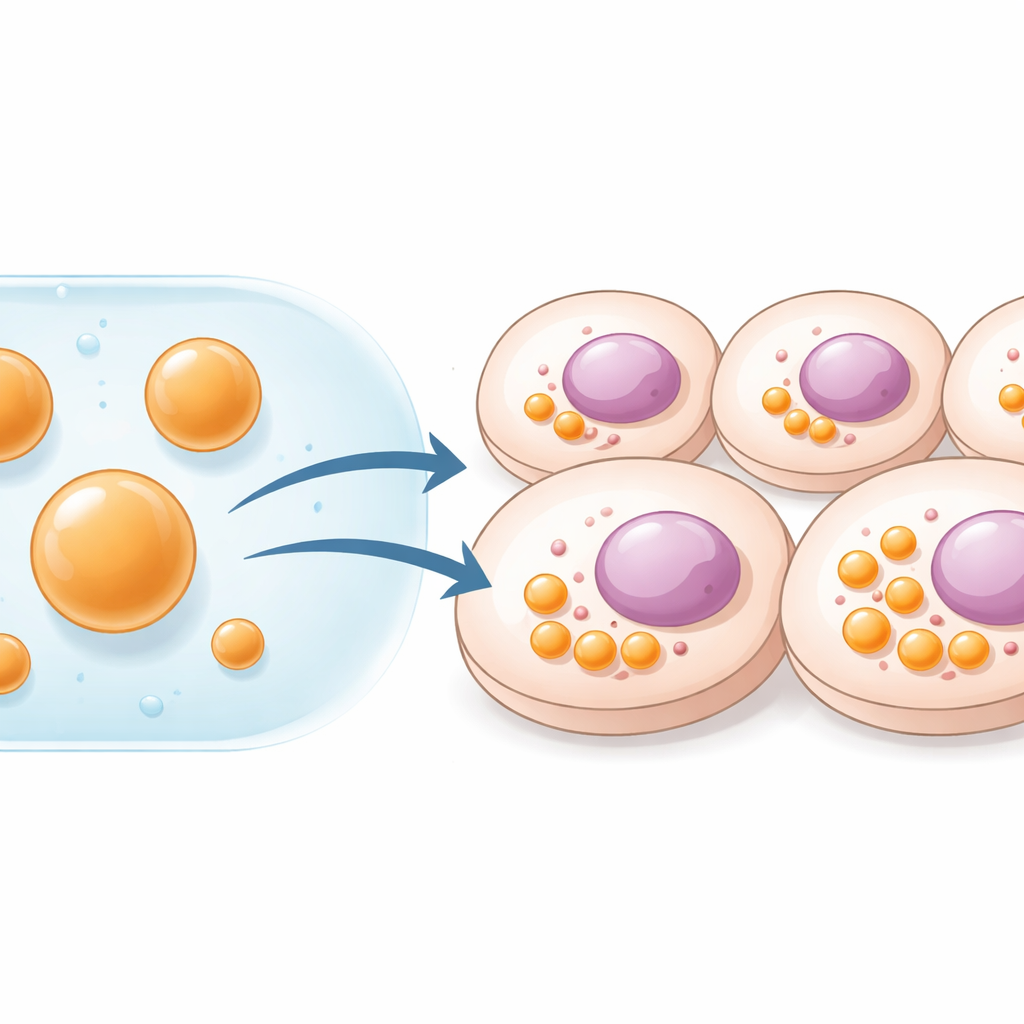
Hücrelerin Özel Çalışma Alanlarına Neden İhtiyacı Var?
Hücreler, farklı görevleri ayrı bölümlere ayırarak düzeni korur. Bazıları mitokondri gibi zarlarla çevrilidir; diğerleri ise belli protein ve RNA’ların kümelenmesiyle oluşan daha yumuşak, damla benzeri yapılardır. Bu akışkan damlacıklar veya kondensatlar, belirli biyokimyasal yolları hızlandıran veya kapatan reaksiyon merkezleri gibi davranır. Bilim insanları daha önce böyle bölümleri, hücreleri özel iskelet proteinleri üretmeye zorlayarak tasarlamışlardır. Bu yöntem güçlü olsa da gen teslimi gerektirir ve hücrenin üretebileceği madde miktarıyla sınırlıdır. Bu çalışmanın yazarları DNA’ya tamamen başvurmadan hazır yapılı bölümleri hücre dışında hazırlayıp, bunları kararlı, mikron boyutlu damlacıklar olarak doğrudan teslim etmeyi hedeflediler.
Kararlı Merkezler Oluşturan Peptid Damlacıkları
Araştırma ekibi kısa, düzensiz peptidler olan HBpep ve redoks-duyarlı bir varyantı HBpep-SA ile çalıştı. Hafif asidik koşullar altında bu peptidler çözünmüş halde kalırken, pH yaklaşıp fizyolojik seviyelere getirildiğinde—veya sıcaklık düşürüldüğünde—yumuşak, jel benzeri damlacıklara ayrışırlar; bunlar yaklaşık 1–5 mikrometre çapındadır. Peptid konsantrasyonunu ayarlayarak araştırmacılar damlacık boyutunu ve sayısını kontrol edebildiler. Floresan teknikler kullanarak, damlacık içindeki peptid moleküllerinin yavaş hareket ettiğini gösterdiler; bu, seyrekliklerine rağmen seyrelme ve işlemeye dayanacak kadar sağlam bir jel durumuna işaret ediyor. İnsan kanser hücreleri, fare melanom hücreleri ve primer insan bağışıklık hücreleri kültürlerine eklendiğinde, damlacıklar verimli biçimde alındı ve sitoplazmada birikti. Özellikle daha büyük damlacıklar en az beş gün boyunca bütünlüklerini korudular ve canlı hücreler içinde uzun ömürlü sentetik organeller gibi davrandılar.
Merkezleri Yükleme ve Hedefleme
Bu merkezlerin işe yaraması için yükleri tutup düzenlemeleri gerekir. Araştırmacılar önce model bir protein olan GFP’ye kısa bir HBpep kaynaklı etiket ekleyerek yüklemeyi iyileştirdiler. Bu etiket GFP’nin damlacıklara güçlü biçimde ayrılmasını teşvik etti ve ilginç bir şekilde yüzey yakınında yoğunlaşarak çekirdek-kabuk organizasyonu yarattı. Ardından hedeflenen proteinlere sıkı bağlanan küçük antikor benzeri proteinler olan nanobodies damlacıkların içine gömüldü. GFP’ye bağlanan bir nanobody, merkezlerin tüplerde ve hücre içinde GFP’yi seçici olarak yakalamasını sağladı. Peptid jeli nispeten yoğun olduğundan, başlangıçta yakalanan GFP çoğunlukla damlacık yüzeyinde toplandı. Ancak iç yapı kısmen gevşetildiğinde—ya redoks koşullarını değiştirerek ya da damlacıkların çevreleyen endozomal zarlardan kaçmasına yardımcı olarak—GFP iç kısımlara da nüfuz etmeye başladı. Hücrelerde endozomal kaçışı teşvik eden kimyasal yardımcılar, hedeflerini başarıyla toplayan merkezlerin oranını büyük ölçüde artırdı.
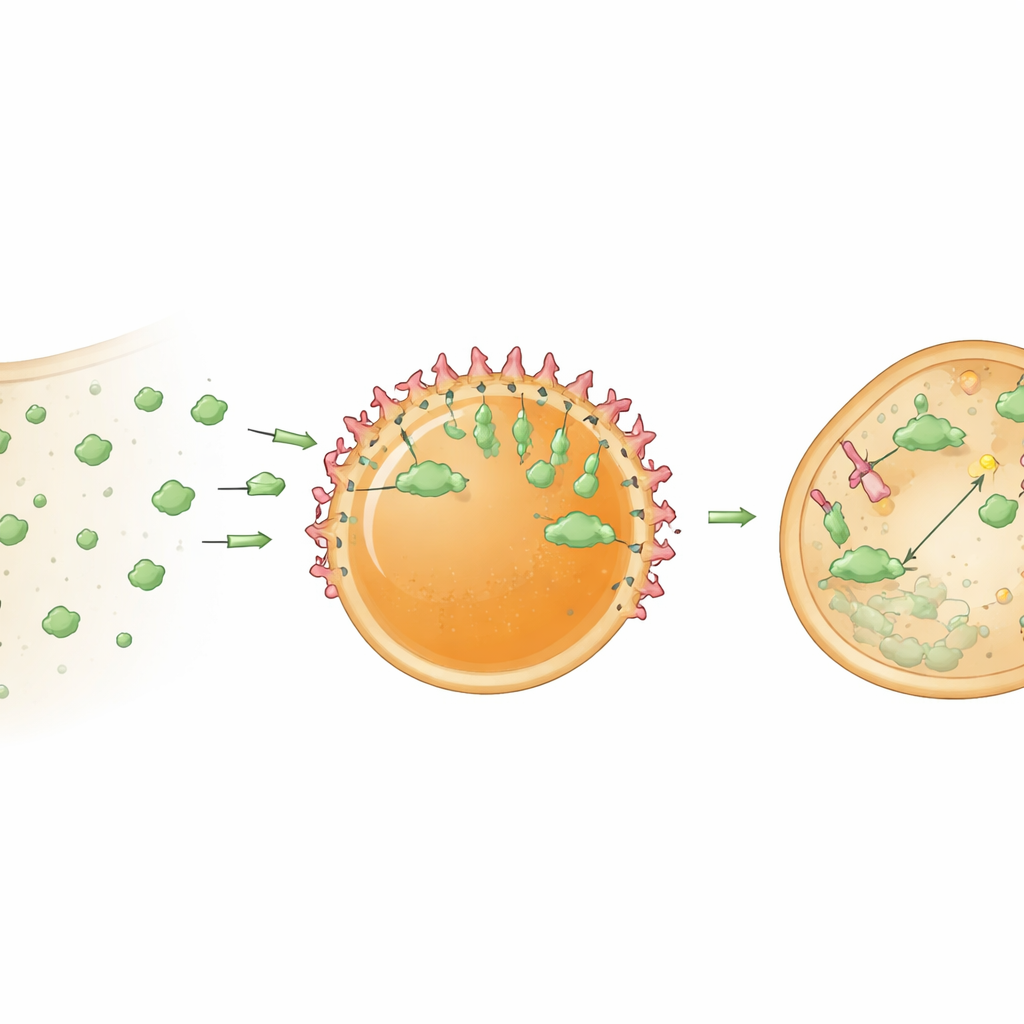
Merkezleri Protein Öğütücülere Dönüştürmek
Yazarlar daha sonra bu merkezleri pasif tuzaklardan aktif işleme merkezlerine yükselttiler. Damlacıkları, hedefe bağlanan bir nanobody ile hücrenin atık-bertaraf mekanizmasına proteinleri işaretleyen bir enzim adaptör parçasını birleştiren bir füzyon protein olan bioPROTAC ile yüklediler. Bu “degradosom” damlacıkları, GFP’yi kararlı olarak eksprese eden hücrelere verildiğinde, sitozolik GFP seviyeleri bir gün içinde yaklaşık yüzde 78 azaldı. Sadece nanobody içeren kontrol merkezleri GFP’yi tutsa da genel seviyesini belirgin şekilde düşürmedi; bu da güçlü azalmanın basit yakalamadan ziyade hedefe yönelik yıkımdan kaynaklandığını doğruladı. Bulgular, bioPROTAC’ların yoğunlaştırılmış bir mikroçevre içinde kümeleşmesinin, serbestçe dağılmış oldukları duruma göre çok daha etkili hale getirdiğini gösteriyor.
Gelecekteki Terapiler İçin Anlamı
Daha basit bir ifadeyle, bu çalışma bilim insanlarının bir tüpte peptid tabanlı damlacıklar üretip bunları özel protein araçlarla doldurabildiğini ve ardından bu yapıların yaşayan hücrelere teslim edildiğinde yeni, uzun ömürlü organeller gibi davrandığını gösteriyor. Bu sentetik merkezler doğal proteinleri seçici olarak çekebilir ve yıkım makineleriyle donatıldıklarında seçilmiş hedefleri aktif biçimde hücreden uzaklaştırabilir. Platformun hücrenin genlerini değiştirmemesi ve taşıyabileceği bileşenler konusunda modüler olması, zararlı proteinleri temizleme veya hatalı sinyalleşmeyi yeniden yönlendirme gibi hücresel davranışları onarmak veya yeniden yazmak için yeni programlanabilir “iş istasyonları” kurarak tedavilere giden bir yol açıyor.
Atıf: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Anahtar kelimeler: sentetik organeller, peptid koaservatları, hücresel iç teslimat, protein yıkımı, hücre mühendisliği