Clear Sky Science · tr
NatA, ribozomal polipeptit tünel çıkışında çok faktörlü komplekslere katılır
Hücrelerin yeni proteinleri doğdukça nasıl ince ayarladığı
Her saniye hücreleriniz ribozom adı verilen küçük makinelerde binlerce yeni protein üretir. Her protein zinciri ortaya çıktıkça doğru şekilde budanmalı, etiketlenmeli ve katlanmalıdır; aksi halde yanlış davranarak hastalıklara katkıda bulunabilir. Bu çalışma, N-terminal asetilasyon adlı ana etiketleme sistemlerinden birini inceliyor ve merkezi bir enzim kompleksi olan NatA'nın yeni proteinlerin ribozomdan çıktığı yerde birkaç ortakla birlikte nasıl çalıştığını gösteriyor. Bu koreografiyi anlamak, hücrelerin protein fabrikalarını sorunsuz çalışır halde nasıl tuttuğunu açıklamaya yardımcı olur.
Önemli küçük kimyasal etiket
Çoğu protein yaşamına aynı ilk yapı taşı olan metiyonin amino asidiyle başlar. Genellikle bu başlangıç metiyonini çıkarılır ve asetil grubı adı verilen küçük bir kimyasal etiketle değiştirilir. Proteinin çok ucuna (N-terminusuna) eklenen bu etiket, proteinin ne kadar süre yaşadığını, hücre içinde nereye gittiğini ve nasıl işlev gördüğünü etkileyebilir. İlk düzenlemeyi yönetmek için ribozom tünel çıkışında yer alan iki ana enzim tipi vardır: başlangıç metiyoninini kesen metiyonin aminopeptidazlar (MAP'ler) ve asetil etiketini ekleyen N-terminal asetiltransferazlar (NAT'lar). NAT'lar arasında NatA, insan hücrelerinde en çok iş yapan kompleks olup muhtemelen tüm proteinlerin yaklaşık %40'ını modifiye eder. Birçok protein aynı anda yapıldığından hücre bu enzimleri budama ve etiketlemenin hızlı ve doğru sırada gerçekleşmesi için düzenlemek zorundadır.
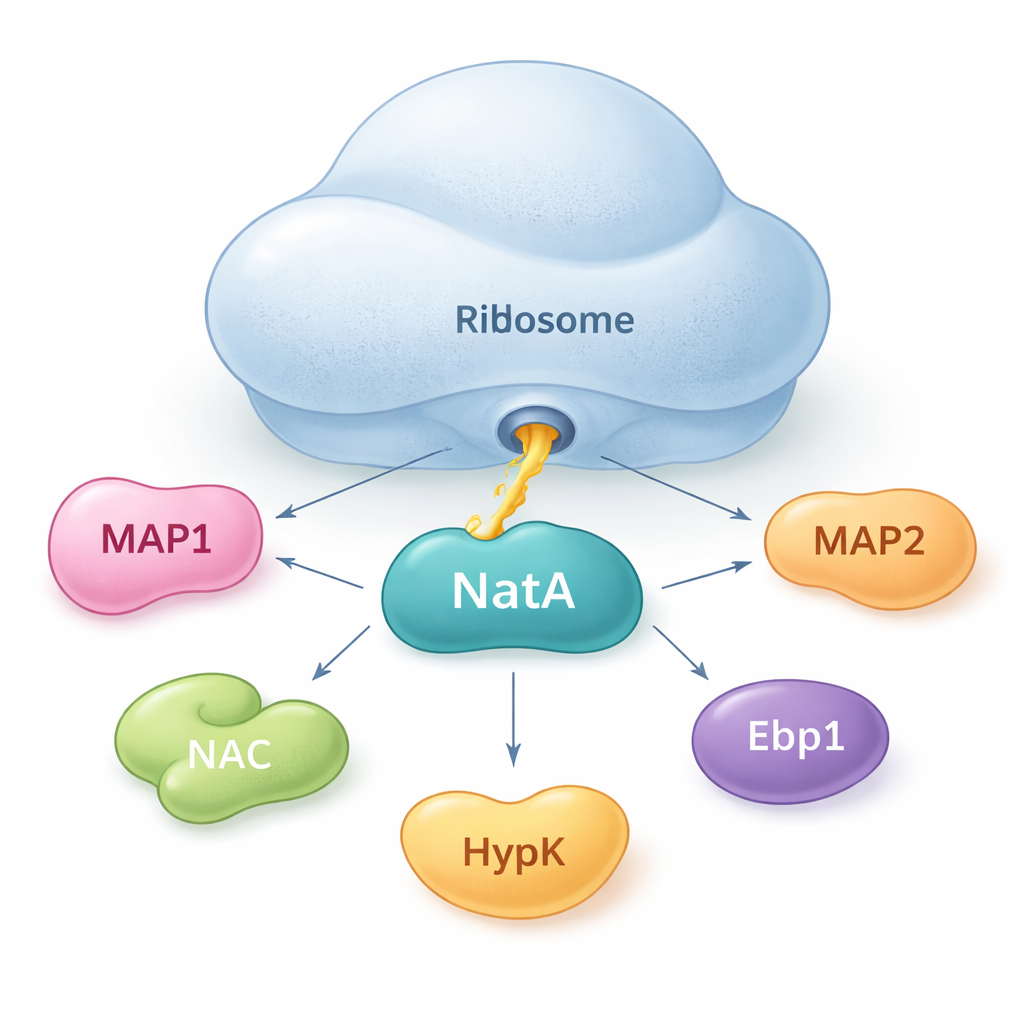
NatA: protein yardımcıları için bir buluşma noktası
Yazarlar NatA'nın tek başına hareket etmediğini gösteriyor. Bunun yerine NatA, ribozomda ve ribozom dışında bir araya getirdiği bir hub gibi davranır. Çözelti içinde hassas bağlanma ölçümleri kullanarak NatA'nın ribozom olmadan da MAP1, yeni oluşan polipeptid ile ilişkili kompleks (NAC), düzenleyici protein HypK ve başka bir enzim olan Naa50 ile sıkı kompleksler oluşturabildiğini buldular. NAC, NatA'yı MAP1'e köprüleyebilir; bu sayede kesme ve etiketleme adımları tek bir montaj içinde bağlanabilir. Ancak HypK, normalde NatA'nın aktivitesini azaltan bir faktör, NAC'in bağlanmasını engelleyebilir. Bu durum, hücrelerin ihtiyaçlarına bağlı olarak NatA'yı daha aktif, NAC-bağlı bir konfigürasyon ile kısıtlı, HypK-bağlı bir konfigürasyon arasında anahtarlayabileceğini önerir.
Tünel çıkışında ikinci bir kenetlenme noktası
Kryo-elektron mikroskopisi kullanarak, yani büyük molekülleri atomlara yakın ayrıntıda görüntüleyen bir teknikle, araştırmacılar NatA'nın ribozoma iki farklı pozisyonda bağlanabildiğini keşfettiler. Önceden bilinen bir site tünel çıkışından biraz uzakta dururken, yeni keşfedilen “proksimal” site NatA'nın katalitik çekirdeğini büyüyen protein zincirinin ortaya çıktığı noktaya çok yakın yerleştirir ve zincirin modifiye edilmek için kat etmesi gereken mesafeyi kısaltır. İlginç şekilde, her iki pozisyon aynı anda işgal edilebilir; yani aynı ribozom üzerinde iki NatA kompleksi bulunabilir. Uzak kopya iskelet ve çapa görevi görürken, proksimal kopya yeni proteinleri etiketlemek için en uygun yerde durur. İki NatA molekülü birbirine dokunur ve bu NatA'nın kendi kopyalarını çok-enzimli takımlara koordine edebileceğini gösterir.
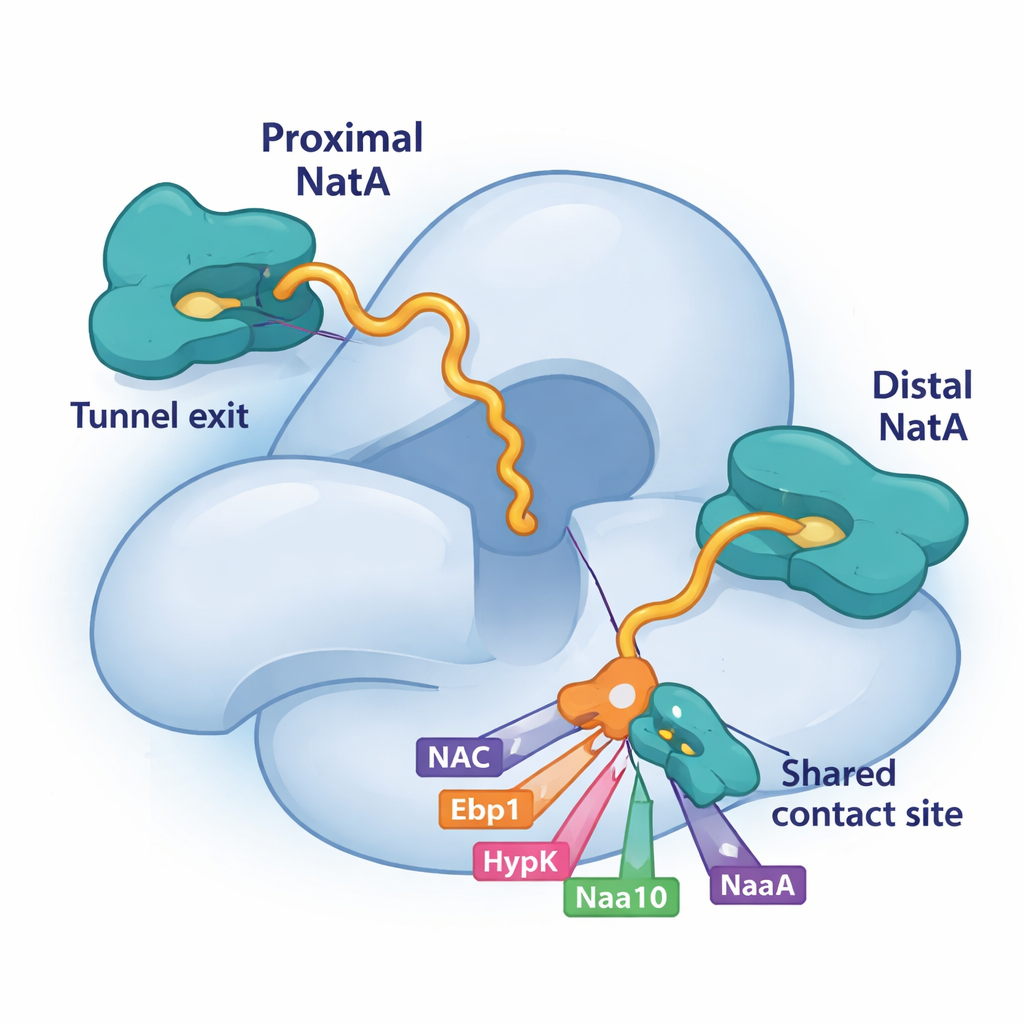
NatA üzerinde paylaşılan bir iniş yeri için rekabet
Bu bulmacanın kilit parçası büyük NatA alt birimi Naa15 üzerinde yer alan küçük bir oluk. Çalışma, NAC, HypK, Ebp1 ve hatta NatA'nın kendi katalitik alt birimi Naa10'un bir kuyruk bölgesinin, kısa heliksler kullanarak tam olarak Naa15 üzerindeki aynı yama üzerine tutunduğunu gösteriyor. Hepsi bu paylaşılan iniş yerine bağımlı olduğu için erişim için rekabet etmek zorundalar. HypK siteyi işgal ettiğinde, NatA'nın aktivitesini susturmakla kalmaz, aynı zamanda NatA'nın NAC ile eşleşmesini veya NatA–NatA dimerleri oluşturmasını da engeller. Bunun yerine NAC, psödo-enzim Ebp1 veya proksimal Naa10 bağlandığında, NatA'nın ribozomdaki pozisyonunu veya bağlantılarını yeniden şekillendirebilirler. Bu rekabetçi bağlanma, hücreye hangi ortakların herhangi bir anda NatA etrafında toplanacağını seçme konusunda esnek bir yol sağlar.
Bir trafik kontrolörü olarak psödo-enzim
Protein Ebp1 özellikle ilgi çekici. O, metiyonini çıkaran enzimlere benzese de katalitik aktiviteden yoksundur; bir “psödo-enzim”dir. Önceki çalışmalar Ebp1'in tünel çıkışına yakın ribozomda oturabildiğini ve uzun bir RNA segmentini sıkıştırabildiğini göstermişti. Bu çalışmada yazarlar, NatA ribozoma katıldığında Ebp1'in pozisyonunu değiştirip RNA'dan vazgeçtiğini ve bunun yerine kendi heliksini kullanarak NAC ve HypK'nın kullandığı aynı Naa15 bağlanma sitesini işgal ettiğini buluyor. Bu yeniden düzenleme, Ebp1'in doğrudan kimyasal işlem yapmadan yer tutucu veya düzenleyici olarak hareket edebileceğini; yerel RNA ortamını şekillendirebileceğini ve ardından MAP'lar ve NatA gibi aktif enzimlere kontrolü devredebileceğini düşündürür.
Bu moleküler kalabalık kontrolünün önemi
Uzman olmayan biri için heliksler ve bağlanma bölgeleri gibi ayrıntılar soyut gelebilir, ancak mesaj basit: hücreler proteinlerin doğduğu yerde yüksek derecede koreografili, çok adımlı bir kalite kontrol sistemi işletir. NatA bu sistemin merkezinde yer alır ve kritik bir kenetlenme yamasına hangi faktörlerin eriştiğine ve NatA'nın hangi ribozomal siteyi işgal ettiğine bağlı olarak farklı ortakları toplayıp bırakabilir. Bu esnek ağ, binlerce farklı protein için budama ve asetilasyonun doğru zamanlama ve sırayla gerçekleşmesini sağlamaya yardımcı olur. N-terminal işleme hatalarının gelişimsel bozukluklar, nörodejenerasyon ve kanserle ilişkilendirilmesi nedeniyle NatA ve ortaklarının nasıl bir araya geldiğini haritalamak, araştırmacılara erken protein işlemenin nasıl kontrol edildiğine ve bozulduğunda nasıl hedeflenebileceğine dair daha net bir yol haritası sunar.
Atıf: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Anahtar kelimeler: protein kalite kontrolü, N-terminal asetilasyon, ribozom tünel çıkışı, NatA kompleksi, ko-translasyonel modifikasyon