Clear Sky Science · tr
Bitki fukoziltransferazı FUT11, geçici bir oksokarbonyum ara ürün mekanizmasıyla katalizlemek için şeker kabul ediciyi bozar
Bitkiler proteinlerindeki şekerleri nasıl ince ayarlar
Hücrelerimizdeki ve bitkilerdeki proteinler genellikle katlanma biçimlerini, ömürlerini ve hangi ortaklarla etkileşebileceklerini yönlendiren karekod benzeri karmaşık şeker zincirleriyle süslenir. Bu çalışma, bu zincirlere küçük bir şeker olan fukozu ekleyen FUT11 adlı bitki enzimi üzerine odaklanıyor. FUT11’in atomik düzeyde tam olarak nasıl çalıştığını ortaya koyarak yazarlar şaşırtıcı bir numara gösteriyor: enzim, zorlu bir kimyasal adımı ilerletmek için şeker partnerini geçici olarak bozar. Bu sürecin anlaşılması sadece temel biyoloji için değil, aynı zamanda insanlarda istenmeyen bağışıklık tepkilerini tetiklemeyen daha güvenli bitki yapımı ilaçların tasarlanması için de önemlidir.
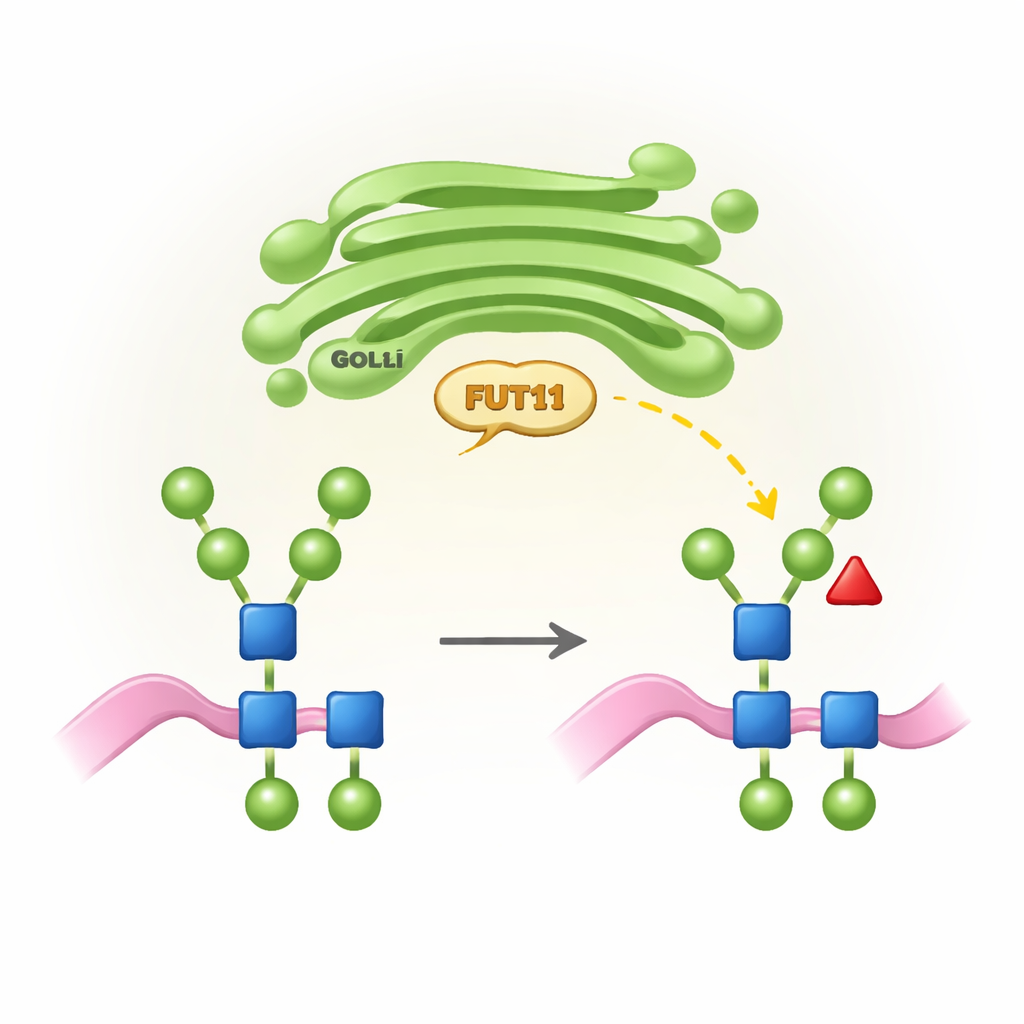
Bitkiye özgü şeker etiketleri ve neden önemli oldukları
Tüm yüksek organizmalar, proteinlerin belirli noktalarına şeker zincirleri (N-glikanlar) bağlamak için N-glikozilasyon adı verilen bir süreç kullanır. Hayvanlarda bu zincirler Golgi aygıtında yeniden düzenlenerek genellikle sialik asitlerle sonlanan ve belirli bir pozisyonda çekirdek fukozu taşıyan karmaşık yapılara dönüşür. Bitkiler ise farklı bir “tasarım kuralı” izler: bitki N-glikanları tipik olarak sialik aside sahip değildir ama çekirdek fukozunu farklı bir konumda (b11,3 olarak adlandırılan) taşır ve ayrıca ekstra bir ksiloza sahiptir. Bu bitkiye özgü özellikler normal büyüme ve üreme için esastır, fakat insan bağışıklık sistemi tarafından yabancı olarak algılanabilir. FUT11, bu çekirdek fukozunu yerleştiren kilit bitki enzimlerinden biridir ve aktivitesi hem bitki gelişimini hem de bitki kaynaklı terapötik proteinlerin insan vücudunda nasıl algılanacağını şekillendirir.
FUT11’in karmaşık şeker dallarında nerede çalışabileceğini haritalamak
FUT11’in neyi tanıdığını anlamak için araştırmacılar enzimi 144 farklı N-glikan yapısından oluşan bir mikroarray üzerinde test ettiler. FUT11’in şeker ağacının tek bir dalı olan sözde b11,3 kolu konusunda oldukça seçici olduğunu buldular—reaksiyonun ilerleyebilmesi için bu kolun uçta belirli bir yapı taşı (terminal N-asetilglukozamin veya GlcNAc) taşıması gerekiyordu. Aynı zamanda FUT11 diğer süslemelere hoşgörülüydü: merkezi mannoz bir bitkiye özgü ksiloz taşıdığında ve hatta çekirdeğin memeli pozisyonunda başka bir fukoz zaten eklenmiş olduğunda bile enzim çalışıyordu. Karşı dal (b11,6) çoğunlukla çözücüye açık ve enzimle zayıf temaslar kuruyor, bu da FUT11’in oradaki çeşitli modifikasyonlarla başa çıkabilmesini açıklıyor. Bu bağlanma tercihleri, bitkilerin karakteristik bir N-glikan yapısı seti üretmelerini açıklamaya yardımcı oluyor ve biyoteknoloji için bitki hücrelerini tasarlarken FUT11’in nasıl kullanılabileceğini veya kaçınılabileceğini gösteriyor.
Şekerleri kavrayıp konumlandırmak için benzersiz bir yapısal tasarım
X-ışını kristalografisi kullanarak ekip, FUT11’in şeker vericisi (GDP-fukoz) ve bir N-glikan kabul edicisine bağlı üç boyutlu yapısını çözdü. Enzim iki loplu bir “GT-B” mimarisine sahip: bir lop GDP-fukozu kavrarken, alışılmadık derecede ayrıntılı olan kabul edici lop —bitkiye özgü bir N-terminal alt bölümü de içeren— N-glikanın etrafını sarar. Disülfit köprüleriyle enzimin geri kalanına bağlı olan bu ekstra alt bölüm glikanın merkezi kısmını sabitleyip reaktif GlcNAc birimini vericiye doğru sunmaya yardımcı olur. Kritik amino asitlerin değiştirilmesi rollerini doğruladı: tek bir glutamatın (Glu158) değiştirilmesi aktiviteyi yok ederken, yakınlardaki iki kalıntının değiştirilmesi mühendislik yapılan insan hücrelerinde fukozilasyonu büyük ölçüde zayıflattı. Bu sonuçlar yapısal anlık görüntüleri gerçek hücresel işleve bağlayarak proteinin hangi bölümlerinin bağlanma ve kataliz için vazgeçilmez olduğunu gösteriyor.
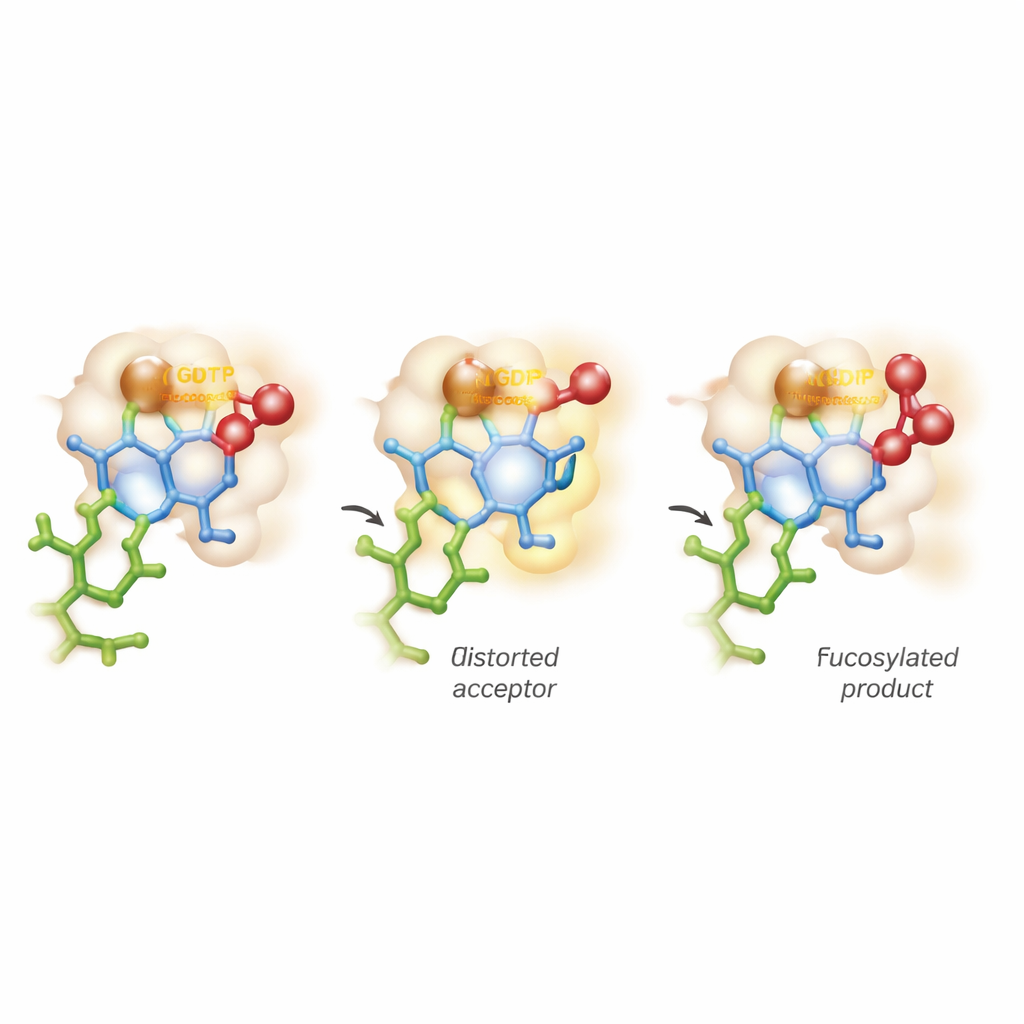
Şekeri bükmek ve iki reaksiyon yolu arasında dengede yürümek
En çarpıcı bulgu, kuantum mekaniği ve moleküler dinamikleri birleştiren ileri bilgisayar simülasyonlarından geliyor. Geleneksel görüşler, kabul edici şekerin kararlı, sandalye benzeri şeklini korurken enzimin yalnızca vericiyi aktive ettiğini varsayar. Burada FUT11 daha agresif davranıyor: Glu158 tarafından yönlendirilen etkileşimler, en içteki GlcNAc halkasını geçici olarak daha az konforlu bir buruşuk forma çarpıtıyor. Bu gerilmiş duruşta, kritik hidroksil grubu fukoz vericisine saldırmak için mükemmel şekilde hizalanmış oluyor. Hesaplamalar, GDP ile kimyasal bağ kırılmaya başlarken şeker üzerinde kısa ömürlü, pozitif yüklü bir “oksokarbonyum-benzeri” durumun ortaya çıktığını ve yeni bağın kabul ediciye tam olarak oluşmasından önce ortaya çıktığını gösteriyor. Bu, reaksiyonun ders kitaplarındaki SN1 veya SN2 kategorilerine tam olarak uymadığını, eşzamansız, neredeyse adım adım bir devamlılık boyunca ilerlediğini anlatıyor.
Gizli esneklik ve evrimsel yankılar
FUT11’i ilişkili bir insan enzimi olan FUT9 ile karşılaştırarak yazarlar, bitki enziminin zayıf da olsa farklı bir şeker motifini (LacNAc) modifiye edip Lewis X olarak bilinen bir yapı oluşturabileceğini buldular. Bu yan aktivite muhtemelen bitkilerde biyolojik olarak önemli değildir (çünkü Lewis X bitkilerde normalde görülmez), fakat benzer protein iskeletlerinin farklı şeker bağlamlarında çalışacak şekilde evrim boyunca nasıl yeniden amaçlanabileceğini vurguluyor. Çalışma, FUT11 ve akrabalarının N-glikanları tanımak için modüler bir çerçeveyi paylaştığını, ince ayarlarla bitki çekirdekleri ile hayvan antenleri arasındaki özgüllüğü kaydırdığını öne sürüyor.
Bu bükme numarasının bilim ve tıp için önemi
Bir arada ele alındığında, çalışma FUT11’in sadece iki şeker partnerini bir araya getirmediğini; kabul edici şekeri reaktif bir pozisyona aktif biçimde büküp kimyayı kısa ömürlü, yüklü bir ara ürün üzerinden yönlendirdiğini gösteriyor. Bir okuyucu için bu, proteindeki şekerin katı bir demirbaşı noktası değil, enzimin ihtiyaçlarına göre biçimlendirdiği esnek bir katılımcı olduğu anlamına gelir. Bu “konformasyonel kataliz”in yeni bakış açısı, enzimlerin hem hız hem de seçicilik nasıl sağladığını açıklamaya yardımcı olur ve glikozilasyon yollarını yeniden tasarlamak için bir yol haritası sunar. Pratik açıdan, FUT11’in bitki N-glikanlarını tam olarak nasıl tanıdığını ve değiştirdiğini bilmek, bağışıklık tetikleyen şeker desenlerini insan terapilerinde en aza indirmek veya istenen biyolojik özelliklere sahip tasarımcı glikoproteinler oluşturmak için tarım bitkilerinin ve bitki bazlı üretim sistemlerinin mühendisliğine rehberlik edebilir.
Atıf: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Anahtar kelimeler: bitki glikozilasyonu, fukoziltransferaz FUT11, N-glikanlar, enzim mekanizması, gliko-mühendislik