Clear Sky Science · tr
Dimerik OS9-SEL1L-HRD1 ERAD Çekirdek Kompleksinin Yapısal Temeli ve Patolojik Çıkarımları
Hücresel Temizlik Ekibi Mikroskop Altında
Her hücremizin içinde, genetik talimatları çalışan proteinlere dönüştüren yoğun bir fabrika bulunur. Her fabrikada olduğu gibi burada da hatalar olur. Proteinler yanlış katlandığında, sistemi tıkayabilir ve hastalığa katkıda bulunabilirler. Bu çalışma, hücrenin ana kalite kontrol makinelerinden biri olan SEL1L‑HRD1 kompleksine yaklaşıp onun ayrıntılı 3B yapısını ortaya koyuyor ve küçük genetik değişikliklerin bu mekanizmayı nasıl bozabileceğini ve potansiyel olarak insan hastalığına yol açabileceğini gösteriyor.
Hücrede Gizli Bir Konveyör Bandı
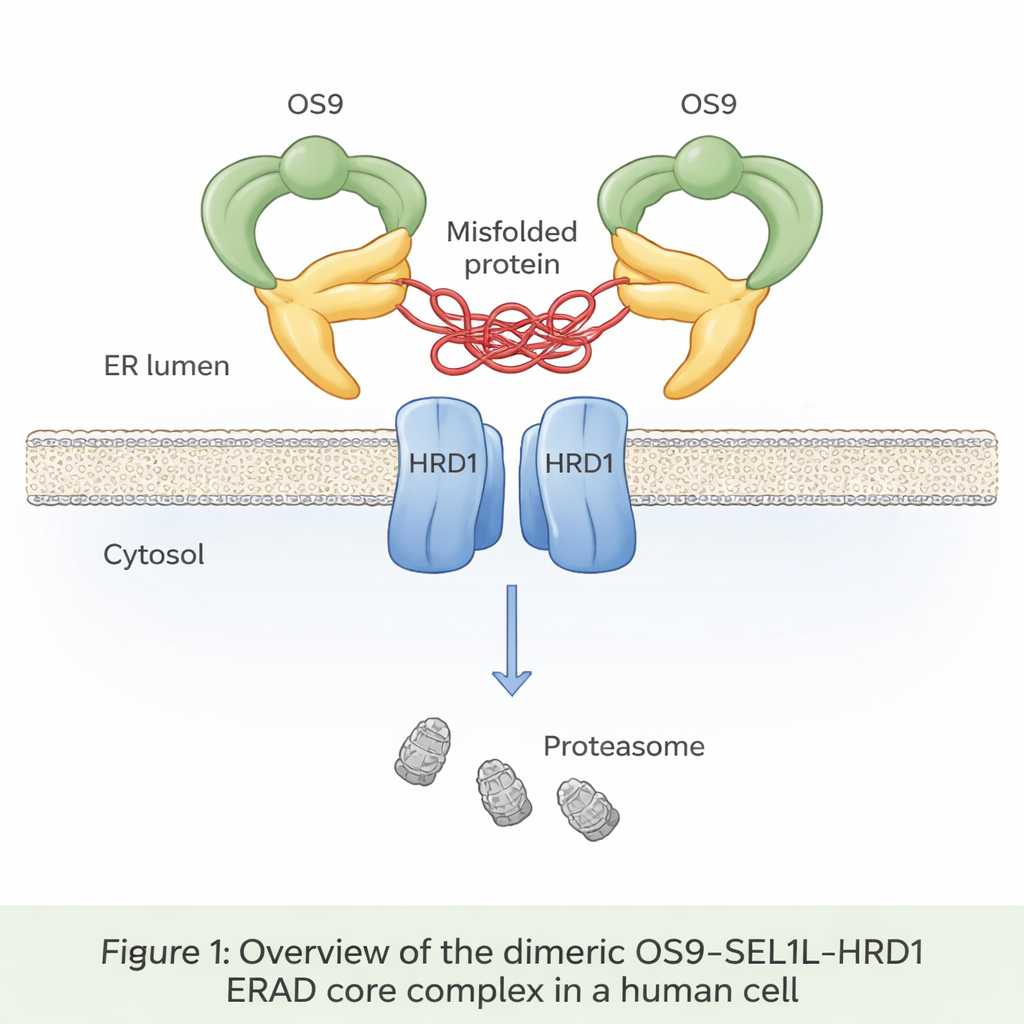
Tüm yeni üretilen proteinlerin üçte birine kadar olanı, katlandıkları ve denetlendikleri endoplazmik retikulum (ER) adlı bir bölmeye girer. Yanlış katlanmış proteinler normalde tanınır, ER’den geri çekilir ve ER ilişkilendirilmiş degradasyon (ERAD) olarak bilinen bir süreçte yok edilir. Bir ana ERAD yolunun merkezinde OS9, SEL1L ve HRD1 adlı üç protein bulunur. OS9 hatalı, şeker işaretli proteinleri algılayan bir sensör görevi görür; SEL1L iskelet görevi üstlenir; HRD1 ise yok edilmek üzere olan proteinleri, hücrenin atık imha birimleri olan proteazomlar tarafından tanınmaları için küçük ubiquitin bayrakları ile işaretler. Ancak şimdiye dek, bu üç parçanın insan hücrelerinde atomik ayrıntıda nasıl bir araya geldiği görülmemişti.
Çekirdek Makinenin Şeklini Ortaya Çıkarmak
Yazarlar, OS9‑SEL1L‑HRD1 kompleksini insan hücrelerinden saflaştırıp, neredeyse atomik çözünürlükte donmuş molekülleri görüntüleyen kriyo‑elektron mikroskopisini kullandılar. Kompleksin tek birimler halinde değil, esasen birbirine bağlı iki özdeş kopyadan oluşan bir dimer oluşturduğunu keşfettiler. ER lümen tarafında (ER’nin iç kısmı) iki OS9 ve iki SEL1L molekülü, yanlış katlanmış proteinleri kavramaya yönelik gibi görünen ortasında açıklık bulunan bir yengeç pençesi benzeri halka oluşturacak şekilde bir araya gelir. Zarın kendi içinde ise iki HRD1 molekülü eşleşerek ortak bir kanal oluşturur. Bu düzenleme “pençeyi” doğrudan HRD1 kapısının üzerine yerleştirir ve yanlış katlanmış proteinlerin ER lümeninden zardan geçip sitozolde degradasyona doğru ilerlediği sürekli bir yol yaratır.
Küçük Değişiklikler Büyük Bir Sistemi Nasıl Bozar
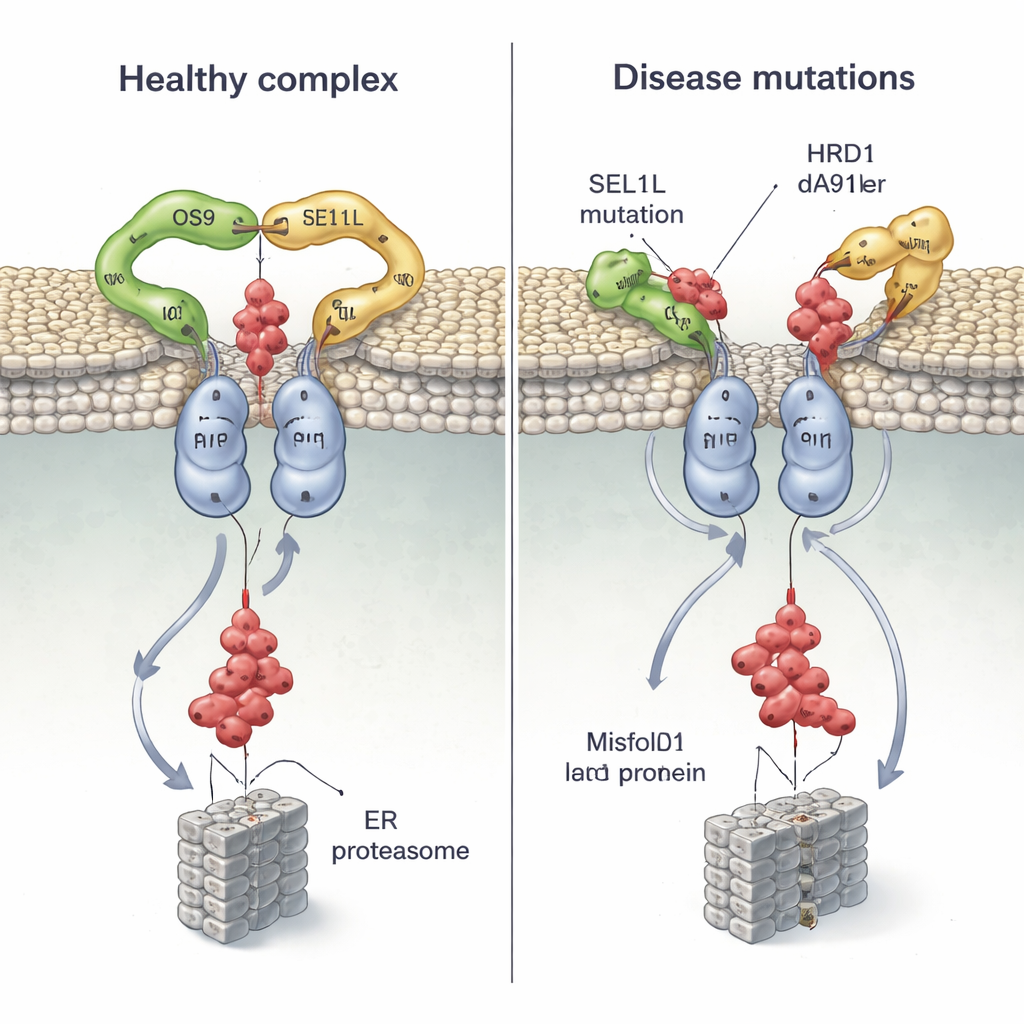
SEL1L ve HRD1’deki mutasyonların ağır nörogelişimsel ve diğer bozuklukları olan hastalarda bulunduğu bilindiğinden, ekip yapıya birkaç hastalıkla ilişkili varyantı yerleştirdi ve bunların hücrelerde nasıl davrandığını test etti. İki SEL1L mutasyonu, G585D ve S658P, sırasıyla OS9 ve HRD1 ile temas noktalarının tam üzerinde yer alır. Hücre deneylerinde G585D, SEL1L’nin OS9’a bağlanma yeteneğini neredeyse ortadan kaldırırken; S658P HRD1 ile bağını büyük ölçüde zayıflattı; her iki mutasyonun bir arada bulunması çekirdek kompleksini esasen bozdu, fakat diğer etkileşimleri etkilemedi. Sonuç olarak, hücreler yanlış katlanmış bir hormon öncülünü işaretleyip temizlemekte zorlandı ve hatalı proteinlerin birikmesine izin verdi.
Zar Kanalındaki Bir Hastalık Mutasyonu
Yapı ayrıca HRD1’in transmembran segment 3’ünün iki HRD1 molekülünün kanalı oluşturmak için buluştuğu ana arayüz olduğunu gösteriyor. Araştırmacılar belirli pozisyonlara sistein “tutacakları” yerleştirip kimyasal çapraz bağlama kullanarak bu bölgelerin canlı hücrelerde yakın temas halinde olduğunu doğruladılar; bu, HRD1’in gerçekten in vivo dimerleştiğini kanıtladı. Bu arayüzdeki tek, yüksek oranda korunan bir kalıntıyı (T93) bozduklarında, dimer çöktü ve ERAD aktivitesi çöktü; buna rağmen kompleks hâlâ OS9 ve SEL1L ile bir araya geliyordu. Daha sonra araştırmacılar, kalp ve akciğer sorunları olan bir çocukta bulunan yeni keşfedilmiş hasta varyantı HRD1 A91D’yi incelediler. Bu değişiklik de dimer arayüzünde yer alıyordu, HRD1 dimerleşmesini yaklaşık yarıya indirdi ve hatalı proteinlerin yok edilmesini ciddi şekilde bozdu; yine, ortak bağlanmaların genel düzenini bozmadı.
Protein Kalite Kontrolü ve Hastalıklara Yeni Bir Bakış
Yapı biyolojisini hücre bazlı testlerle birleştirerek, bu çalışma OS9‑SEL1L‑HRD1 kompleksinin eşleşmiş, dimerik bir makine olarak çalıştığını gösteriyor: hatalı proteinleri ER’den dışarı taşıyan ortak bir kanala bağlı pençe benzeri bir yakalayıcı. Pençenin kavrayışını gevşeten veya HRD1 çiftini kararsızlaştıran mutasyonlar yalnızca verimliliği biraz düşürmez—sistemi fiilen tıkayabilir, hasarlı proteinlerin birikmesine ve insan hastalıklarına katkıda bulunmasına izin verebilir. Uzman olmayanlar için temel mesaj şudur: DNA’mızdaki tek harflik değişiklikler bile temel hücresel makinelerin şeklini ince bir şekilde bozabilir ve beyin gelişimi, bağışıklık ve organ fonksiyonu üzerinde geniş etkiler doğurabilir.
Atıf: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Anahtar kelimeler: protein kalite kontrolü, endoplazmik retikulum, ERAD, SEL1L-HRD1 kompleksi, protein yanlış katlanması